
- •Вопрос 1.
- •Вопрос 2.
- •Вопрос 3.
- •Вопрос 4.
- •Вопрос 5.
- •Вопрос 6.
- •Билет 7.
- •Вопрос 8.
- •Билет 9.
- •Билет 10.
- •Билет 11.
- •Билет 12.
- •Билет 13
- •Билет 14.
- •Вопрос 15.
- •Билет 16.
- •Билет 17.
- •Вопрос 18.
- •Билет 19.
- •Билет 20.
- •Билет 21.
- •Билет 22.
- •Билет 23.
- •Билет 24.
- •Билет 25.
- •Билет 26.
- •Вопрос 27.
- •Билет 28.
- •Билет 29.
- •Билет 30.
- •Билет 31.
- •Билет 32. Донорные и акцепторные примеси в полупроводниках. Зонные диаграммы, примесных полупроводников, основные и не основные носители тока.
- •Билет 33.
- •Билет 34.
- •Билет 35.
- •Вопрос 36.
- •Вопрос 38.
Вопрос 6.
Типы кристаллических решеток. Решетки Бравею вывод формул для постоянной кубической решетки.
Типы кристаллических решеток:
Ионная (координационная)
Молекулярная (преобладает сила Ван-дер-Ваальса)
Атомные (ковалентные)
С водородной связью
Решетки Браве:
Триклинная
Моноклинная
Ромбическая
Тетрагональная
Гексагональная
Кубическая



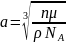
 - молярная масса
- молярная масса
ρ = плотность при н.у.
n = число одинаковых атомов, приходящихся на элементарную ячейку
 =
6,022
[моль-1
] - Число Авогадро
=
6,022
[моль-1
] - Число Авогадро
Билет 7.
Индексы Миллера для направления и плоскостей в кристаллической решетке. Определение межплоскостных расстояний в кристаллической решетке с помощью дифракции рентгеновских лучей. Формула Брэгга-Вульфа.
Индексы Миллера — кристаллографические индексы, характеризующие расположение атомных плоскостей в кристалле. Индексы Миллера связаны с отрезками, отсекаемыми выбранной плоскостью на трёх осях кристаллографической системы координат (не обязательно декартовой). Таким образом, возможны три варианта относительного расположения осей и плоскости:
плоскость пересекает все три оси
плоскость пересекает две оси, а третьей параллельна
плоскость пересекает одну ось и параллельна двум другим
Индексы направления прямой, проходящей через начало координат, является индекс первого узла, через которую проходит прямая и обозначается [ m n p ] это индексы плоскости (индексы Миллера).
Используя дифракцию рентгеновских лучей на кристалле можно с помощью формулы, закона Вульфа – Брэгга, определить расстояние D.
Условие Вульфа — Брэгга определяет направление максимумов дифракции упруго рассеянного на кристалле рентгеновского излучения. Имеет вид:
![]() ;
;
где d — межплоскостное расстояние, θ — угол скольжения (брэгговский угол), n — порядок дифракционного максимума, λ — длина волны.
Вопрос 8.
Виды связей в кристаллах, зависимость типа решетки от вида связи. Кристаллические решетки с плотной упаковкой атомов.
Кристалли́ческая решётка — пространственное периодическое расположение атомов или ионов в кристалле. Для описания кристаллической решётки достаточно знать расположение частиц в элементарной ячейке кристалла, повторением которой образуется вся кристаллическая решётка.
Виды связей:
Связь Ван-дер Вальса (играет роль взаимодействия атомов и молекул) Молекулярные решетки
Ионные связи (типичная связь в химических соединениях)
Валентные (ковалентная связь) Атомные решетки
Металлическая связь присуще для всех металлов
Водородная связь (Решетки с водородной связью)
В реальных решетках может присутствовать две и более связи но одна из них является основной.
Билет 9.
Виды дефектов в кристалле. Образование дефектов по Шаттке и по Френкелю, равновесная концентрация дифектов. Влияние точечных дефектов на механические и электрические свойства кристаллов.
Различают точечные дефекты, линейные, поверхностные и объемные.
По Шатке происходит полное испарение атома с поверхности с образованием вакансии. Происходит частичное испарение, т.е. атом переходит в состояние над поверхностью.
По Френкелю происходит диффузия дислокационного атома в другое междоузлие ( возникает вакансия).
Если имеется у нас n вакансия значит равновесная концентрация при температуре T и наличие N узлов равна

Влияние точечных дефектов на механические и электрические свойства кристаллов.
При точечных дефектах атомы примесей вызывают искажение кристаллов решетки.
Энергия образования вакансии. Равновесная концентрация вакансий в кристалле.
Энергия образования вакансии возникает в результате нарушения связей в кристаллической решетке при удалении атома из узла.
Равновесная концентрация вакансий:
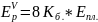
где
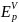 —
энергия образования одной вакансии,
—
энергия образования одной вакансии, —
постоянная Больцмана, T — абсолютная
температура. Формула показывает, что
концентрация вакансий должна сильно
зависеть от температуры.
—
постоянная Больцмана, T — абсолютная
температура. Формула показывает, что
концентрация вакансий должна сильно
зависеть от температуры.
Механизм диффузии по вакансиям. Коэффициент диффузии. Температурная зависимость коэффициента диффузии (уравнение Арениуса). Расчет длины диффузионного пути атома в кристалле.
Для диффузии вакансий и атомов необходимо два условия
Около атома должна находится вакансия, для образования которой необходимо энергия
Атом должен обладать энергией для перехода в эту вакансию (
 ) .
) .

Коэффицие́нт диффу́зии — количественная характеристика скорости диффузии, равная количеству вещества , проходящего в единицу времени через участок единичной площади при градиенте концентрации, равном единице.
Зависимость коэффициента диффузии от температуры в простейшем случае выражается законом Аррениуса:
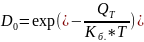 ,
,
где ![]() —
коэффициент диффузии [м²/с];
—
коэффициент диффузии [м²/с]; ![]() — энергия
активации [Дж];
— энергия
активации [Дж]; ![]() — универсальная
газовая постоянная [Дж/К];
— универсальная
газовая постоянная [Дж/К]; ![]() —
температура [K].
—
температура [K].
