
- •Опыты Резерфорда по рассеянию альфа-частиц
- •Планетарная модель атома
- •Постулаты Бора
- •Модель атома водорода по Бору
- •Опыты Франка и Герца
- •Волны де Бройля
- •Опыты по рассеянию электронов
- •Свойства волн де Бройля
- •Соотношение неопределенностей
- •Уравнение Шредингера
- •Принцип суперпозиции состояний
- •Операторы
Лекции 3,4
Опыты Резерфорда по рассеянию альфа-частиц
Большую роль в развитии представлений о строении атома сыграли опыты английского физика Э.Резерфорда по рассеянию альфа частиц в веществе. Альфа-частицы, как было показано опытами, являются дважды ионизованными атомами гелия.
При прохождении быстрых альфа-частиц в веществе большая часть испытывает отклонение на 2-3 градуса. Однако около 0,01% отклоняется на углы, достигающие 180 градусов. Все альфа-частицы, вылетающие из атомов данного сорта, имеют практически одинаковую скорость. Кроме того, они обладают большой массой. Это особенно важно, т.к. они не могут отклоняться при столкновении с электронами и по рассеянию альфа-частиц в веществе можно судить о распределении положительно заряженной материи в атоме.
О собый
интерес представляют опыты сотрудников
Резерфорда - Гейгера и Марсдена,
исследовавших рассеяние в тончайшей
металлической фольге (золото, серебро
и т.д.). Толщина фольги около 4 мкм.
Выделенный тонкий пучок от источника
альфа-частиц (И), рис.14, рассеивался при
прохождении через фольгу Ф. Рассеянные
альфа - частицы регистрировались по
вспышкам (сцинцилляциям) на экране,
укрепленном на объективе микроскопа
М. Экран покрывался флюоресцирующим
веществом. Микроскоп поворачивался для
определения количества частиц, рассеянных
под разными углами .
собый
интерес представляют опыты сотрудников
Резерфорда - Гейгера и Марсдена,
исследовавших рассеяние в тончайшей
металлической фольге (золото, серебро
и т.д.). Толщина фольги около 4 мкм.
Выделенный тонкий пучок от источника
альфа-частиц (И), рис.14, рассеивался при
прохождении через фольгу Ф. Рассеянные
альфа - частицы регистрировались по
вспышкам (сцинцилляциям) на экране,
укрепленном на объективе микроскопа
М. Экран покрывался флюоресцирующим
веществом. Микроскоп поворачивался для
определения количества частиц, рассеянных
под разными углами .
На угол более 90 градусов отклонялась примерно одна из 20000 частиц. Некоторые отклонялись почти на 180 градусов. Теоретическое исследование показало, что это не может являться результатом многократных отклонений на малые углы. Резерфорд пришел к заключению, что отклонение происходит в результате однократного взаимодействия альфа-частицы с положительным зарядом. Этот положительный заряд связан с большой массой, заключенной в очень малом объеме по сравнению с объемом атома в целом. В первом приближении (неподвижный атом) отклонение альфа-частицы можно описать как результат отталкивания от положительного заряда.
Следовательно, основная масса атома локализована в очень малом объеме, причем этот малый объем несет на себе весь положительный заряд атома. Исходя из этого, Резерфорд предложил ядерную (планетарную) модель атома.
Планетарная модель атома
В данной модели в центре атома находится положительно заряженное ядро, масса которого почти равна массе атома. Вокруг ядра под действием электрических сил движутся легкие электроны.
 Т.к.
кулоновские силы убывают с расстоянием
по тому же закону, что и силы ньютоновского
тяготения
Т.к.
кулоновские силы убывают с расстоянием
по тому же закону, что и силы ньютоновского
тяготения
![]() ,
то атом, по представлениям Резерфорда,
подобен солнечной системе. Поэтому и
возникло название - планетарная
модель, рис.15. Т.к. атомы электрически
нейтральны то при заряде +Ze вокруг ядра
должны двигаться Z электронов. Для
электрона, движущегося по определенной
орбите, наблюдается действие на него
центростремительной силы, которой в
данном случае является сила кулоновского
притяжения:
,
то атом, по представлениям Резерфорда,
подобен солнечной системе. Поэтому и
возникло название - планетарная
модель, рис.15. Т.к. атомы электрически
нейтральны то при заряде +Ze вокруг ядра
должны двигаться Z электронов. Для
электрона, движущегося по определенной
орбите, наблюдается действие на него
центростремительной силы, которой в
данном случае является сила кулоновского
притяжения:
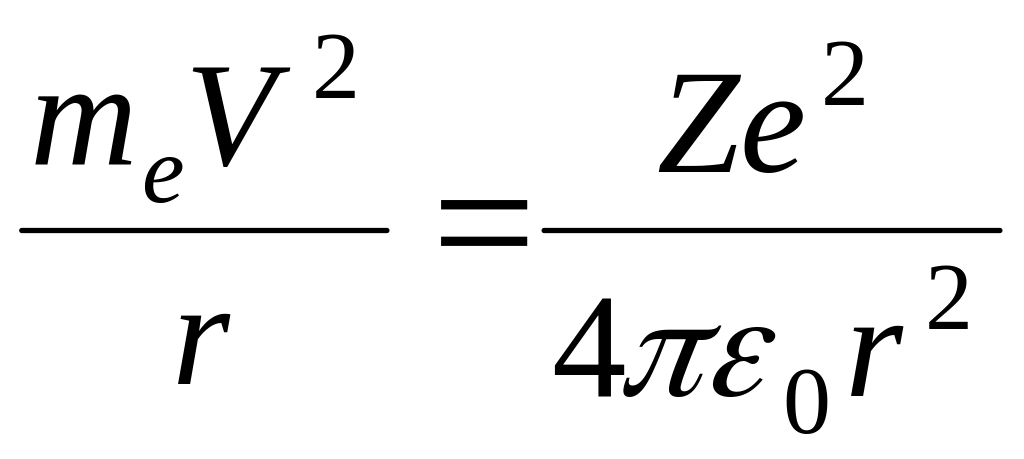 ,
,
![]() -
радиус орбиты,
-
радиус орбиты,
![]() -
скорость электрона на орбите,
-
скорость электрона на орбите,
![]() -
масса электрона. Однако эта модель имела
ряд существенных недостатков:
-
масса электрона. Однако эта модель имела
ряд существенных недостатков:
уравнение содержит два неизвестных и им отвечает бесконечное множество орбит на различных расстояниях от ядра. Любому значению
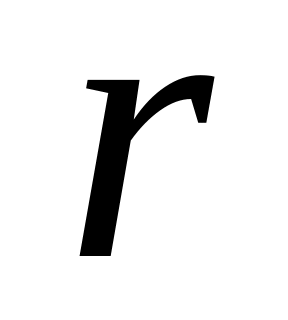 соответствует определенная скорость
соответствует определенная скорость
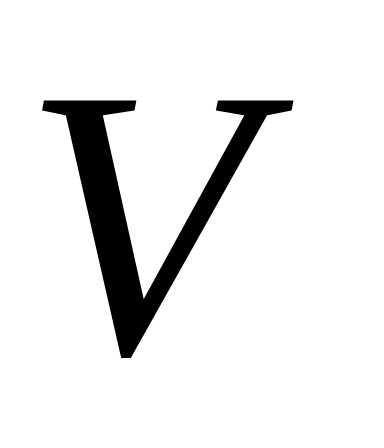 и энергия Е электрона на данной орбите.
Эти величины могут меняться непрерывно
и при переходе с одной орбиты на другую
может испускаться любая, а не вполне
определенная порция энергии. Согласно
этой модели спектр должен быть сплошным,
а не линейчатым.
и энергия Е электрона на данной орбите.
Эти величины могут меняться непрерывно
и при переходе с одной орбиты на другую
может испускаться любая, а не вполне
определенная порция энергии. Согласно
этой модели спектр должен быть сплошным,
а не линейчатым.согласно записанному выше равенству центростремительной и кулоновской силы модель механически устойчива. Однако она оказалась неустойчивой с точки зрения классической электродинамики. Электроны как частицы, несущие отрицательный заряд и движущиеся по круговым орбитам, обладают нормальным ускорением:
![]()
При
радиусе орбиты равной 10 -10
м можно оценить скорость и частота
обращения электрона равна:![]() .
При таких огромных ускорениях электроны
должны интенсивно излучать электромагнитные
волны. Их энергия будет быстро уменьшаться,
вследствие чего они должны непрерывно
приближаться к ядру и в конечном итоге
должны упасть на него. Следовательно,
данная модель непригодна для описания
водородоподобного атома. Задача создания
модели, описывающей закономерности
спектра водорода была решена Бором.
.
При таких огромных ускорениях электроны
должны интенсивно излучать электромагнитные
волны. Их энергия будет быстро уменьшаться,
вследствие чего они должны непрерывно
приближаться к ядру и в конечном итоге
должны упасть на него. Следовательно,
данная модель непригодна для описания
водородоподобного атома. Задача создания
модели, описывающей закономерности
спектра водорода была решена Бором.
