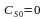Реакторы Периодического действия

Рисунок 177 - Реакторы периодического действия.
В реакторе периодического действия все отдельные стадии процесса протекают последовательно, в разное время.
В простейшем случае реактор периодического действия состоит из сосуда с мешалкой, которая обеспечивает такое интенсивное перемешивание среды, при котором концентрация во всем объеме в любой момент времени одинакова. Теплообмен осуществляется через рубашку или змеевик.
Состав реакционной массы меняется со временем, а поэтому скорость реакции изменяется в течение процесса.
Как
видно из рисунка 177 с течением времени
концентрация реагента А уменьшается
от начального значения
![]() до
значения
до
значения
![]() ,
соответствующего требуемой степени
превращения. Так как на единицу объема
реагирует
-
из
общего количества
молей,
то глубина превращения может быть
определена как
,
соответствующего требуемой степени
превращения. Так как на единицу объема
реагирует
-
из
общего количества
молей,
то глубина превращения может быть
определена как
 ,
(12.7)
,
(12.7)
Время
пребывания реагента в реакторе можно
найти следующим образом. Обозначим
через
![]() -
объем реакционной массы,
-
объем реакционной массы,
![]() -
число молей реагента А.
-
число молей реагента А.
Процесс протекает во времени. Тогда по материальному балансу для исходного компонента А найдем.
![]() ,
(12.8)
,
(12.8)
где r - скорость реакции, с-1.
Поскольку
![]() ,
(12.9)
,
(12.9)
То с учетом выражения (12.9) уравнение материального баланса (2.8) заменяется
![]() ,
(12.10)
,
(12.10)
или
 ,
(12.11)
,
(12.11)
В общем случае для реакции любого n-ого порядка скорость реакции r с учетом выражения (12.7) можно представить
![]() ,
(12.12)
,
(12.12)
И тогда уравнение (12.11) примет вид:
![]() ,
(12.13)
,
(12.13)
Выражая
![]() через
степень превращения
через
степень превращения
![]() получим
получим
![]() ,
(12.14)
,
(12.14)
Подставив
найденное значение
![]() из
(12.14) в (12.13) будем иметь
из
(12.14) в (12.13) будем иметь
 ,
(12.15)
,
(12.15)
Или после деления левой и правой части на С
![]() ,
(12.16)
,
(12.16)
После интегрирования выражения (12.16) время пребывания реагентов в реакторе равно
 ,
(12.17)
,
(12.17)
при
![]() получим
получим
 ,
(12.18)
,
(12.18)
при n=1
![]() ,
(12.19)
,
(12.19)
Примеры расчетов показателей процесса: степени превращения, конверсии и т.п.
Описание: Определить степень конверсии реагентов если уравнение процесса таково: 25СН2=СН216Н2О→С2Н5ОН24СН2=СН215Н2О Решение. Определить селективность процесса. Определить объем этиленовой фракции если объемная доля этилена в ней равна 90 необходимый для получения 810 кг этилхлорида. Определить вместимость реактора приняв для расчета константы скорости формулы: Решение.
Пример 1. Определить степень конверсии реагентов, если уравнение процесса таково:
25СН2=СН2+16Н2О→С2Н5ОН+24СН2=СН2+15Н2О
Решение. Количество превращенных реагентов
Этилен 25-24 = 1 моль
Вода 16-15 = 1 моль
Степень конверсии реагентов:
Этилен 1 : 25 = 0,04, или 4%
Вода 1 : 16 = 0,0625, или 6,25%
Пример 2. Пиролизу подвергли 1500 м3 метана. Степень конверсии метана равна 60%, масса ацетилена в продуктах пиролиза составляет 400 кг. Определить селективность процесса.
Решение. Уравнение реакции:
2СН4 → С2Н2 + 3Н2
2∙22,4 м3 26 кг. 3∙2 кг
Объем превращения метана:
1500 ∙ 0,6 = 900 м3
Теоретически возможную массу ацетилена (в расчете на превращенный метан) определяют, исходя из стехиометрических соотношений по пропорции:
2∙22,4 м3 С4 – 26 кг С2Н2
900 м3 СН4 – m кг С2Н2
Откуда
![]()
Селективность процесса:
400 : 522 = 0,766 или 76,6%
Пример 3. Выход этилхлорида, получаемого гидрохлорированием этилена, составляет 90% от теоретического. Определить объем этиленовой фракции, если объемная доля этилена в ней равна 90%, необходимый для получения 810 кг этилхлорида.
Решение. Уравнение реакции:
С2Н4 + НCL → С2Н2CL
22,4 м3 36,5 кг 64,5 кг
Максимально возможную (теоретическую) массу этилхлорида определяют с учетом выхода продукта:
810 : 0,9 = 900 кг С2H2Cl
Объем этилена исходя из стехиометрических соотношений:
22,4 ∙ 900 : 64,5 = 312 м3 С2Н4
Объем этиловой фракции:
312,6 : 0,9 = 347,3 м3
Элементы расчетов химических реакторов
Расчет реактора для провидения химического взаимодействия является основной частью технологического расчета производства. Этот расчет сводится к определению основных конструктивных размеров аппаратов и их числа. Размеры и число аппаратов как периодического, так и непрерывного действия определяются их производительностью.
Производительность реакционного аппарата или установки – количество целевого продукта (кг, т, м2), получаемого в единицу времени (с, ч, сутки, год). Зафиксированная производительность аппарата установки называется мощностью.
Объем рабочей части (реакционной зоны) аппаратов непрерывного действия определяют по уравнению:
![]()
где – Nc – секундная объемная производительность (м3/с). а τ – время, необходимое для проведения процесса, с.
Площадь поперечного сечения аппарата составляет (в м2):
![]()
где ω – скорость течения среды в аппарате, м/с.
Определив площадь сечения, легко найти диаметр аппарата (в м):

Высота (длина) реакционной зоны аппарата равна (в м):
![]()
Для аппаратов, заполненных катализатором, объем рабочей части равным объему катализатора Vк (м3), который определяют исходя из объемной скорости газа (жидкости) или производительности катализатора.
Объемная скорость – объем газовой смеси( жидкости), проходящей через единицу катализатора в единицу времени [м3/ (м3∙ч) или ч-1]:

Откуда

Производительность катализатора – масса (объема) целевого продукта снимаемого с единицы объема (массы) катализатора в единицу времени [кг/ (м3∙ч), м3/ (м3∙ч), кг/(кг∙ч), м3/ (кг∙ч)]:


Для периодических процессов общей реакционный объем аппаратов равен (в м3):

где Vсут – суточный объем перерабатываемых веществ,
τ – время технологического цикла (на проведение собственно процесса и вспомогательных операций), κзап – коэффициент заполнения аппарата (принимается от 0,4 до 0,9).
В специальной литературе описаны конструкции реакторов для многочисленных химических процессов, их собственности и методов расчета, поэтому ограничимся здесь некоторыми сведениями по элементам расчета реакторов, не имеющих прототипа.
Выбор конструкции промышленного реактора зависит прежде всего от следующих параметров: скорости протекания химических реакций (от времени пребывания в реакционной зоне), оптимальных условий тепло - и массобмена и оптимальных температуры и давления. Так как на практике сложно удовлетворить все требования, предъявляемые к промышленному реактору, то определяющими являются экономические показатели.
Для расчета химического реактора используют их идеализированные модели, среди которых выделяют:
а) периодический реактор полного смешения;
б) непрерывный реактор идеального вытеснения;
в) непрерывный реактор полного смешения.
Известно, что химические реакции могут протекать в диффузионной, кинетической или переходной области, но в общем случае скорость химико-технологического процесса можно выразить уравнением и=κ∆С, где и – скорость процесса, κ – константа скорости, а ∆С движущая сила процесса.
В технологии основного органического и нефтехимического синтеза многие процессы осуществляют непрерывно, следовательно, достижение максимального выхода продукта определяется временем пребывания реагирующих веществ в реакционной зоне. Отсюда следует, что необходимая вместимость реакционного аппарата, его производительность и интенсивность работы зависит от скорости провидения процесса.
Время пребывания реагирующих веществ реакционной зоне (τ) определяют из кинетических уравнений первого, второго и третьего порядков. В реакциях первого порядка стехиометрический коэффициент прямой реакции равен единицы, в реакции второго порядка – двум, третьего – трем. Так как стехиометрические коэффициенты химического уравнения не всегда определяют порядок реакции, то его устанавливают экспериментально. Для реакции первого порядка:
![]()
Для реакции второго порядка:

В случае равенства концентрации двух веществ кинетическое урвнение для второго порядка упрощается :
![]()
Для реакции третьего порядка имеем:
![]()
Где τ – время реакции, с; κ’, κ’’, κ’’’ - соответственно константы скорости реакции первого, второго и третьего порядка, с-1, л/ (моль∙с); a и b – начальные концентрации веществ, моль/л; x – количество вещества, вступившего в реакцию к моменту времени τ, моль/л.
Пример 4. Производительность реактора дегидрирования н-бутана до н-бутенов составляет 17400 кг целевого продукта в час. Процесс проводят при 6000С, и в этих условиях степень конверсии н-бутана равна 30%, а селективность по н-бутенам составляет 75%. Определить вместимость реактора, приняв для расчета константы скорости формулы:
![]()
Решение. Уравнение реакции:
СН3 – СН2 – СН2 – СН3 ↔ СН2 = СН – СН2 – СН3 + Н2
58 кг (22,4 м3) 56 кг 2 кг
Расход н-бутана для проведения процесса:
![]()
![]()
или 30933 : 3600 = 8,6 м3/с
Константа скорости:
![]()
Вместимость реактора:
Vp = 8,6 ∙ 2,2 = 19 м3
Пример 5. Акрилонитрил получают окислительным аммонолизом пропилена в псевдоожиженном слое катализатора. В реактор, производительность которого по целевому продукту равна 5600 кг/ч, поступает газовая смесь, объемная доля пропилена в которой 8%. При 4500С степень конверсии пропилена равна 60%, а селективность по акрилонитрилу составляет 75%. Определить объем катализатора в реакторе, приняв для расчета константы скорости такую формулу:
k = 2,8 ∙ 105 e-80000/RT
Решение. Уравнение реакции:
СН2 = СН – СН3 + NH3 + 1,5O2 → CH2 = CHCN + 3H2O
42 кг (22,4 м3) 17 кг 15∙32 кг 53 кг 3∙18 кг
Расход пропилена на проведение процесса:
![]()
![]()
Объемный расход газовой смеси на входе в реактор:
![]()
Определение константы скорости:
k = 2,8 ∙105 ∙ 2,72-80000/8,314(450+273) = 2,8 ∙ 105 ∙ 2,72-13,3 = 2,8 ∙ 105 ∙ 0,2 ∙ 10-5 = 0,56 с-1
где R=8,314 кДж/(моль∙К), а e=2,72.
При соотношении исходных веществ С3Н6 : NH3 : O2 : H2OЮ равном 1: 0,7 : 1,7 : 3, реакция окислительного аммонолиза имеет первый порядок по пропилену, а по кислороду и аммиаку – нулевой.
Формула для расчета времени пребывания веществ в реакционной зоне :
![]()
Объем катализатора в реакторе:
18,3 ∙ 1,65 = 30 м3
Пример 6. Время пребывания углеводородов при получении ацетилена электрокрекингом равно 0,001 с, объемный расход газов пиролиза равен 25500 м3/ч, скорость газов в реакционной камере составляет 900 м/с. определить площадь сечения, высоты и объем реакционной камеры электродугового реактора.
Решение. Секундная объемная производительность реактора (по газам электрокрекинга) :
25500 : 3600 = 7,08 м3/с
Объем реакционной камеры:
7,08 ∙ 0,001 = 0,0071 м3
Площадь сечения реакционной камеры:
7,08 : 900 = 0,0079 м2
Высота реакционной камеры:
0,0071 : 0,0079 = 0,9 м или 900 ∙ 0,001 = 0,9 м
Пример 7. Объемная скорость подачи этилена в реактор прямой гидратации равна 1900 ч-1, а объемный расход этилена составляет 22000 м3/ч. Определить объем катализатора, необходимый для проведения процесса.
Решение. Объем катализатора:
22000 : 1900 = 11,6 м3
Пример 8. Производительность реактора окисления метанола составляет 3500 кг формалина в час; массовая доля формальдегида в нем равна 37%. Диаметр сечения аппарата 1,4 м, высота слоя контактной массы 75 мм. Определить производительность 1 кг и 1л контактной массы. Насыпная плотность катализатора равна 600 кг/м3.
Решение. Производительность реактора по целевому продукту – формальдегиду:
3500 ∙ 0,37 = 1295 кг/ч
Объем катализатора в реакторе (V=πD2H/4 = 0,785 D2 H) :
0,785 (1,4)2 ∙ 0,075 = 115 м3 или 115 л
Производительность 1 л катализатора:
1295 : 115 = 11,3 кг/(л∙ч)
Масса катализатора в реакторе:
0,115 ∙ 600 = 69 кг
Производительность 1 кг катализатора:
1295 : 69 = 18,8/(кг∙ч)
Реактор идеального смешения непрерывного действия
Схема потоков в реакторе полного смешения представлена на рис. 1. В реакторе такого типа концентрация любого компонента равномерна по всему реакционному объему, и поэтому уравнение материального баланса можно записать для всего объема реактора. Для установившегося режима:
Gпр= Gух+ Gхр (1),
где Gпр – масса вещества, поступающего в элементарный объем в единицу времени; Gух - масса вещества, выходящего из элементарного объема в единицу времени; Gхр – скорость расходования исходного вещества в результате химической реакции, протекающей в элементарном объеме:
Так как степень превращения равна:
|
Рис.1. Схема реактора идеального смешения. |
где,
 -
начальная концентрация исходного
вещества,
-
начальная концентрация исходного
вещества,
 -
конечная концентрация исходного
вещества,
-
конечная концентрация исходного
вещества,
 -
объемный расход реакционной смеси,
-
объемный расход реакционной смеси,
 -
скорость химической реакции,
-
скорость химической реакции,
 -
время химической реакции,
-
время химической реакции,
 -степень
превращения, V-
объем реакционной смеси.
-степень
превращения, V-
объем реакционной смеси.
Уравнение (5, 6) представляют собой проектные уравнения реактора идеального смешения и позволяют определить неизвестную величину по заданным. В любом случае для реактора идеального смешения его размер, расход реагентов, начальные и конечные концентрации могут быть определены только при условии, если известна кинетика процесса.
В таблице 1 приведены расчетные уравнения для реактора идеального смешения непрерывного действия при проведении в нем простых обратимых и необратимых, а также сложных химических реакций.
Таблица 1. Расчетные уравнения для РИС-Н
Схема реакции |
Кинетическая модель |
Расчетные уравнения |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Рассмотрим некоторые примеры расчета такого типа реакторов.
Пример 9.
Определить объем реактора идеального смешения для реакции протекающего без изменения объема реакционной массы.
Дано:
реакция А → 2S;
порядок реакции n=1;
объемный расход исходного вещества GV = 0,25 л/мин;
начальная концентрация исходного вещества СА0= 0,5 моль/л;
константа скорости реакции k= 0.15 мин -1;
степень превращения xA = 0,52.
Решение.
Так как реакция первого порядка, скорость реакции определяем по уравнению:
 .
.
В РИС-Н приравниваем объем реакционной массы к объему реактора, тогда по уравнению:


Пример 10.
Определить объем реактора идеального смешения для обратимой реакции протекающего без изменения объема реакционной массы.
Дано:
реакция 2А ↔R+S;
порядок реакции n=2;
объемный расход исходного вещества GV = 4,8 м3/ч;
начальная концентрация исходного вещества СА,0= 1,5 кмоль/м3;
константа скорости прямой реакции k1 = 2*10-3 м3/(кмоль∙с);
константа равновесия Кр = 9;
требуемая степень превращения xA = 0,8 от равновесной.
Решение.
Объем реактора, в котором проводится данная реакция, определяем из базового уравнения для РИС-Н:
;
 .
.
Так как реакция обратимая, составляем кинетическую модель для данной реакции:
 т.к.
т.к.
 и
и
 .
.
С учетом вышеизложенного выражаем время реакции:
 ,
,
где
 -
фактическая степень превращения;
-
фактическая степень превращения;
 -
константа скорости обратной реакции.
-
константа скорости обратной реакции.
В этом уравнении неизвестными величинами являются фактическая степень превращения и константа скорости обратной реакции. Константу скорости обратимой реакции определяем из уравнения:
 .
.
Для определения равновесной степени превращения используем константу равновесия, выраженную через концентрации веществ:
 ,
,
где
 -равновесная степень превращения.
-равновесная степень превращения.
Подставляя
в данное выражение значения константы
равновесия, получаем
 .
Так как требуемая степень превращения
равна 0,8, то фактическая степень
превращения будет равна:
.
Так как требуемая степень превращения
равна 0,8, то фактическая степень
превращения будет равна:
 .
.
Тогда время реакции будет равно:
 .
.
С учетом полученного времени реакции объем реактора составит:


 (2);
(2); (3).
(3). (4);
(4); (5); то
(5); то
 (6),
(6),





 при
при