
- •1)Қатты дене деген не? Оны түсіндіріңіздер
- •3)Құрылымына байланысты қатты денелерінің топтастыру
- •4)Ленард-Джонс потенциалы және оның шығарылуы
- •5.Дисперсия заңы. Оны түсіндіріңіздер.
- •6 Кристалдық зат және оның кенестік торы
- •7 Иондық байланысы және оның энергиясы
- •8Кристалдың түйіндері, бағыттары, жазықтықтары және олардың белгіленуі.
- •9Аккустикалық пен оптикалық толқындары
- •10Маделунг тұрақтысы және оның шығару
- •21.Кубқатән симметрия элементтерініңжиынтығы.
- •22.Электрондық газдыңжылусыйымдылығы мен байланыс энергиясынесептеу.
- •23.Сингониябойы 14 түрліБравэрешеткаларыныңүлестірілуі.
- •24.Дебайжылусиымдылығыжәне оның шығарылуы
- •25.Кері тордың векторы және оның қасиеттері
- •26.Ферми энергиясы және оның толқын векторына тәуелділігі
- •27.Вульф-Брегг тендеуі, оны дәлелдеу
- •28.Ферми бос электрондық газдың байланыс энергиясы
- •29. Шектік симметрия топтары. Оны қалай түсінесіз
- •30.Блох теоремасыжәне оның шығарылуы
1 |
Қатты дене деген не? Оны түсіндіріңіздер. |
2 |
Вандер-Ваальс байланысы және оның шығарылуы |
3 |
Құрылымына байланысты қатты денелерінің топтастыру. |
4 |
Ленард-Джонс потенциалы және оның шығарылуы |
5 |
Дисперсия заңы. Оны түсіндіріңіздер. |
6 |
Кристалдық зат және оның кенестік торы. |
7 |
Иондық байланысы және оның энергиясы. |
8 |
Кристалдың түйіндері, бағыттары, жазықтықтары және олардың белгіленуі. |
9 |
Аккустикалық пен оптикалық толқындары. |
10 |
Маделунг тұрақтысы және оның шығару |
11 |
Қатты дененің электрөткізгіштігі және оның шығарылуы |
12 |
Кристалл симметриясының нүктелік топтары. |
13 |
Толқындар мен кристалдық тордың арасындағы әрекеттесу. |
14 |
Металдардың электрөткізгіштігі, оның Кf байланысы |
15 |
Симметрия топтарының комбинациясы.Симметрияның 32 нүктелік топтары. |
16 |
Кристалдардың квадраттық тендеулері. |
17 |
Бірөлшемді (одномерный) моноатомдық тізбегіндегі атомдардың тербелістері. |
18 |
Тура және кері торлардың параметрлерінің өзара байланысы. |
19 |
Екі атом тізбегіндегі атомдардың тербелістері. |
20 |
Симметрияның кеністіктік топтары. |
21 |
Кубқа тән симметрия элементтерінің жиынтығы. |
22 |
Электрондық газдың жылусыйымдылығы мен байланыс энергиясын есептеу. |
23 |
Сингония бойы 14 түрлі Бравэ решеткаларының үлестірілуі. |
24 |
Дебай жылусиымдылығы және оның шығарылуы |
25 |
Кері тордың векторы және оның қасиеттері. |
26 |
Ферми энергиясы және оның толқын векторына тәуелділігі. |
27 |
Вульф-Брегг тендеуі, оны дәлелдеу. |
28 |
Ферми бос электрондық газдың байланыс энергиясы. |
29 |
Шектік симметрия топтары. Оны қалай түсінесіз |
30 |
Блох теоремасы және оның шығарылуы |
31 |
Аккустикалық толқындарының табиғаты |
32 |
Кеністіктік симметрия топтары. |
33 |
Бриллюэн аумақтары, олардың құрылуы. Келтірілген Бриллюэн аумақтары. |
34 |
Оптикалық толқынының шығуы. |
35 |
Кеністіктік тор және кері тор. Олардың өзара байланысын түсіндіріңіздер |
36 |
Псевдопотенциал және дисперсия заңдары. |
37 |
Қатты денелерінің құрылымына байланысты топтастырылуы. |
38 |
Вигнер-Зейц ұяшығы мен Бриллюэн аумағы. |
39 |
Эффективтік масса және оның шығарылуы |
40 |
Эйнштейн бойынша қатты дененің жылусиымдылығы. |
Атомдары немесе молекулалары реттелiп орналасқан және периодты түрде қайталанып тұратын iшкi структурасын түзетiн қатты денелер кристаллдар деп аталады. Кристалдардың қырлары әрқашан жазық және дұрыс геометриялық пiшiндi болып келедi . Бөлшектердiң орналасуының салыстырмалы түрде орныққан скелетi кристалдық торлар деп аталады, ал сол торлардың орналасқан орындары түйiндер деп аталады
|
|
Кристалдардың сыртқы пiшiнiнiң дұрыстығы - олардың реттелген құрылысының бiр ғана салдары емес. Олардың ең басты ерекшелiгi кристалдың физикалық қасиеттерiнiң ондағы таңдалған бағытына байланыстылығында. Кристалдардың бұл қасиетi анизотропия деп аталады.
Барлық кристалды денелер анизотропты болып келедi. Анизотропияның бiр себебi - кристалдық тор түйiндерiнiң тығыздығы әр түрлi бағытта әр түрлi болған жағдайдағы, бөлшектердiң дұрыс ретпен орналасуы. Осы бағыттардағы бөлшектердiң өзара әсерi де бiрдей болмайды. Бұдан, әр түрлi бағыттардағы кисталдардың механикалық берiктiгi әр түрлi екендiгi шығады.
Көптеген кристалдар жылу мен электр тогын әр бағытта әр-түрлi өткiзедi. Кристаллдың оптикалық қасиеттерi де оның бағытына байланысты болуы мүмкiн
1)Қатты дене деген не? Оны түсіндіріңіздер
ҚАТТЫ ДЕНЕ – заттың агрегаттық күйі; Қатты денелер сұиықтар сияқты өзінің көлемін ғана сақтап қоймады, сонымен бірге пішінін де сақтай алады. пішінінің орнықтылығымен және атомдарының жылулық қозғалыс әсерінен тепе-теңдік қалпының маңында мардымсыз аз тербелістер жасайтындығымен сипатталады. Атомдарының орналасу сипатына қарай Қ. д-лер кристалдар және аморф денелерге бөлінеді.
Кристалдар атомдары кеңістікте белгілі бір тәртіппен орналасады. Кристалдың сыртқы пішіні дүрыс яғни бірқаліпті болуында осған байланысты. Сондықтан оның қасиеттерінде кеңістіктік периодтылық байқалады. Кристалдар – анизотропты. Кеңістіктік тор. Криталдағы бөлшектердің дұрыс орналасуын кристалдардың кейбір қасиеттерінің бағытқа тәуелділігі, яғни анизотропиясы шығады. Анизотропия қасиетінің тек монокристалдарға ғана тән болатындығын да айта кетейік. Қатты денелердің көпшілігінің құрылымы поликристалды (грек. поли - көп), яғни микроскоппен ғана көруге болатын өте ұсақ кристалдардың жиынтығынан тұрады. Поликристалды денелер мен аморфты денелердің айырмашылығы мынада: поликристалдық денелердің анизотропия байқалатын өте кішкентай бөлігін бөліп алуға болады, ал аморфты денелердің кез-келген бөлігін қарастырсақ та, ол әрқашан изотропты
Аморфты денелердің сырт қарағанда көлемін және пішінін сақтауы оларды қатты дене етіп көрсеткенімен, бұл денелер өте тұтқыр сұйық деп қарастырылады. Температура жоғарылаған сайын олардың сұйыққа тән қасиеттері бірден көріне бастайды, бірте-бірте еріп, сүйықтың барлық қасиеттеріне ие болады. Аморфты денелер – изотропты. Кристалдың қасиеттері әр түрлі бағыттарда түрліше болады. Аморфтық денелерде атомдар бей-берекет орналасқан нүктелердің төңірегінде тербеліп тұрадыАморфты денелер. Атомдарының ретті орналасуы алыс қашықтықтарда да қайталанып отыруымен сипатталатын кристалдық денелерден аморфты денелердің айырмашылығы, мұнда тек жуық тәртіп қана орын алады. Кейбір заттар кристалл және аморфтық түрде де бола алады. Қатты денедегі атомдар. Атом аралық байланыстар. Сонымен қатар Қ. д-нің құрылымы мен қасиеттері темп-раның өзгерісіне, магнит өрісінің әсеріне, басқа да сыртқы әсерлерге байланысты өзгереді. Байланыстарының түрі бойынша Қ. д. 5 класқа бөлінеді (иондық, атомдық, металдық, молекулалық, сутектік). Иондық кристалдарда (NaCl, KСl, т.б.) Қ. д-нің механикалық қасиеттері. Қ. д. мех. қасиеттері оның сыртқы мех. әсерлерге реакциясын сипаттайды: сығу, созу, бұрау, соққы, т.б. Қ. д. мех. қасиеттері оның құрылымдық бөлшектердің арасында әсер ететін байланыс күштерімен анықталады. Бұл күштердің әр түрлі болуы мех. қасиеттердің де әр түрлі болуына әкеледі: Қ. д-лердің бірі майысқыш болса, басқалары – морт келеді. Әдетте, металдар диэлектриктерге қарағанда майысуға икемді. Түсірілген күш шамасы азырақ болатын кездерде барлық денелерде кернеу мен деформация арасында сызықтық байланыс орнайды (Гук заңы). Кристалдардың беріктігі атомдар арасындағы байланыс күштеріне тәуелді болмайды.
2)Вандер-Ваальс байланысы және оның шығарылуы
Ван-дер-Ваальс күштери. Салыстырмалы үлкен қашықтықтарда молекулалар арасында Ван-дер-Ваальс күштери деп аталатын тартылыс күштері әсер етеді.
Қ ұрамындағы
теріс және оң зарядлары бир бирине
салыстырғанда ауысқанда нейтрал молекула
электрлік жақтан диполге айналады.
ұрамындағы
теріс және оң зарядлары бир бирине
салыстырғанда ауысқанда нейтрал молекула
электрлік жақтан диполге айналады.
Дипол электр моментімен әсерлеседі. Дипол моменті заряд мәні мен осы заряд арасындағы қашықтықтың көбейтіндісіне тең (р = е*d). Дипол өзінің төңірегінде электр өрісін туғызады. Және сол өріс арқалы басқа дипольдармен әсерлеседі.
Тұрақты диполь моментіне ие молекулалар болады. Мұндай молекулаларды поляр молекулалар деп атаймыз. Әдетте поляр молекулалар өзара тартысады. Мұндай күштерді дипольдық-ориентациялық деп атаймыз.
Ван-дер-Ваальс күштерінің пайда болуы
Жалпы жағдайда, Ван-дер-Ваальс байланысы дисперсиялық, бағдарлаушы және индукциялық өзара әсерлесулерді біріктіреді. Осылардың әрбіреуіне қысқаша тоқталайық.
Дисперсиялық өзара әсерлесу.
Қарапайым мысал ретінде 1.1-суретте көрсетілген екі гелий атомының өзара әсерлесуін аламыз. Гелий атомының электрондық тығыздығы сфералық симметриялы, соның нәтижесінде оның электрлік моменті нөлге тең. Бірақ, бұл тек қана атомның орташа электрлік моменті нөлге тең дегенді білдіреді. Уақыттың әрбір мезетінде электрондар кеңістіктің қандай да бір белгілі нүктелерінде өте тез өзгеріп отыратын лездік электрлік дипольдерді тудырады. Екі гелий атомы жақындасқанда электрондар қозғалысында корреляция (келісушілік) орнайды, ол өзара әсерлесуші күштердің пайда болуына алып келеді. Бұл күштер екі жақтылық сипатта болады. Егер электрондар қозғалысы 1.1 а –суретте көрсетілгендей болса, онда лездік дипольдар арасында тартылыс, ал 1.1 б - суреттегідей болса, онда атомдар арасында тебіліс пайда болады. 1.1 а-суреттегідей конфигурация іске асқанда жүйе энергиясы кемиді, оның ықтималдылығы жоғары және жиі кездеседі. Бұл гелий атомдарын байланыстыратын тұрақты тартылыс күштерінің болатынын көрсетеді. Электрондардың осындай келісілген қозғалысы нәтижесінде пайда болатын байланыс күштері дисперсиялық күштер деп аталады. Оларды ең алғаш рет 1930 жылы Лондон есептеді.

а) б)
1.1 - сурет
Есептеулер кезінде келесі модель негіз ретінде алынды: бір атомның лездік моментінің әсерінен екінші атом поляризацияланады және онда тартылыс болатындай дипольдардың орналасуы пайда болады (1.1 а-сурет). Есептеулер бөлшектердің дисперсиялық өзара әсерлесу энергиясын анықтайтын теңдеуді алуға мүмкіндік берді:
 (1.2)
(1.2)
мұндағы
 — бөлшектердің поляризациялануы;
— бөлшектердің поляризациялануы;
 -
олардың қозу энергиясы;
-
олардың қозу энергиясы;
 — ара қашықтықтары.
— ара қашықтықтары.
Бағдарлаушы өзара әсерлесу.
Егер
молекулалардың тұрақты дипольдік
моменті
 ,
яғни полярлы болса, онда олардың арасында
молекулаларды қатаң тәртіппен
орналастыруға тырысатын электростатикалық
өзара әсерлесулер (1.2 –сурет) пайда
болады. Бұл кезде жүйе энергиясы кемиді.
Молекулалардың дұрыс орналасуын жылулық
қозғалыс бұзады. Сондықтан, молекулалардың
бағытталып орналасуын анықтайтын жүйе
энергиясы температураға күшті тәуелді
болады. Молекулалардың толығымен
бағытталып орналасуы болатын төмен
температураларда өзара әсерлесу
энергиясы мына қатынаспен анықталады:
,
яғни полярлы болса, онда олардың арасында
молекулаларды қатаң тәртіппен
орналастыруға тырысатын электростатикалық
өзара әсерлесулер (1.2 –сурет) пайда
болады. Бұл кезде жүйе энергиясы кемиді.
Молекулалардың дұрыс орналасуын жылулық
қозғалыс бұзады. Сондықтан, молекулалардың
бағытталып орналасуын анықтайтын жүйе
энергиясы температураға күшті тәуелді
болады. Молекулалардың толығымен
бағытталып орналасуы болатын төмен
температураларда өзара әсерлесу
энергиясы мына қатынаспен анықталады:
 (1.3)
(1.3)
мұндағы
-
молекулалардың ара қашықтықтары,
 — диэлектрлік тұрақты.
— диэлектрлік тұрақты.
Жоғары температуралардағы дипольдік молекулалардың өзара әсерлесулері Кеезом көрсеткендей мына теңдеумен анықталады:
 (1.4)
(1.4)

1.2 – сурет 1.3 – сурет
Қарастырған өзара әсерлесу бағытталушы (ориентациялық) деп аталады.
Индукциялық өзара әсерлесу.
Поляризациялануы жоғары болатын полярлы молекулаларда көршілес молекулалардың тұрақты өрістерінің әсерінен индукциялық моменттер пайда болуы мүмкін (1.3-суретте үзік сызықтармен индукцияланған диполдар көрсетілген). Бірінші және екінші молекулалардың дипольдері арасында пайда болған өзара тартылыс энергиясы Дебай көрсеткендей температураға байланысты болмайды және мына қатынаспен анықталады:
 (1.5)
(1.5)
мұндағы М — молекулалардың тұрақты дипольдік моменті, α — олардың поляризациялануы.
Осындай өзара әсерлесу индукциялық немесе деформациялық деп аталады.
Жалпы
алғанда, екі молекула бір-біріне
жақындағанда барлық үш түрлі байланыстың
пайда болуы мүмкін, және өзара әсерлесу
энергиясы
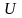 дисперсиялық
дисперсиялық
 ,
бағдарлаушы
,
бағдарлаушы
 және индукциялық
және индукциялық
 өзара әсерлесулер энергияларының
қосындысына тең болады:
өзара әсерлесулер энергияларының
қосындысына тең болады:

1.1 - кесте
Заттар |
Өзара әсерлесулер түрлері |
||
дисперсиялық |
индукциялық |
Бағдарлаушы |
|
Су |
19 |
4 |
77 |
Аммиак |
50 |
5 |
45 |
Хлорлы сутек |
81 |
4 |
15 |
Көміртек окисі |
100 |
|
|
1.1- кестеде cу, аммиак, хлорлы сутек, көміртек окисі үшін осы байланыс энергияларының әрбіреуінің салыстырмалы пайыздық мөлшері берілген.
1.1- кестеден барлық заттардың байланыс энергияларының ішінде индукциялық өзара әсерлесу энергиясының аз екендігі көрініп тұр. Полярлы молекулалалы заттардың бай ланыс энергияларының 3/4 немесе 1/2 бөлігі қатаң (жесткии) дипольдердің бағытталып өзара әсерлесу энергиясынан тұрады. Ал полярлы емес молекулалы заттардың байланыс энергиялары толығымен дисперсиялық өзара әсерлесу энергиясы болып табылады деп айтуға болады.
1.2 – кесте

Неон
|
........................1,9 |
Оттегі
|
............................8,2 |
Аргон
|
........................8,4 |
Көміртек
окисі
|
............................8,4 |
Азот
|
........................6,6 |
Метан
|
............................10,8 |
1.2 - кестеде кейбір молекулалық кристалдардың Ван-дер-Ваальс күштері әсерінен пайда болған байланыс энергияларының мәндері келтірілген.






