
- •Установки изомеризации фракции н.К.-62 °с
- •Краткие сведения об истории развития гидрогенизационных процессов
- •8.4.2. Химизм, термодинамика и кинетика
- •Катализаторы гидрогенизационных процессов
- •Процессы гидрооблагораживания нефтяных остатков
- •I Менее 5 Менее 10
- •V Более 20 Более 150
- •8.5. Каталитические процессы гидрокрекинга нефтяного сырья
и
значительно сокращается загрязнение
атмосферы окислами серы.
Нефтяные
масла подвергают неглубокому
гидрообессериванию
с целью осветления
и снижения их коксуемости, кислотности
и эмуль-
гируемое™. С заменой
сольвентной очистки высоковязкого
масляного
сырья, например деасфальтизата,
на гидрокрекинг появилась возмож-
ность
производить масла с высоким индексом
вязкости (более 105).
Гидроочищенные
масляные продукты удовлетворяют
требованиям
стандартов по цвету,
стабильности, запаху, допустимому
содержанию
примесей и другим
экологическим и эксплуатационным
показателям.
РЕАКЦИЙ
ГИДРОГЕНОЛИЗА
ГЕТЕРООРГАНИЧЕСКИХ
СОЕДИНЕНИЙ СЫРЬЯ
Гидрогенолиз
гетероорганических соединений в
процессах гидро-
облагораживания
происходит в результате разрыва связей
C-S,
C-N,
С-0
и насыщения водородом образующихся
гетероатомов и двойной связи
у
углеводородной части молекул нефтяного
сырья. При этом сера, азот
и кислород
выделяются в виде соответственно H2S,
NH3
и Н20.
Содер-
жащиеся в сырье непредельные
гидрируются до предельных парафино-
вых
углеводородов. В зависимости от условий
процессов возможны
частичное
гидрирование и гидрокрекинг полициклических
ароматиче-
ских и смолисто-асфальтеновых
углеводородов. Металлоорганические
соединения
сырья разрушаются, и выделяющиеся
металлы отлагаются
на катализаторе.
Гидрогенолиз
сероорганических соединений. Меркаптаны
гидриру-
ются до сероводорода и
соответствующего углеводорода:
Сульфиды
гидрируются через образование
меркаптанов:
Дисульфиды
гидрируются аналогично:
Циклические
сульфиды, например тиофан и тиофен,
гидрируются с образованием соответствующих
алифатических углеводородов:
304
Бенз-
и либензтиофены гидрируются по схеме:
Гидрогенолиз
азоторганических соединений. Азот
в нецн иним сырье
находится
преимущественно в гетероциклах в виде
производных пирро-
ла и пиридина.
Гидрирование их протекает в общем
аналогично гидри-
рованию сульфидов:
I—i+Нт
■—. +н2 +н2
Г\
-*~ГЛ
-»
c4H9NH2
-Vc4h10
+ nh3
mi
nh
Пиррол
CQ+”4
CQ"2
0"C5H‘NH2
+S2Q'C3H7+nh3
Хинолин
Гидрогенолиз
кислородсодержащих соединений. Кислород
в топ-
ливных
фракциях может быть представлен
соединениями типа спиртов,
эфиров,
фенолов и нафтеновых кислот. В газойлевых
фракциях и нефтя-
ных остатках
кислород находится в основном в
мостиковых связях
и в циклах
полициклических ароматических и
смолисто-асфальтеновых
соединений
нефти.
При
гидрировании кислородных соединений
образуются соответ-
ствующие
углеводороды и вода:
R-^^-COOH
—У R^^-СНз
+ Н20
В
табл. 8.12 приведены термодинамические
данные для реакций
гидрогенолиза
некоторых серо- и кислородсодержащих
органических
углеводородов.
Как
видно из этих данных, реакции гидрогенолиза
гетероатомных
углеводородов
экзотермичны и протекают либо без
изменения объема
или в случае
гидрогенолиза непредельных
гетероорганических соедине-
ний
(как, например, производных тиофена) —
с уменьшением объема
и более высоким
экзотермическим эффектом. Следовательно,
реакции
гидрогенолиза всех без
исключения гетероорганических
соединений
являются термодинамически
низкотемпературными. Давление либо
не
оказывает влияния на равновесие
газофазных реакций, либо благопри-
ятствует
образованию продуктов гидрогенолиза.
Из
табл. 8.12 следует, что с повышением
температуры константы
равновесия
реакций гидрогенолиза уменьшаются,
особенно сильно для
305
8.4.2. Химизм, термодинамика и кинетика
![]()

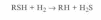

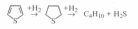

Таблица
8.12
Тепловой
эффект и константы равновесия (A"p)
реакций
гидрогенолиза |
Тепловой эффект, кДж/моль |
ЛР |
|||||
|
при |
при |
при |
при |
|||
|
300 К |
800 К |
300 К |
800 К |
|||
C3H7SH+H2^C3H8+H2S |
+47,9 |
+55,9 |
2,6 |
• Ю9 |
77 |
103 |
|
С5Н1 |SH+H2^C5H12+H,S |
+58,2 |
+66,6 |
3.9 |
10ю |
90- |
Ю3 |
|
CH3SC3H7+2H2<±CH4+C3H8+H2S |
+120,2 |
+ 135,3 |
2,1 |
1(Я2 |
47- |
108 |
|
CH3SC4H9+2H2^ CH4+C4H10+H2S |
+108,6 |
+124,0 |
1,1 |
1021 |
4 5 • |
108 |
|
C4H4S+4I [2 ^C4H10+H2s |
+262,4 |
+283,6 |
5,3 |
юзо |
18 |
5 |
|
C4H5S+2H9 <^C4H10+H7S |
+112,6 |
+121,8 |
5,4- |
ю16 |
14- |
104 |
|
C5H10S+2H2^C5H12+H2S |
+103,4 |
+117,0 |
2,8 • |
ю16 |
63- |
Ю4 |
|
CioH2]OH+H2^Ci0H22+H20 |
+88,3 |
+92,4 |
4,5- |
ю15 |
7,8- |
ю5 |
|
