
- •Понятия о диаграммах фазового равновесия систем. Применение.
- •Основные виды диаграмм (5 видов).
- •Виды взаимодействия элементов в твердом состоянии (3 основных вида).
- •Диаграмма Fe-c.
- •Диаграммы Al-Cu.
- •Диаграммы Cu-Zn.
- •Общая классификация металлических материалов.
- •Виды сталей и чугунов. Диаграмма Fe- Fe3c с классификацией Fe-c сплавов.
- •Три основных вида термической обработки: отжиг, закалка, отпуск (старение). Их назначение.
- •Общие понятия об отжиге: разновидности, назначение.
- •Закалка с полиморфным и без полиморфного превращения.
- •Этапы распада пересыщенного твердого раствора при отпуске.
- •Зависимость механических свойств от степени распада твердого раствора. Влияние отпуска на механические свойства.
- •Основные механические свойства и методы испытаний.
- •Холодная и горячая пластическая деформации.
2.2.1 Металл
Основные виды кристаллических решеток металлов.
1.Кубическая объемно-центрированная или сокращенно ОЦК (свинец, вольфрам) 9 атомов;
2.Кубическая гранецентрированная (ГЦК) (серебро, золото) 14 атомов;
3.Гексагональная плотно-упакованная (ГПУ) (магний, цинк).
Решетки ГЦК и ГПУ более компактны, чем ОЦК.
Все металлы являются кристаллическими телами, имеющими определенный тип кристаллической решетки, состоящей из малоподвижных положительно заряженных ионов, между которыми движутся свободные электроны.
Такой тип структуры называется металлической связью.
Тип решетки определяется формой элементарного геометрического тела, многократное повторение которого по трем пространственным осям образует решетку данного кристаллического тела.
1 .
ОЦК-решетки составляет элементарная
кубическая ячейка, в которой
положительно заряженные ионы металла
находятся в вершинах куба, и один атом
в центре его объема, т. е. на пересечении
его диагоналей. Такой тип решетки в
определенных диапазонах температур
имеют железо, хром, ванадий, вольфрам,
молибден и др. металлы.
.
ОЦК-решетки составляет элементарная
кубическая ячейка, в которой
положительно заряженные ионы металла
находятся в вершинах куба, и один атом
в центре его объема, т. е. на пересечении
его диагоналей. Такой тип решетки в
определенных диапазонах температур
имеют железо, хром, ванадий, вольфрам,
молибден и др. металлы.
2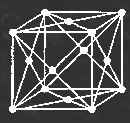 .
ГЦК-решетки элементарной ячейкой служит
куб с центрированными гранями. Подобную
решетку имеют железо, алюминий, медь,
никель, свинец и др. металлы.
.
ГЦК-решетки элементарной ячейкой служит
куб с центрированными гранями. Подобную
решетку имеют железо, алюминий, медь,
никель, свинец и др. металлы.
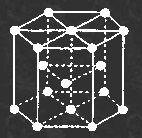 3.
ГПУ. Это плотноупакованных решеток
является гексагональная плотноупакованная
гпу. ГПУ-ячейка состоит из отстоящих
друг от друга на параметр с параллельных
центрированных гексагональных
оснований. Три иона (атома) находятся
на средней плоскости между основаниями.Такую
решетку имеют магний, цинк, кадмий,
берилий, титан и др.
3.
ГПУ. Это плотноупакованных решеток
является гексагональная плотноупакованная
гпу. ГПУ-ячейка состоит из отстоящих
друг от друга на параметр с параллельных
центрированных гексагональных
оснований. Три иона (атома) находятся
на средней плоскости между основаниями.Такую
решетку имеют магний, цинк, кадмий,
берилий, титан и др.
Дефекты кристаллического строения. В решетке реального металла могут находиться различные дефекты. Все дефекты кристаллической решетки делят: на точечные, линейные, простейшие-краевые и винтовые.
1.Точечные дефекты, характеризуются малыми размерами во всех трех измерениях. Величина их не превышает нескольких атомных диаметров. Это: а) свободные места в узлах кристаллической решетки — вакансии (дефекты Шоттки); б) атомы, сместившиеся из узлов кристаллической решетки в межузельные промежутки — дислоцированные атомы (дефекты Френкеля); в) атомы других элементов, находящиеся как в узлах, так и в междоузлиях кристаллической решетки — примесные атомы. Точечные дефекты образуются в процессе кристаллизации под воздействием тепловых, механических, электрических воздействий, при облучении нейтронами, электронами, рентгеновскими лучами.Точечные дефекты приводят к локальным изменениям межатомных расстояний и, следовательно, к искажениям кристаллической решетки.
2.Линейные дефекты, характеризуются малыми размерами в двух измерениях, но имеют значительную протяженность в третьем измерении. Наиболее важный вид линейных дефектов — дислокации(смещение). (краевые дислокаций, винтовые дислокации). Винтовая дислокация соответствует оси спиральной структуры в кристалле, характеризуемом искажением, которое присоединяется к нормальным параллельным плоскостям, вместе формирующим непрерывную винтовую наклонную плоскость (с одним периодом), вращающуюся относительно дислокации. Наиболее распространена так называемая смешанная дислокация, которая является любой комбинацией краевой и винтовой дислокаций.
Краевая дислакация— в кристаллографии линейный дефект структуры, связанный с наличием дополнительного неполного ряда частиц или отсутствием частиц на определенном отрезке ряда; характеризуется вектором сдвига, перпендикулярным дислокации; от винтовой дислокации отличается лишь расположением вектора сдвига относительно дислокации.
3. Поверхностные дефекты имеют малую толщину и значительные размеры в двух других измерениях. Обычно это места стыка двух ориентированных участков кристаллической решетки. Ими могут быть границы зерен, границы фрагментов внутри зерна, границы блоков внутри фрагментов.
4.Граница между зернами это узкая зона шириной 5–10 атомных расстояний с нарушенным порядком расположения атомов. В граничной зоне кристаллическая решетка одного зерна переходит в решетку другого.
Понятие сплав. Компоненты сплава. Фазы и структурные составляющие.
Сплав – вещество, полученное сплавлением нескольких элементов. Сплав – это твердое вещество, обладающее всеми признаками металлов и состоящее из 2-х и более химических элементов. Состоят из основы (одного или нескольких металлов), малых добавок специально вводимых в сплав легирующих и модифицирующих элементов, а также из неудалённых примесей (природных, технологических и случайных).
Компонент – элемент или химическое соединение, входящее в состав сплава. Компонент, кот. больше называется основным. Компоненты, вводимые в сплав для придания ему нужных свойств, называются легирующими.
Фазовая составляющая (фаза) – однородная часть сплава, характеризующаяся определенным составом, свойствами, типом кристаллической решетки и отделенная от других частей сплава поверхностью раздела. Сплавы могут быть и однофазными и многофазными. Однофазные сплавы всегда состоят из кристаллов твердого раствора одного вида (состава). В многофазных сплавах может одновременно присутствовать несколько структурных составляющих: 1) кристаллы твердого раствора (одного или нескольких составов), 2) кристаллы химических соединений, 3) кристаллы компонент сплава, 4) эвтектики и 5) эвтектоиды.
Основными структурами, составляющими железоуглеродистые сплавы, являются следующие.
Феррит – твердый раствор углерода. При температуре 723° С предельное содержание углерода 0,02 %. При отсутствии примесей не корродирует. Цементит – карбид железа Fe3C – химическое соединение, содержащее 6,67 % углерода. Является составной частью эвтектической смеси, а также самостоятельной структурной составляющей. Способен образовывать твердые растворы путем замещения атомами других металлов, неустойчив, распадается при термической обработке. Цементит хрупкий.
Аустенит – твердый раствор углерода. Атомы углерода внедряются в кристаллическую решетку, насыщение разное в зависимости от температуры и примесей. Устойчив только при высокой температуре, а с примесями Mn, Сг – при обычных, даже низких температурах.
Перлит – эвтектоидная смесь феррита и цементита, образуется при распаде аустенита при температуре 723° С и содержании углерода 0,83 %. Примеси Si и Мn способствуют образованию перлита и при меньшем содержании углерода.Структура перлита может быть пластинчатой и зернистой.
Ледебурит – эвтектическая смесь аустенита и цементита, образующаяся при 1130° С и содержании углерода 4,3 % Структура неустойчивая: при охлаждении аустенит, входящий в состав ледебурита, распадается на вторичный цементит и перлит.
Графит – мягкая и хрупкая составляющая чугуна, состоящая из разновидностей углерода. Встречается в серых и ковких чугунах.
Понятия о диаграммах фазового равновесия систем. Применение.
Это графическое отображение равновесного состояния бесконечной физико-химической системы при условиях, отвечающих координатам рассматриваемой точки на диаграмме.(выражающая зависимость состояния системы и фазовых равновесий в ней от внешних условий или ее состава, показывает какие фазы могут существовать при данных условиях.) Фазовые диаграммы позволяют узнать, какие фазы (т. е. однородные подсистемы, отличающиеся строением и/или свойствами от других) могут присутствовать в данной системе при данных условиях и составе.Для сложных систем, состоящих из многих фаз и компонентов, построение диаграмм состояния по экспериментальным данным и данным термодинамического моделирования является важнейшим способом предсказания поведения в ходе различных процессов.Анализ относительного расположения полей, разделяющих их поверхностей и линий, а также точек сочленения последних позволяет однозначно и наглядно определять условия фазовых равновесий, появления в системе новых фаз и химических соединений, образования и распада жидких и твердых растворов и т. п.
Фазовые диаграммы однокомпонентных систем изображаются на плоскости в координат. На них присутствуют поля, той или иной фазы вещества (газообразной, жидкой, различных твердых модификаций), разделенные линиями фазового равновесия, вдоль которых возможно сосуществование граничащих фаз. Места, где сходятся три разные линии фазовых равновесий, образуют тройные точки, в которых могут сосуществовать три фазы. Это максимальное число фаз, способных равновесно сосуществовать в однокомпонентных системах.
Помимо температуры и давления могут рассматриваться и другие параметры состояния системы, например, напряженность магнитного поля (H). Тогда фазовая диаграмма становится многомерной и рассматриваются различные ее сечения, например H–T, а в правиле фаз число 2 меняется на соответствующее число обобщенных сил (полей).
Основные виды диаграмм (5 видов).
1.Диаграмма состояния сплавов системы Pb – Sb. Диаграмма строится на основе использования кривых охлаждения, полученных методом термического анализа
2.Диаграмма состояния сплавов с неограниченной растворимостью компонентов в твердом состоянии (2 рода)
3. Диаграмма состояния сплавов с ограниченной растворимостью компонентов в твердом состоянии (3 рода), диаграмма с эвтектическим превращением.
4. Диаграмма состояния сплавов, испытывающих полиморфные превращения.
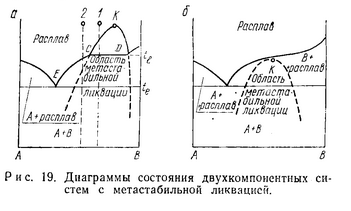
5. Диаграмма состояния двухкомпанентных систем с метастабильной ликвидацией.
1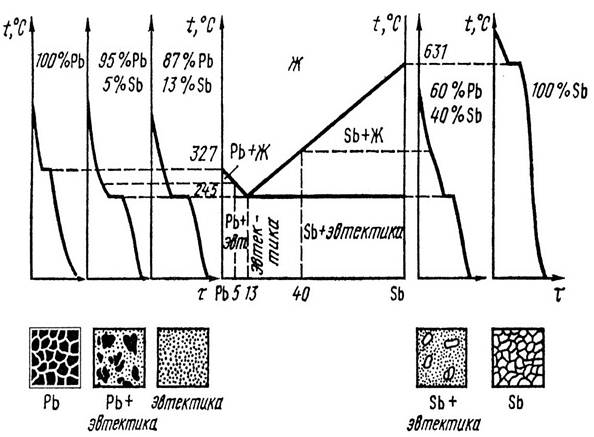 .Диаграмма
состояния сплавов системы Pb – Sb
Система сплавов Pb – Sb включает в себя
составы со 100% Pb и 0% Sb, т.е. чистый свинец
и со 100% Sb и 0% Pb , т.е. чистую сурьму. Кривые
охлаждения для чистых металлов имеют
по одному горизонтальному участку,
характеризующему температуру
кристаллизации: соответственно для
свинца 3270С и для сурьмы 6310С. На диаграмме
состояния эти температуры находятся
на осях ординат, где содержатся
соответственно чистый свинец и чистая
сурьма. Структура чистых металлов
представляет собой однородные зерна.
Сплав, содержащий 13% Sb и 87%Pb , также имеет
один горизонтальный участок, т.е. одну
критическую точку (2450С) – температуру
кристаллизации этого сплава. Принято
эвтектическую реакцию записывать так:
Ж → Pb + Sb или в общем виде Ж → А + В.
Кристаллизация любого сплава, имеющего
0% < Sb < 13% , начинается с выделения
кристаллов Pb. Эти сплавы затвердевают
в интервале температур и на кривых
охлаждения имеются две критические
точки, соответствующие началу и концу
затвердевания. Все они называются
доэвтектическими сплавами, претерпевают
эвтектическое превращение при охлаждении
ниже температуры 2450С и имеют после
окончания охлаждения структуру Pb + Э(Pb
+ Sb). В этой структуре имеется две
структурные составляющие: кристаллы и
эвтектика Э(Pb + Sb). Кристаллизация любого
сплава с концентрацией 100% > Sb > 13%
начинается с выделения кристаллов Sb.
Эти сплавы также затвердевают в интервале
температур, при охлаждении ниже
температуры 2450С в них протекает
эвтектическое превращение. Эти сплавы
называются заэвтектическими и имеют
после охлаждения окончательную структуру
Sb + Э(Pb + Sb).На диаграмме можно выделить
три характерные зоны: область, где
существует только жидкая фаза – выше
линий, ограниченной точками: температура
3270С – эвтектическая точка 2450С –
температура 6310С. Линия,
ограничивающая на диаграмме область
жидкой фазы сплавов, называется линией
ликвидус. Линия, ограничивающая область
полностью затвердевшего сплава от
остальной области на диаграмме, называется
линией солидус.
.Диаграмма
состояния сплавов системы Pb – Sb
Система сплавов Pb – Sb включает в себя
составы со 100% Pb и 0% Sb, т.е. чистый свинец
и со 100% Sb и 0% Pb , т.е. чистую сурьму. Кривые
охлаждения для чистых металлов имеют
по одному горизонтальному участку,
характеризующему температуру
кристаллизации: соответственно для
свинца 3270С и для сурьмы 6310С. На диаграмме
состояния эти температуры находятся
на осях ординат, где содержатся
соответственно чистый свинец и чистая
сурьма. Структура чистых металлов
представляет собой однородные зерна.
Сплав, содержащий 13% Sb и 87%Pb , также имеет
один горизонтальный участок, т.е. одну
критическую точку (2450С) – температуру
кристаллизации этого сплава. Принято
эвтектическую реакцию записывать так:
Ж → Pb + Sb или в общем виде Ж → А + В.
Кристаллизация любого сплава, имеющего
0% < Sb < 13% , начинается с выделения
кристаллов Pb. Эти сплавы затвердевают
в интервале температур и на кривых
охлаждения имеются две критические
точки, соответствующие началу и концу
затвердевания. Все они называются
доэвтектическими сплавами, претерпевают
эвтектическое превращение при охлаждении
ниже температуры 2450С и имеют после
окончания охлаждения структуру Pb + Э(Pb
+ Sb). В этой структуре имеется две
структурные составляющие: кристаллы и
эвтектика Э(Pb + Sb). Кристаллизация любого
сплава с концентрацией 100% > Sb > 13%
начинается с выделения кристаллов Sb.
Эти сплавы также затвердевают в интервале
температур, при охлаждении ниже
температуры 2450С в них протекает
эвтектическое превращение. Эти сплавы
называются заэвтектическими и имеют
после охлаждения окончательную структуру
Sb + Э(Pb + Sb).На диаграмме можно выделить
три характерные зоны: область, где
существует только жидкая фаза – выше
линий, ограниченной точками: температура
3270С – эвтектическая точка 2450С –
температура 6310С. Линия,
ограничивающая на диаграмме область
жидкой фазы сплавов, называется линией
ликвидус. Линия, ограничивающая область
полностью затвердевшего сплава от
остальной области на диаграмме, называется
линией солидус.
2. Диаграмма
состояния сплавов с неограниченной
растворимостью компонентов в твердом
состоянии (2 рода). Исходные
данные: оба к омпонента
неограничено растворимы в твердом и
жидком состоянии и не образуют химических
соединений.Компоненты: химические
элементы А, В (К = 2).Фазы: жидкость Ж,
кристаллы твердого раствора α (Ф =
2).Примером сплавов с такими диаграммами
состояния являются сплавы системы Cu –
Ni. На диаграмме есть три
области:
область выше
линии Аа/В – жидкость; область между
линиями Аа/В и Аb/В – жидкость и твердый
раствор.
Ниже лини Аb/B – область твердого раствора.
Линия Аа/В называется линией ликвидус;
линия Аb/B называется линией солидус.
Кристаллизация любого сплава начинается
выпадением из жидкого расплава отдельных
кристаллов твердого раствора α (например,
в точке а/) и заканчивается полным
затвердеванием твердого раствора
(например, в точке b/). Но так как в интервале
кристаллизации сплавы находятся в
двухфазном состоянии (Ж + α), то при
понижении температуры должно изменяться
соотношение количеств жидкой и твердой
фазы в двухфазной области – количество
жидкости уменьшается, а количество
α-твердого раствора растет. Кроме того,
при понижении температуры будут меняться
также составы жидкой и твержой фаз.
омпонента
неограничено растворимы в твердом и
жидком состоянии и не образуют химических
соединений.Компоненты: химические
элементы А, В (К = 2).Фазы: жидкость Ж,
кристаллы твердого раствора α (Ф =
2).Примером сплавов с такими диаграммами
состояния являются сплавы системы Cu –
Ni. На диаграмме есть три
области:
область выше
линии Аа/В – жидкость; область между
линиями Аа/В и Аb/В – жидкость и твердый
раствор.
Ниже лини Аb/B – область твердого раствора.
Линия Аа/В называется линией ликвидус;
линия Аb/B называется линией солидус.
Кристаллизация любого сплава начинается
выпадением из жидкого расплава отдельных
кристаллов твердого раствора α (например,
в точке а/) и заканчивается полным
затвердеванием твердого раствора
(например, в точке b/). Но так как в интервале
кристаллизации сплавы находятся в
двухфазном состоянии (Ж + α), то при
понижении температуры должно изменяться
соотношение количеств жидкой и твердой
фазы в двухфазной области – количество
жидкости уменьшается, а количество
α-твердого раствора растет. Кроме того,
при понижении температуры будут меняться
также составы жидкой и твержой фаз.
3 .
Диаграмма
состояния сплавов с ограниченной
растворимостью компонентов в твердом
состоянии (3 рода), диаграмма с эвтектическим
превращением.
.
Диаграмма
состояния сплавов с ограниченной
растворимостью компонентов в твердом
состоянии (3 рода), диаграмма с эвтектическим
превращением.
Исходные данные: оба компонента неограниченно растворимы в жидком состоянии, ограничено растворимы в твердом состоянии и не образуют химических соединений. Компоненты: химические элементы А и В (К = 2).Фазы: жидкость Ж, твердые растворы α (раствор компонента А в В) и β (раствор В в А) (Ф = 3).На диаграмме растворимость В в А не меняется с изменением температуры, а растворимость А в В – меняется. Линия GCH –линия ликвидус, линия GEDH –линия солидус.
4 .
Диаграмма
состояния сплавов, испытывающих
полиморфные превращения.Исходное
состояние: оба компонента неограниченно
растворимы в жидком состоянии, в твердом
состоянии могут образовывать механические
смеси в результате эвтектического или
перитекгического превращения, а могут
образовывать непрерывные твердые
растворы и кроме всего перечисленного,
хотя бы один из компонентов обладает
полиморфизмом. Компоненты:химические
элементы: А, В (К= 2). Фазы: жидкость Ж,
твердые растворы α, β, γ. При полиморфных
превращениях в сплавах происходит
перекристаллизация существующих
твердых фаз, которая подчиняется тем
же закономерностям, которые определяют
процесс кристаллизации из жидкого
состояния. Если в сплавах один или
оба компонента обладают полиморфизмом,
то и сами сплавы из этих компонентов
претерпевают полиморфные превращения
в твердом состоянии. В этом случае
диаграммы состояния становятся
«многоярусными», причем верхний ярус
диаграммы характеризует первичную
кристаллизацию из жидкого состояния,
а нижняя часть - вторичную (перекристаллизацию).
т.е. выделение кристаллов новой твердой
фазы из твердой первичной фазы, например,
кристаллов α-твердого раствора из
первичного β-твердого раствора с другой
кристаллической решеткой (рис. 14, а). В
общем случае вид рассматриваемой
диаграммы зависит от того, какие фазы
образуются в сплавах в процессе
полиморфных превращений. Всевозможных
вариантов может быть много. Но мы
рассмотрим два наиболее характерных
случая (рис. 14, а, б).
.
Диаграмма
состояния сплавов, испытывающих
полиморфные превращения.Исходное
состояние: оба компонента неограниченно
растворимы в жидком состоянии, в твердом
состоянии могут образовывать механические
смеси в результате эвтектического или
перитекгического превращения, а могут
образовывать непрерывные твердые
растворы и кроме всего перечисленного,
хотя бы один из компонентов обладает
полиморфизмом. Компоненты:химические
элементы: А, В (К= 2). Фазы: жидкость Ж,
твердые растворы α, β, γ. При полиморфных
превращениях в сплавах происходит
перекристаллизация существующих
твердых фаз, которая подчиняется тем
же закономерностям, которые определяют
процесс кристаллизации из жидкого
состояния. Если в сплавах один или
оба компонента обладают полиморфизмом,
то и сами сплавы из этих компонентов
претерпевают полиморфные превращения
в твердом состоянии. В этом случае
диаграммы состояния становятся
«многоярусными», причем верхний ярус
диаграммы характеризует первичную
кристаллизацию из жидкого состояния,
а нижняя часть - вторичную (перекристаллизацию).
т.е. выделение кристаллов новой твердой
фазы из твердой первичной фазы, например,
кристаллов α-твердого раствора из
первичного β-твердого раствора с другой
кристаллической решеткой (рис. 14, а). В
общем случае вид рассматриваемой
диаграммы зависит от того, какие фазы
образуются в сплавах в процессе
полиморфных превращений. Всевозможных
вариантов может быть много. Но мы
рассмотрим два наиболее характерных
случая (рис. 14, а, б).
5. Диаграмма состояния двухкомпанентных систем с метастабильной ликвидацией.
10 основных вопросов, решаемых с помощью диаграмм состояния.
С помощью диаграмм состояния для данных равновесных условий можно определить
1. число фаз в системе
2.относительное количество каждой из фаз
3.состав каждой фазы и ее природу (чистый компонент, твердый раствор, соединение).
Экспериментальное и теоретическое построение диаграмм состояния является главным путем в решении проблемы 4.описания гетерогенных равновесий при анализе реальных систем. В основе физико-химического анализа лежит изучение функциональной зависимости между значениями физических свойств и параметрами Р, Т, Х. 5.Знание этих зависимостей позволяет устанавливать физико-химическую природу фаз и границы их существования. Изучение диаграмм состояния помогает выбрать 6.оптимальные составы смесей и сплавов. 7.определить эффективность процессов разделения и 8.глубокой очистки веществ при перегонке (процесс перегонки жидкого металла для разделения его на отличные по составу компоненты).
