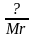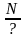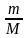- •Тема 1: Основные химические понятия.
- •Ход урока
- •I. Организационно-психологический этап
- •II. Ориентировочно-мотивационный этап
- •III. Операционно-познавательный этап
- •IV. Контрольно-корректирующий этап
- •V. Рефлексивный этап
- •Молярный объем газов
- •Тема 1: Основные химические понятия.
- •Ход урока
- •I. Организационно-психологический этап
- •II. Ориентировочно-мотивационный этап
- •III. Операционно-познавательный этап
- •IV. Контрольно-корректирующий этап
- •V. Рефлексивный этап
- •Химические свойства воды
- •Тема 5: Вода.
- •Ход урока
- •I. Организационно-психологический этап
- •II. Ориентировочно-мотивационный этап
- •III. Операционно-познавательный этап
- •IV. Контрольно-корректирующий этап
- •V. Рефлексивный этап
- •Повторение и обобщение изученного материала по теме «вода»
- •Тема 5: Вода.
- •Ход урока
- •I. Организационно-психологический этап
- •II. Ориентировочно-мотивационный этап
- •III. Операционно-познавательный этап
- •Примерный перечень вопросов и ответов
- •Вода реагирует с
- •IV. Рефлексивный этап
- •Гимн химиков
- •Строение атома
- •Тема 1: Строение атома и систематизация химических элементов.
- •Организационно-психологический этап (1 мин)
- •Ориентировочно-мотивационный (6-8 мин)
- •Содержательно-деятельностный этап (30мин)
- •Рефлексивно-оценочный этап (6 мин)
- •§ 7 Учебника, упражнения 4, 5, 6 с. 36 учебника – для всех.
- •Изотопы. Понятие о природе радиоактивности
- •Тема 1: Строение атома и систематизация химических элементов.
- •Организационно-психологический этап (1-2 мин)
- •Ориентировочно-мотивационный этап (10-12 мин)
- •Операционально-познавательный этап (15 мин)
- •IV Контрольно-коррекционный (10 мин)
- •V. Рефлексивно- диагностический этап (6 мин)
- •Роль периодического закона для развития естествознания: обобщение знаний по теме
- •Тема 1: Строение атома и систематизация химических элементов.
- •Ход урока
- •I. Организационно-психологический этап
- •II. Ориентировочно-мотивационный этап
- •Раунд 2 Путешествие по периодической системе
- •Раунд 3 Некоторые факты из биографии д.И.Менделеева
- •Раунд 4 Знакомы ли вы с химическими веществами?
- •Тема 2: Химическая связь.
- •Ход урока
- •Строение молекулы воды. Вода как универсальный растворитель. Растворы
- •Тема 3: Растворы.
- •Жесткость воды и способы ее устранения. Обобщение знаний по теме «растворы»
- •Тема 3: Растворы
- •Ход урока
- •I. Организационно-психологический этап
- •II. Ориентировочно-мотивационный этап
- •III. Операционно-познавательный этап
- •Инструктивная карточка
- •IV. Контрольно-коррекционный этап
- •V. Рефлексивный этап
- •Общие химические свойства металлов
- •Тема 4: Металлы
- •I. Организационно-психологический этап
- •П. Ориентировочно-мотивационный этап
- •III. Операционно-познавательный этап
- •IV. Контрольно-коррекционный этап
- •I этап.
- •II. Этап.
- •V. Рефлексивный этап
- •§35. Задания 4-8
- •Галогены
- •Тема 1: Неметаллы.
- •Ход урока
- •I. Организационно-психологический этап
- •II. Ориентировочно-мотивационный этап
- •III. Операционно-познавательный этап
- •Химические свойства галогенов
- •IV. Контрольно-коррекционный этап
- •V. Рефлексивный этап
- •Кислород и сера
- •Тема 1: Неметаллы.
- •Ход урока
- •I. Организационно-психологический этап
- •II. Ориентировочно-мотивационный этап
- •III. Операционно-познавательный этап
- •IV. Контрольно-коррекционный этап
- •V. Рефлексивный этап
- •Химические свойства и применение серной кислоты
- •Тема 1: Неметаллы
- •Ход урока
- •I. Организационно-психологический этап
- •II. Ориентировочно-мотивационный этап
- •III. Операционно-познавательный этап
- •IV. Контрольно-коррекционный этап
- •V. Рефлексивный этап
- •Тема 1: Неметаллы
- •Ход урока
- •I. Организационно-психологический этап
- •II. Ориентировочно-мотивационный этап
- •III. Операционно-познавательный этап
- •IV. Контрольно-коррекционный этап
- •V. Рефлексивный этап
- •Минеральные удобрения
- •Тема 1: Неметаллы
- •Ход урока
- •I. Организационно-психологический этап
- •II. Ориентировочно-мотивационный этап
- •III. Операционно-познавательный этап
- •IV. Контрольно-коррекционный этап
- •V. Рефлексивный этап
- •Общая характеристика органических соединений. Структурные и молекулярные формулы углеводородов
- •Тема 2: Введение в органическую химию. Углеводороды.
- •Ход урока
- •I. Организационно-психологический этап
- •II. Ориентировочно-мотивационный этап
- •III. Операционно-познавательный этап
- •IV. Контрольно-коррекционный этап
- •V. Рефлексивный этап
- •Алканы. Метан
- •Тема 2: Введение в органическую химию. Углеводороды.
- •Номенклатура алканов
- •Тема 2: Введение в органическую химию. Углеводороды.
- •Ход урока
- •I. Организационно-психологический этап
- •II. Ориентировочно-мотивационный этап
- •III. Операционно-познавательный этап
- •IV. Контрольно-коррекционный этап
- •V. Рефлексивный этап
- •Основные источники углеводородов
- •Тема 2: Введение в органическую химию. Углеводороды.
- •Ход урока
- •I. Организационно-психологический этап
- •II. Ориентировочно-мотивационный этап
- •III. Операционно-познавательный этап
- •IV. Контрольно-коррекционный этап
- •V. Рефлексивный этап
Молярный объем газов
Дидактический сценарий урока по учебному предмету «Химия» в VII классе
Тема 1: Основные химические понятия.
Количество часов в изучаемой теме: 15.
Место урока в изучаемой теме: 11.
Цель урока: ознакомление с понятием «молярный объем газов». Формирование умений решать расчетные задачи с использованием данного понятия.
Задачи урока:
Обучающие
ознакомить учащихся с понятием «молярный объем», и обозначением данной величины.
Развивающие
формировать умение решать задачи с употреблением понятий «молярная масса», «молярный объем»;
продолжить формирование умений анализировать, сравнивать, сопоставлять на материале данной темы
Воспитательные
расширять кругозор учащихся за счет установления межпредметных связей со школьными курсами физики и математики;
совершенствовать навыки самостоятельной работы и деятельности в группе.
Тип урока: урок – изучение нового материала.
Материалы и оборудование к уроку: таблица «Молярные массы и молярные объемы некоторых веществ», куб объемом 22,4 дм3, карточки-задания.
Методы обучения: письменная проверочная работа, беседа, решение расчетных задач.
Формы деятельности учащихся: индивидуальная, фронтальная, групповая работа в парах.
Ход урока
I. Организационно-психологический этап
Задача учителя: психологически подготовить школьников к совместной деятельности на уроке, создать благоприятную эмоциональную обстановку на уроке, раскрыть основные задачи урока.
II. Ориентировочно-мотивационный этап
Задача учителя: актуализировать опорные знания учащихся, сформировать познавательные мотивы к восприятию нового материала.
В начале урока с целью проверки знаний учащихся и подготовки их к восприятию нового материала проводим фронтальный опрос по домашнему заданию, а затем письменную самостоятельную работу, используя карточки-задания по 4-м вариантам.
№п/п |
Задания |
Вариант 1 |
Вариант 2 |
Вариант 3 |
Вариант 4 |
1. |
Допишите формулу: |
w(Э)= |
n
=
|
? =
|
M=численно |
2. |
Определите массу, если известно количество вещества… |
О2 0,2 моль |
H2O 1,5 моль
|
N2 0,5 моль
|
CО2 0,75 моль
|
3. |
Определите количество вещества, если известна масса… |
Н2 10г |
СО 14г |
SO2 6,4г |
NН3 8,5г
|
III. Операционно-познавательный этап
Задача учителя: ознакомить учащихся с понятиями «молярный объем газов», обозначением данной величины и сформировать умение решать задачи с использованием этих понятий.
Изучение нового материала проводим с использованием поисковых методов обучения в сочетании с дедуктивными методами: от вывода формулы, выражающей зависимость между молярной массой и молекулярным объемом к решению частных задач.
Выясняем вопрос (опираясь на знания учащихся по физике): какую зависимость можно установить между массой вещества и объемом, который занимает это вещество?
V
=
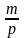
Предлагаем заменить m на M и получаем формулу:
Vm
=
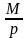
Vm – молярный объем (объем одного моля), его выражают в м3/моль.
Предлагаем учащимся, пользуясь справочными данными рассчитать молярный объем для воды (Н2О) и серной кислоты (H2SO4).
Химическая формула |
Агрегатное состояние при н.у. |
Молярная масса (М) |
Плотность вещества (ρ) |
Молярный объем (Vm) |
Н2О |
ж |
18г/моль |
1000г/дм3 |
|
H2SO4 |
ж |
98г/моль |
1980г/дм3 |
|
Vm(Н2О) = 0,018 дм3/моль
Vm(H2SO4 ) = 0,053 дм3/моль
Далее акцентируем внимание учащихся на газообразном состоянии вещества. Выясняем: какое влияние оказывают температура и давление на свойства газов? Делаем вывод, что при вычислении Vm следует оговорить, что газы находятся при определенных условиях, т.е. нормальных условиях:
t = 00C; p = 101,325кПа.
Предлагаем учащимся рассчитать молярный объем некоторых газов (Н2; О2; СО2), используя карточку-задание.
Формулу вещества (в скобках указан вариант) |
Молярная масса (М) |
Плотность при н.у. (ρ) |
Молярный объем (Vm) |
Н2 (1 вариат) |
≈ 2 г/моль |
0,09 г/дм3 |
|
O2 (2 вариат)) |
≈ 32 г/моль |
1,43 г/дм3 |
|
CO2 (3 вариат)) |
≈ 44 г/моль |
1,97 г/дм3 |
|
Vm(Н2) ≈ 22,4 дм3/моль
Vm(О2) ≈ 22,4 дм3/моль
Vm(СО2) ≈ 22,4 дм3/моль
Записываем ответы на доске и сравниваем. Учащиеся делают выводы: Vm применяют только для газов, т.к. при н.у. Vm (всех газов) 22,4 дм3/моль. Демонстрируем учащимся куб 22,4 дм3. Делаем вывод, молярный объем Vm находится по отношению объема порции газа(V) к соответствующему количеству вещества этой порции:
Vm
=
 ,
отсюда
n
=
,
отсюда
n
= ;
V
= Vm
• n
;
V
= Vm
• n