
Буферные системы крови.
Плазма крови.
Нормальное значение рН крови 7.40 ± 0.05, т.е. а(Н+) ≈ 3.7 . 10-8 – 4 . 10-8 моль/л. Постоянство этих величин обеспечивается одновременным действием гидрокарбонатной, фосфатной, белковой и аминокислотной буферных систем.
Гидрокарбонатная.
Особенность этой системы состоит в том, что один из компонентов системы – H2CO3 образуется при взаимодействии CO2 с H2O.
![]()
В свою очередь концентрация СО2 определяется равновесием
![]()
которое описывается законом Генри

Т. о. в крови устанавливается равновесие
![]()
В соответствии с уравнением 1 значение рН гидрокарбонатного буфера в конечном счёте определяется концентрацией НСО3- и парциальным давлением СО2:
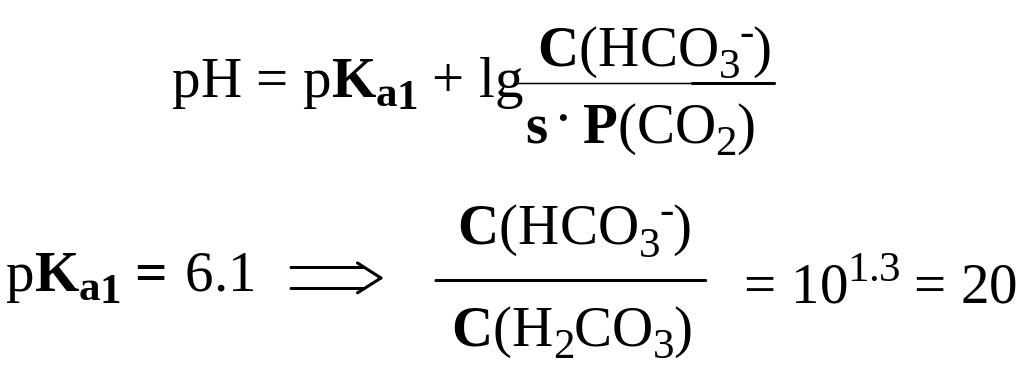
Очевидно, что ёмкость гидрокарбонатной системы по кислоте значительно превышает этот показатель по щёлочи (таблица 2).
Между СО2 в альвеолах и гидрокарбонатным буфером в плазме крови устанавливается равновесие:
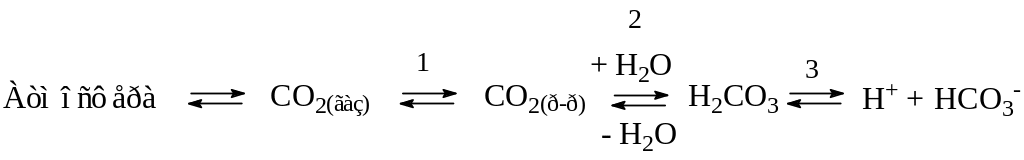
При поступлении в кровь доноров протонов равновесие 3 смещается в сторону Н2СО3. При этом концентрация Н2СО3 возрастает, а концентрация НСО3- снижается. Это приводит к смещению равновесия 2 влево, в результате чего равновесие 1 смещается в сторону образования газообразного СО2 , что приводит к повышению давления СО2 в лёгких и выведению его за счёт увеличения лёгочной вентиляции.
При поступлении акцепторов протонов равновесие смещается в обратном направлении, что приводит к растворению в плазме крови дополнительного количества СО2, содержащегося в лёгких.
В результате описанных процессов гидрокарбонатная буферная система эффективно обеспечивает постоянство рН плазмы крови. Эта система содержится также в эритроцитах и почечной ткани.
2. Фосфатная буферная система.

Ёмкость данной системы по кислоте выше ёмкости по щелочи (таблица 2). Фосфатная буферная система менее мощная, чем гидрокарбонатная, что обусловлено малым содержанием фосфатов в плазме крови.
Фосфатная система содержится также в тканях, почках, эритроцитах.
Белковая буферная система – представляет собой совокупность альбуминов и глобулинов.
При физиологическом значении рН = 7.40 белки находятся преимущественно в форме «белок – основание» и соль «белка – основания» и ёмкость по кислоте буферной системы выше ёмкости по щелочи (таблица 2).
Аминокислотные буферные системы.
Почти все аминокислоты имеют значения рН заметно отличающиеся от 7.4 и мощность их невелика.
Таким образом, мощность буферных систем плазмы крови убывает в ряду Н2СО3/НСО3- >белки > Н2РО4-/НРО42- > аминокислоты.
Эритроциты.
рН эритроцитов в норме 7.25 ± 0.05. Действуют гидрокарбонатная и фосфатная буферные системы. Их мощность невелика по сравнению с мощностью в плазме крови. Большую роль играет система гемоглобин – оксигемоглобин, на долю которой приходится около 80% всей буферной ёмкости цельной крови.
Гемоглобин – слабая кислота (рКа = 8.2), диссоциирует по схеме:
![]()
Недиссоциированной
части больше, т.е.
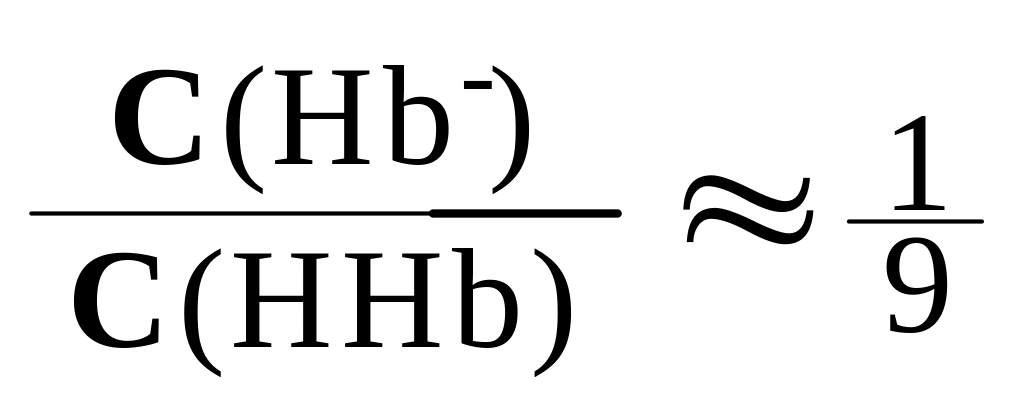 , следовательно буферная ёмкость системы
HHb/Hb-
выше по щёлочи, чем по кислоте (таблица
2).
, следовательно буферная ёмкость системы
HHb/Hb-
выше по щёлочи, чем по кислоте (таблица
2).
В легких HHb реагирует с О2,
![]()
образуя оксигемоглобин, который переносится кровью в капиллярные сосуды, откуда О2 попадает в ткани. HHbO2 – слабая кислота –рКа (HHbO2) = 6.95. Поэтому при действии доноров протонов их в первую очередь будет нейтрализовать анион Hb-
![]()
т.к. имеет большее сродство к Н+. Но при действии оснований – акцепторов протонов – в первую очередь будет реагировать оксигемоглобин
![]()
Система HHbO2/HbO2- осуществляет также протонирование HCO3- ионов с последующим выделением СО2 через легкие:
![]()
Необходимо также отметить участие эфиров фосфорных кислот в поддержании постоянства рН. Фосфолипиды являются слабыми кислотами. рКа диссоциации полярных фосфатных групп находятся в интервале 6.8-7.2. Поэтому при физиологическом значении рН=7.25 фосфолипиды мембран эритроцитов находятся как в виде ионизированной, так и неионизированной формы. При этом соотношение ионизированной и неионизированной форм составляет примерно 3:1.
Вывод – сама мембрана эритроцитов обладает буферным действием, поддерживая постоянство рН внутренней среды эритроцитов.
Резюме – совокупное действие нескольких буферных систем обеспечивает кислотно-основной гомеостаз в организме.
Таблица 2.
