
7.2.4. Убихинон
Убихинон (коэнзим Q) – жирорастворимое витаминоподобное вещество, производное бензохинона, обладающее антиоксидантными свойствами. Важнейшая роль убихинона заключается в его участии в митохондриальной цепи электронного транспорта в качестве кофермента (Ленинджер А., 1976). Основная часть внутриклеточного убихинона сконцентрирована в митохондриях (40–50%). Также убихинон обнаружен в ядрах, эндоплазматическом ретикулуме, лизосомах, аппарате Гольджи, но здесь его концентрации гораздо ниже, чем в митохондриях. Так как убихинон участвует в метаболизме, то его наибольшая концентрация определена в органах с наиболее высоким уровнем энергетического обмена – сердце, печени, почках.
Восстановление окисленной формы убихинона постоянно осуществляется с помощью ферментных систем. Выраженная антиоксидантная активность коэнзима Q, связана именно с образованием окислительно-восстановительной системы убихинол-убихинон (см. рис. 4.3). Антиоксидантное действие убихинона заключается в прерывании цепных процессов ПОЛ за счет связывания свободных радикалов, что защищает клетку от повреждения и препятствует образованию окисленных липидов и запуску процессов атерогенеза. Подавляя процессы пероксидации, он, как большинство антиоксидантов, обладает способностью повышать толерантность клеток к гипоксии (Кулинский В.И., 1990). При включении убихинона в комплексную терапию больных с ишемической болезнью сердца появляются позитивные изменения в клиническом течении заболевания, сокращается частота приступов стенокардии, что сопровождается снижением интенсивности ПОЛ и повышением активности антиоксидантной защиты (Langsjoen P.H. et al., 1999; Лакомкин В.Л. и др., 2002; Аронов Д.М., 2004). Также он участвует в защите ДНК от действия АФК, снижая риск развития различных мутаций. Коэнзим Q восстанавливает витамин Е и не допускает образования из него феноксил-радикалов, оказывая таким образом непрямое антиоксидантное действие (Ланкин В.З. и др., 2004).
7.2.5. Тиоктовая кислота
Тиоктовая кислота (α-липоевая кислота, витамин N) является распространённым в природе коферментом, который связан с ферментами класса оксидоредуктаз пептидной связью (Passwater R.A., 1995).
Тиоктовая кислота участвует в переносе ацильных групп и в реакциях окислительного декарбоксилирования. При этом окисленная форма тиоктовой кислоты переходит в восстановленную, которая затем под действием специфического фермента вновь превращается в окисленную:
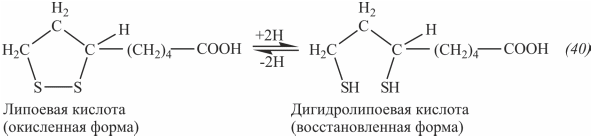
Наибольшее количество свободной формы липоевой кислоты обнаружено в сердце (Strodter D. et al., 1995).
Тиоктовая кислота обладает высокой гидрофобностью, что позволяет ей беспрепятственно проникать через биологические мембраны.
Антиоксидантный эффект тиоктовой кислоты обусловлен наличием двух тиоловых групп в молекуле, а также способностью связывать молекулы радикалов и ионы металлов, тем самым предотвращая их участие в ПОЛ. Получены убедительные доказательства того, что тиоктовая кислота не только обладает самостоятельным антиоксидантным потенциалом, но и обеспечивает мощную поддержку работы других антиоксидантных звеньев в организме: глутатиона, убихинона, супероксиддисмутазы и каталазы (Щербак А.В., 2002). Тиоктовая кислота усиливает эндоневральный кровоток, предотвращая ингибирование NO-синтетазы и таким образом, предупреждает ишемическое повреждение нервной ткани. Было выявлено ее участие в ускорении процессов проведения импульса по нерву, а также нормализации уровня глутатиона (Nagamatsu M. et al., 1995).
α-Липоевая кислота предотвращает обусловленную свободными радикалами активацию транскрипционного фактора NF-kB, который стимулирует выработку эндотеллина-1 и тканевого эндотелиального фактора, являющихся важным звеном в патогенезе диабетической нейропатии (Верткин А.Л. и др.). α-Липоевая кислота способствуют снижению уровня токсичных свободнорадикальных соединений, образованных в результате реакций образования гидрофильных пероксильных радикалов (Rosenburg H.R., et al., 1959; Scholich H. et al., 1989; Scott B.C. et al., 1994).
Восстановленная форма тиоктовой кислоты может участвовать в обмене железа, связанного с ферритином, что сопровождается образованием комплексов в виде ферритной формы. Это, очевидно, может отражаться на скорости реакции Фентона, генерирующей гидроксильный радикал, так как Fe2+ компонентом данной реакции. (Бустаманте Д. и др., 2001).
