
- •Предисловие
- •Неорганические лекарственные средства Алгоритм изучения неорганических лекарственных средств.
- •VII группа периодической системы д.И.Менделеева. Соединения галогенов.
- •Соединения галогенов с другими элементами находят большое применение в медицине.
- •Кислота хлористоводородная
- •Кислота хлористоводородная разведенная
- •Натрия хлорид
- •Калия хлорид
- •Натрия бромид
- •Калия бромид
- •Натрия йодид
- •Калия йодид
- •Йод и его спиртовые растворы
- •VI группа периодической системы д.И.Менделеева Соединения кислорода. Перекись водорода. Соединения серы. Натрия тиосульфат.
- •Вода очищенная
- •Перекись водорода
- •Раствор перекиси водорода
- •Натрия тиосульфат
- •IV и III группы Периодической системы д.И.Менделеева Соединения бора и углерода.
- •Кислота борная
- •Натрия тетраборат
- •Натрия гидрокарбонат
- •II и I группы периодической системы д.И.Менделеева. Соединения магния, кальция, цинка.
- •Магния сульфат
- •Кальция хлорид
- •Цинка сульфата
- •Соединения серебра.
- •Серебра нитрат
- •Колларгол
- •Протаргол
- •Органические лекарственные средства Алгоритм изучения органических лекарственных средств.
- •Ациклические и карбоциклические лекарственные средства Спирты
- •Спирт этиловый 95 %
- •Альдегиды и их производные
- •Раствор формальдегида
- •Гексаметилентетрамин
- •Углеводы (глициды)
- •Глюкоза
- •Простые эфиры
- •Димедрол
- •Карбоновые кислоты, аминокислоты и их производные
- •Кислота аскорбиновая
- •Натрия цитрат для инъекций
- •Натрия гидроцитрат (двузамещенный) для инъекций
- •Кальция глюконат
- •Кальция лактат
- •Аминокислоты
- •Кислота глютаминовая
- •Кислота аминокапроновая
- •Аминоспирты и их производные
- •Эфедрина гидрохлорид
- •Адреналина гидротартрат
- •Терпеноиды. Тепингидрат, ментол, валидол, бромкамфора. Роль современных ученых в разработке полусинтетического метода получения камфоры.
- •Валидол
- •Камфора
- •Бромкамфора
- •Терпингидрат
- •Ароматические соединения Фенолы
- •Резорцин
- •Ароматические кислоты
- •Кислота бензойная
- •Натрия бензоат
- •Кислота салициловая
- •Натрия салицилат
- •Кислота ацетилсалициловая
- •Фенилсалицилат
- •Ароматические аминокислоты и их производные
- •Анестезин
- •Бензокаин
- •Новокаин
- •Ацетаминопроизводные ароматического ряда
- •Парацетамол
- •Лидокаина гидрохлорид
- •Тримекаин
- •Сульфаниламидные препараты. Общая характеристика. Амиды сульфаниловой кислоты
- •Механизм антимикробного действия сульфаниламидов
- •Свойства сульфаниламидных препаратов
- •Методы количественного определения.
- •Стрептоцид
- •Стрептоцид растворимый
- •Сульфацил-натрий
- •Норсульфазол
- •Фталазол
- •Сульфадимезин
- •Гетероциклические соединения
- •Производные пиразола и фурана
- •Антипирин
- •Анальгин
- •Бутадион
- •Производные фурана
- •Фурацилин
- •Производные имидазола
- •Пилокарпина гидрохлорид
- •Производные бензимидазола
- •Дибазол
- •Производные пиридина
- •Пиридоксина гидрохлорид
- •Кислота никотиновая
- •Никотинамид
- •Производные пиримидина
- •Тиамина бромид (хлорид)
- •Производные пиперидина
- •Промедол
- •Производные тропана
- •Атропина сульфат
- •Производные хинолина
- •Хинина дигидрохлорид
- •Хинина гидрохлорид
- •Хинина сульфат
- •Производные изохинолина
- •Папаверина гидрохлорид
- •Производные барбитуровой кислоты
- •Барбитал
- •Барбитал - натрий
- •Фенобарбитал
- •Этаминал - натрий
- •Производные фенантренизохинолина
- •Морфина гидрохлорид
- •Кодеина фосфат
- •Этилморфина гидрохлорид
- •Производные пурина
- •Кофеин-бензоат натрия
- •Теобромин
- •Теофиллин
- •Эуфиллин
- •Производные изоаллоксозина
- •Рибофлавин
- •Антибиотики
- •Производные ароматического ряда
- •Левомицетин
- •Пенициллины (лактамиды)
- •Бензилпенициллина калиевая соль
- •Бензилпенициллина натриевая соль
- •Феноксиметилпенициллин
- •Полусинтетические пенициллины
- •Общая структура пенициллинов
- •Приложения Качественные реакции на катионы
- •Критерии оценки знаний по фармацевтической химии
- •Список литературы
Резорцин

м-Диоксибензол
С6Н6О2 |
М.в. 110,11 |
Получение. Получают из бензола.
Описание. Белый или белый со слабым желтоватым оттенком кристаллический порошок со слабым характерным запахом. Под влиянием света и воздуха постепенно окрашивается в розовый цвет.
Растворимость. Очень легко растворим в воде и 95% спирте, легко растворим в эфире, очень мало растворим в хлороформе, растворим в глицерине и жирном масле.
Подлинность.
1) При прибавлении к раствору препарата раствора хлорида окисного железа появляется сине-фиолетовое окрашивание, переходящее от прибавления раствора аммиака в буровато-желтое.
2) При сплавлении в фарфоровой чашке нескольких кристаллов препарата с избытком фталевого ангидрида получается плав желто-красного цвета. При растворении плава в растворе едкого натра появляется интенсивная зеленая флюоресценция.
Температура плавления 109—112°.
Количественное определение.
Броматометрический метод (вариант обратного титрования).
Точную навеску препарата помещают в мерную колбу, растворяют в воде, прибавляют избыток 0,1М KBrO3, KBr, H2SO4, затем к смеси прибавляют раствор йодида калия, смесь сильно взбалтывают и оставляют на 10 минут в темном месте. После этого добавляют хлороформ и титруют выделившийся йод 0,1М раствором тиосульфата натрия до обесцвечивания.
KBrO3 + 5KBr + 3H2SO4 → 3Br2 + 3K2SO4 + 3H2O

Br2 + 2KJ = J2 + 2KBr
J2 + 2Na2S2O3 = 2NaJ + Na2S4O6
УЧ = 1/6, формула обратного титрования
C%
=
![]()
Хранение. В хорошо укупоренных банках оранжевого стекла.
Применение. Антисептическое средство, при кожных заболеваниях, экземе, наружно в мазях, пастах или растворах, редко применяется внутрь как средство, дезинфицирующее ЖКТ.
Резорцин несовместим с тимолом, ментолом, аспирином, камфорой (образует сыреющие смеси).
Легко разлагается (в щелочной среде) – окисляется, восстанавливает препараты ртути до металлической.
См. Учебно-методическое пособие по внутриаптечному контролю: глазные капели - раствор резорцина 1%.
Ароматические кислоты
Ароматические кислоты – это органические соединения, имеющие функциональную группу –COOH, а в качестве радикала бензольное ядро.
Простейший представитель – бензойная кислота.

Свойства ароматических кислот определяются:
1. Свойствами бензольного ядра, для которого характерны:
1.1. Реакции замещения водорода в ядре на галоген, NO2-, SO32- - группы.
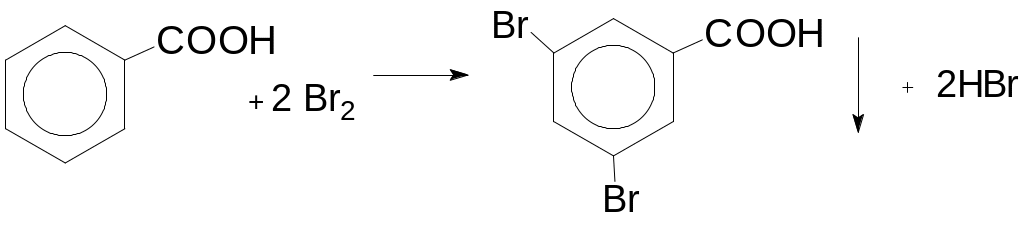
|
Дибромбензойная кислота |
2. Свойствами – COOH группы.
2.1. Образовывать соли со щелочными, тяжелыми металлами, щелочами, карбонатами щелочных металлов.

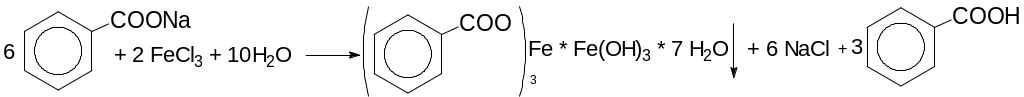
2.2. Образовывать ангидриды, галогенангидриды, амиды.

2.3. Образовывать сложные эфиры в присутствии концентрированной серной кислоты.

|
этилбензоат |
3. Реакция среды ароматических кислот определяется по индикаторам (кислая).

Свободные ароматические кислоты применяют только наружно, т.к. диссоциируя на ионы, отщепляют ион H+, который обладает раздражающим действием, даже прижигающим. Кроме того, попадая в кровь, изменяет структуру кровяных телец, поэтому внутрь назначают только соли и сложные эфиры ароматических кислот.
Acidum benzoicum
