
- •Методичні вказівки і завдання з контрольної роботи
- •Методичні вказівки по виконанню завдань контрольної роботи
- •Завдання до контрольної роботи
- •Приклади рішення задач
- •Рішення
- •Рішення
- •Рішення
- •Рішення Ізотермічний процес.
- •Ізобарний процес. Теплота ізобарного процесу:
- •Рішення
- •Рішення Рівняння теплопередачі:
- •Рекомендована література Основна
- •Додаткова
Приклади рішення задач
ПРИКЛАД 1.
Суміш газів, яка складається з 0,3
кіломолів СО2 та
0,7 кіломолів N2,
з початковими параметрами
![]() МПа і
МПа і
![]() К розширюється до кінцевого об’єму
К розширюється до кінцевого об’єму
![]() .
Розширення здійснюється по ізотермі,
по адіабаті та по політропі з показником
.
Розширення здійснюється по ізотермі,
по адіабаті та по політропі з показником
![]() .
Визначити газову сталу суміші, її масу,
кінцеві параметри суміші, роботу
розширення, теплоту процесу, зміну
внутрішньої енергії, ентальпії та
ентропії. Дати таблиці результатів та
їх аналіз. Показати процеси в pv-
та Ts-координатах.
.
Визначити газову сталу суміші, її масу,
кінцеві параметри суміші, роботу
розширення, теплоту процесу, зміну
внутрішньої енергії, ентальпії та
ентропії. Дати таблиці результатів та
їх аналіз. Показати процеси в pv-
та Ts-координатах.
Рішення
Маса суміші:
![]() ,
,
![]() ;
;![]() ,
,
де
![]() —
мольні частки компонентів суміші;
—
мольні частки компонентів суміші;
![]() —
молекулярні маси компонентів суміші.
—
молекулярні маси компонентів суміші.
Тоді:
![]() кг.
кг.
Молекулярна маса суміші чисельно дорівнює її масі, адже:
![]()
Тоді газова стала суміші:
![]() КДж/кг.
КДж/кг.
Початковий об’єм суміші визначимо з рівняння стану:
![]() м3.
м3.
Кінцевий об’єм:
![]() м3.
м3.
Роботу розширення, теплоту та зміну внутрішньої енергії, ентальпії та ентропії визначаємо для кожного процесу окремо.
Ізотермічне розширення.
Для даного процесу:
![]() ;
;
![]() МПа.
МПа.
При Т=Const, ![]() ,
,
![]() ,
,
![]()
Зміна ентропії:
![]()
Адіабатне розширення.
Зв’язок між параметрами адіабатного процесу:
![]() .
.
Показник адіабати:
![]() ,
,
де
![]() і
і
![]() — середні мольні теплоємкості суміші
газів при постійному тиску та
постійному об’ємі.
— середні мольні теплоємкості суміші
газів при постійному тиску та
постійному об’ємі.
Оскільки мольні та об’ємні частки компонентів суміші однакові, то:
![]() ;
;
![]() .
.
Теплоємкості та для відповідних газів знаходимо по таблицях.
![]() ;
;
![]() ;
;
![]() .
.
Тоді:
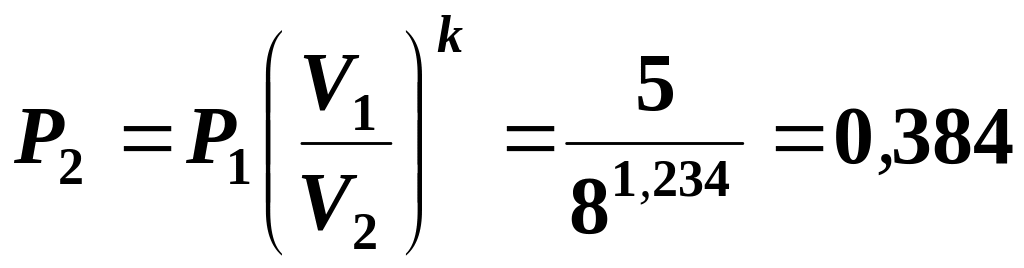 МПа.
МПа.
Температура:
 К.
К.
Робота розширення суміші газів:
![]() кДж.
кДж.
В адіабатному процесі:
![]() кДж;
кДж;
![]() .
.
Зміна ентропії також
![]() ,
тому що:
,
тому що:
![]() .
.
Зміна ентальпії:
![]()
Політропний процес.
Залежність між параметрами стану:
![]() ,
,
звідки:
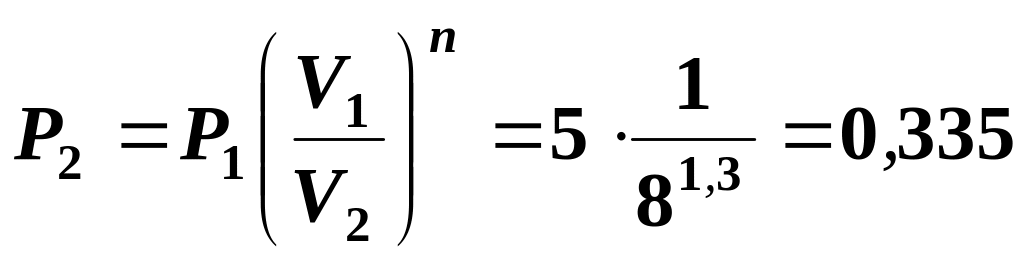 МПа.
МПа.
Температура в кінці розширення:
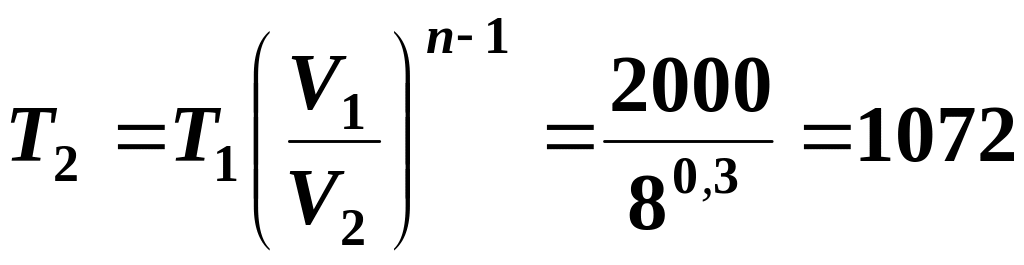 К.
К.
Робота політропного розширення суміші:
![]() кДж.
кДж.
Кількість теплоти, що бере участь у процесі:
![]()
Тобто в результаті розширення від суміші в навколишнє середовище відводиться 5949 кДж теплоти.
Згідно з 1-м законом термодинаміки:
![]() ,
,
Тоді:
![]() кДж.
кДж.
Внутрішня енергія при розширенні зменшується.
Зміну ентальпії суміші при політропному розширенні знаходимо за загальним виразом:
![]() кДж;
кДж;
![]() .
.
Тобто ентальпія суміші зменшується при політропному розширенні.
Зміна ентропії при політропному розширенні:
![]()
Результати розрахунків заносимо в таблицю:
Параметр суміші газів |
Р1, МПа |
Р2 МПа |
Т1, К |
Т2, К |
V1, М3 |
V2, М3 |
Q, кДж |
L, кДж |
кДж |
кДж |
|
Ізо-термічний |
5 |
0,625 |
2000 |
2000 |
3,31 |
26,48 |
34512 |
34512 |
0 |
0 |
11,26 |
Адіабатний |
5 |
0,384 |
2000 |
1229 |
3,31 |
26,48 |
0 |
27342 |
-27342 |
-33615 |
0 |
Політропний |
5 |
0,335 |
2000 |
1072 |
3,31 |
26,48 |
-5949 |
25669 |
-31618 |
-40461 |
0,889 |
В pv- і Ts-координатах розраховані процеси мають такий вигляд:

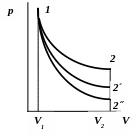
![]() -
ізотермічний процес;
-
ізотермічний процес;
![]() -
адіабатний процес;
-
адіабатний процес;
![]() - політропний процес.
- політропний процес.
Рис.1. Термодинамічні процеси в Ts- та pV - координатах
ПРИКЛАД 2. В циклі двигуна зі змішаним
підводом теплоти на початку стиску
р1=0,1 МПа і
температура t1=27
ºC. Степінь стиску
![]() =16;
степінь підвищення тиску
=16;
степінь підвищення тиску![]() =1,6;
степінь попереднього розширення
=1,6;
степінь попереднього розширення
![]() = 1,4. Визначити параметри робочого тіла
в характерних точках циклу, роботу
циклу, його термічний к.к.д. та зміну
ентропії окремих процесів циклу. За
робоче тіло прийняти повітря.
= 1,4. Визначити параметри робочого тіла
в характерних точках циклу, роботу
циклу, його термічний к.к.д. та зміну
ентропії окремих процесів циклу. За
робоче тіло прийняти повітря.
