
- •Теорія методу і опис установки.
- •Порядок| виконання роботи
- •Результати вимірювань і обчислень
- •Контрольні питання
- •Лабораторна робота №2 визначення теплоємності газів
- •Теоретична частина
- •Класифікація теплоємностей
- •Порядок|лад| виконання роботи
- •Результати вимірювань
- •Результати обчислення
- •Контрольні питання
- •Лабораторна робота №3 визначення параметрів водяної пари
- •Теоретична частина
- •Порядок|лад| виконання роботи
- •Результати вимірювань
- •Результати обчислення
- •Контрольні питання
- •Порядок|лад| виконання роботи
- •Результати вимірювань та обчислень
- •Контрольні питання
Лабораторна робота №1
ВИЗНАЧЕННЯ УНІВЕРСАЛЬНОЇ ГАЗОВОЇ СТАЛОЇ
МЕТОДОМ ВІДКАЧУВАННЯ
|Ціль роботи: визначити універсальну газову сталу.
Обладнання: вакуумний насос, мановакуумметр, барометр, термометр
скляна куля, ваги з важками.
Теоретична частина
Для вивчення фізичних властивостей макроскопічних систем, що складаються з великого числа часток, використовують два методи – статистичний і термодинамічний.
Статистичний метод заснований на законах теорії вірогідності і математичної статистики. Розділ теоретичної фізики, в якій вивчають фізичні властивості макроскопічних систем за допомогою статистичного методу, називається статистичною фізикою.
Термодинамічний метод полягає у вивченні фізичних властивостей макроскопічних систем шляхом аналізу умов і кількісних співвідношень для процесів перетворення енергії в даних системах. Відповідний розділ теоретичної фізики називається термодинамікою, а макроскопічна система в термодинаміці - термодинамічною системою.
Фізичні величини, що служать для характеристики стану термодинамічної системи, називають термодинамічними параметрами стану системи.
До них відносяться: об'єм, тиск, температура, концентрація і ін.
Тиск - фізична величина Р, чисельно рівна силі, що діє на одиницю площі поверхні тіла по напряму нормалі до цієї поверхні:
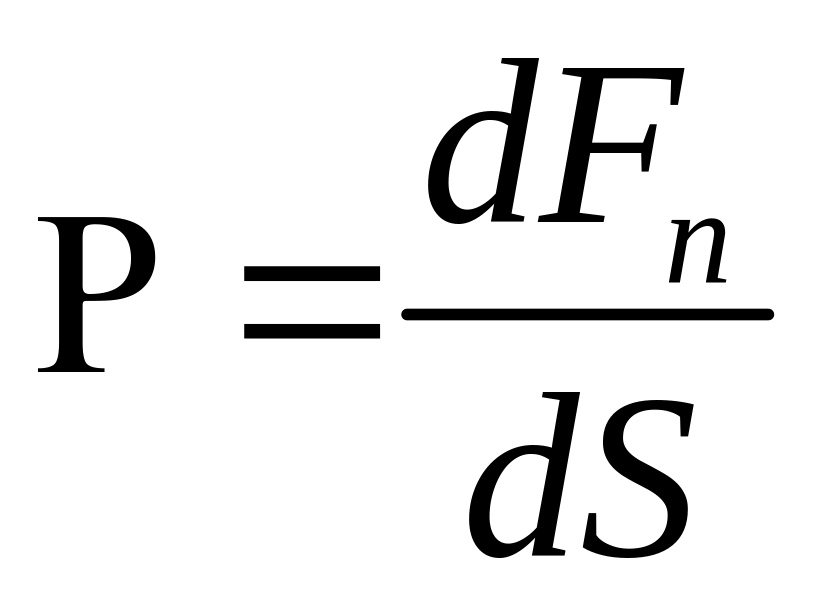 ,
,
де dFn – чисельне значення нормальної сили, що діє на малу ділянку поверхні тіла площею dS .
Складнішим і менш наочним являється параметр стану, званий температурою. Поняття температури має сенс лише для рівноважних станів системи. Під рівноважним станом розуміють такий стан системи, який не змінюється з часом, причому ця незмінність не пов'язана з протіканням якого-небудь процесу в зовнішньому середовищі. З молекулярно-кінетичної точки зору температура рівноважної системи характеризує інтенсивність теплового руху частинок|часток,часточок|.
Абсолютна температура є мірою середньої кінетичної енергії поступальної ходи молекул ідеального газу:
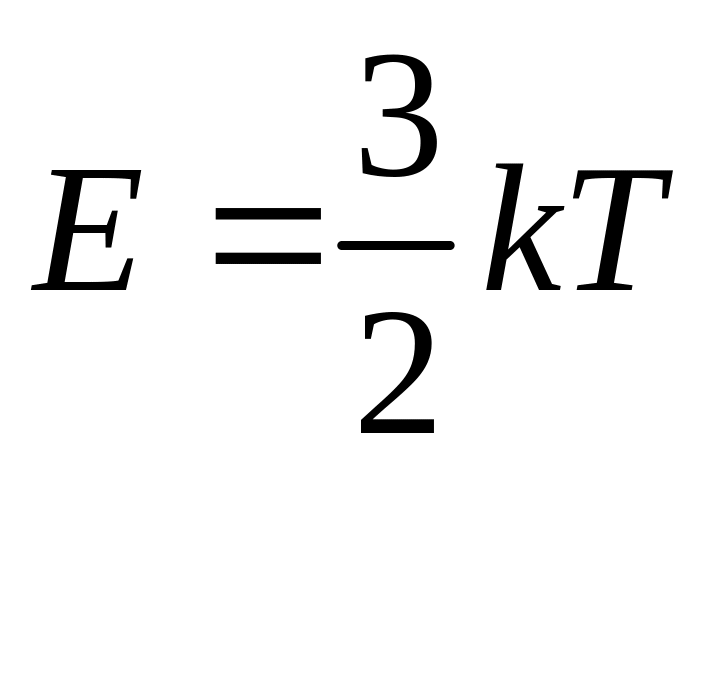
де k – постійна Больцмана.
Простим об'єктом досліджень в термодинаміці і статистичній фізиці являється ідеальний газ. Ідеальним газом називається газ, молекули якого мають малий власний об'єм яким можна нехтувати і не взаємодіють один із одним на відстані. Вважається, що при зіткненні молекули ідеального газу поводяться, як абсолютно пружні кульки.
На основі експериментів із досить розрідженими газами були встановлені прості закони, справедливі для ідеального газу.
1. Закон Бойля - Маріотта (для ізотермічного процесу).
![]() (1)
(1)
2. Закон Гей-Люссака (для ізохорного| процесу).
 (2)
(2)
3. Закон Гей-Люсса.ка (для ізобарного| процесу).
 (3)
(3)
За допомогою законів Бойля - Маріотта і Гей-Люссака легко знайти зв'язок між об'ємом, тиском і температурою для довільного рівноважного стану ідеального газу:
![]() (4)
(4)
де V0 – об'єм|обсяг| одного моля газу
R – універсальна газова стала, чисельно рівна роботі, що здійснюється одним молем газу при ізобарному нагріванні його на один градус.
Рівняння 4 називається рівнянням Менделєєва - Клапейрона. Для будь-якої маси газу воно запишеться у вигляді:
 (5)
(5)
де
![]() -
число
молей.
-
число
молей.
Моль – кількість речовини системи, в якій міститься стільки ж структурних елементів (молекул, атомів, іонів, електронів і ін. часток), скільки атомів міститься в 0,012 кг нукліда С (ізотопу вуглецю із атомною масою 12).
З даного визначення, очевидно, що молі різних газів, містять однакове число молекул, зване числом Авогадро
NA = 6,023×1023 молекул/моль
μ =m/v називається молярною масою газу. Маса моля, виражена в грамах, чисельно рівна відносній молекулярній масі.
Теорія методу і опис установки.
У даній роботі універсальна газова стала визначається методом відкачування.
Експериментальна установка складається з вакуумного насоса 5, мановакуумметра| 2, скляної кулі 4, з'єднаних між собою гумовими шлангами (рис.1).

Рис. 1.1. Схема установки для визначення універсальної газової сталої: 1,3- запірні крани, 2- мановаккууметр, 4- скляна куля, 5- вакуумний насос.
Мановакуумметри призначені для вимірювання надлишкового або вакуумметричного тиску рідин, газів і пари, що не діє агресивно на мідні сплави і сталь. У нашій установці даний прилад використовується як вакуумметр.
Рівняння Менделєєва-Клапейрона (5) для об'єму V при кімнатній температурі Т і атмосферному тиску Р1 для маси повітря М1 в кулі запишеться:
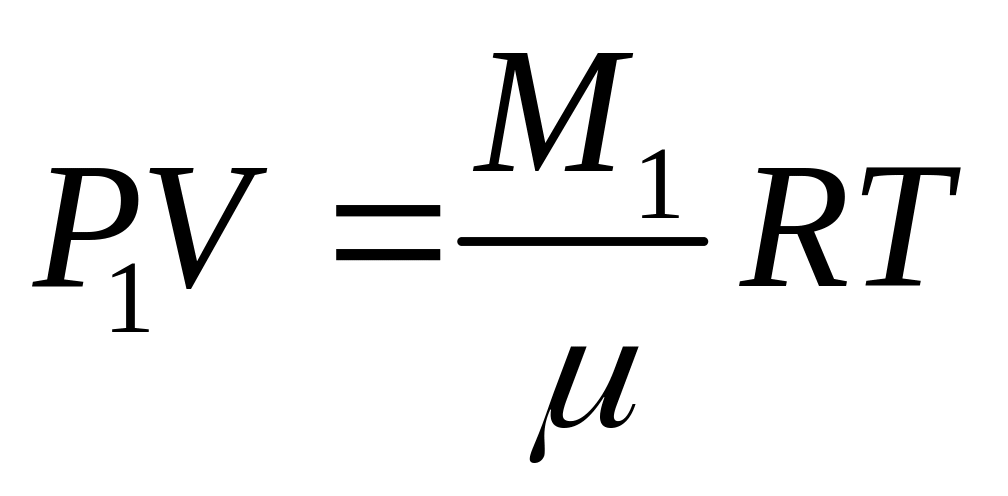 ,
,
де M1 = m1- m0', m0 - маса порожньої кулі; m1 - сумарна маса кулі і повітря в ньому при тиску P1.
Якщо відкачати насосом повітря із кулі, то тиск у ньому буде P2 (при тій же температурі Т). Рівняння 5 запишеться|занотується| так:
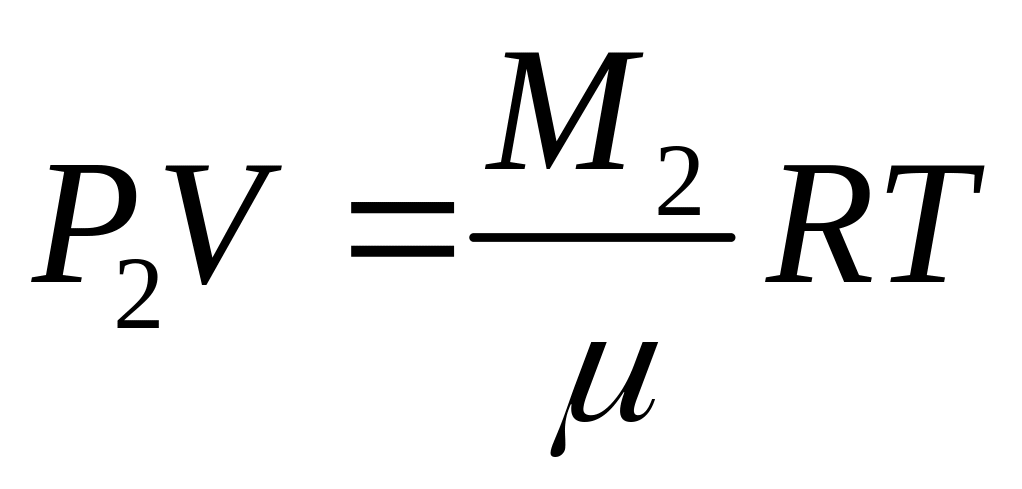 ,
,
де M2 = m2 – m0; m2 - сумарна маса кулі і повітря в ньому при тиску|тисненні| P2.
Із останніх рівнянь знайдемо універсальну газову сталу:
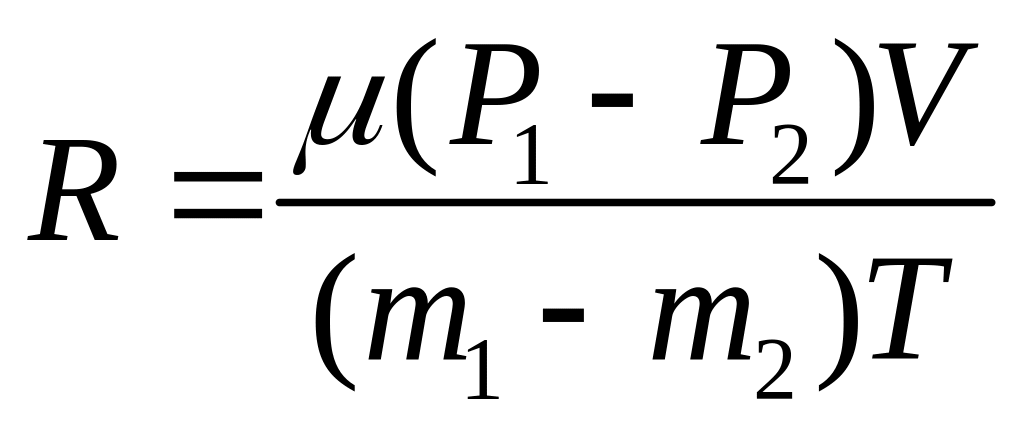
Порядок| виконання роботи
1. Акуратно зніміть зі штатива кулю, не виймаючи її із мішечка (мішечок надітий для безпеки!). При відкритому крані визначите на вагах сумарну масу m1 (кулі і повітря в ній до відкачування).
2. Закріпіть кулю на штативі, з'єднавши його за допомогою гумової трубки з мановакуумметром і насосом.
3. Викачайте повітря із кулі до тиску, вказаного викладачем. Закрийте кран 3 мановакуумметра (кран I завжди перекритий), а потім перекрійте затиском кулю.
4. Визначте на вагах сумарну масу m2 (кулі і повітря в ньому після відкачування).
5. Дослідження повторити 3 рази, змінюючи тиск відкачування Р, де Р=Р1 - Р2, тобто різниця тиску атмосферного Р1 і тиск в кулі після відкачування Р2.
6. Розрахуйте універсальну газову сталу R .
7. Результати вимірювань і обчислень занесіть в табл.1.1
Таблиця1.1
Результати вимірювань і обчислень
№ з/п|досліду| |
m1 |
m2 |
m1 - m2 |
Р |
R |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Контрольні питання
1. У чому суть і відмінність термодинамічного і статистичного методів дослідження фізичних явищ?
2. Який смисл вкладається в поняття "термодинамічний стан тіла"? Які параметри стану ви знаєте?
3. Який газ називається ідеальним?
4. Який фізичний смисл універсальної газової сталої? У яких одиницях вона вимірюється?
5. Виведіть рівняння Менделєєва - Клапейрона.
6. Що таке моль? Що таке число Авогадро?
7. Що таке відносна молекулярна маса?
8. Які прилади служать для вимірювання тиску рідин і газів? Чим відрізняється вакуумметр від манометра?
