
- •Введение
- •1 Теоретические основы процесса
- •2 Металлургический расчет с составлением материального и теплового балансов
- •2.1 Расчет рационального состава штейна
- •2.2 Расчет рационального состава кварцевого флюса
- •2.3 Расчет рационального состава конвертерного шлака
- •2.4 Расчет рационального состава холодных материалов
- •2.5 Расчет первого периода конвертирования
- •2.6 Расчет второго периода конвертирования
- •2.7 Расчет теплового баланса I периода конвертирования
- •2.8 Расчет теплового баланса II периода конвертирования
- •2.9 Расчет времени операции конвертирования
- •3 Расчет и выбор оборудования
- •3.1 Расчет конвертера
- •3.2 Выбор конвертера
- •4 Мероприятия по охране труда
- •5 Охрана окружающей среды
- •6 Мероприятия по гражданской обороне
- •Приложение а
- •Приложение б
- •Список использованных источников
2.5 Расчет первого периода конвертирования
Определение количества конвертерного шлака (х) и кварцевого флюса (y).
Железа поступает в конвертер, кг:
с горячим штейном — 29,40 кг;
с холодными материалами — 7,22 кг;
с кварцевым флюсом — y × 0,05;
Всего: 36,62 + y × 0,05
Количество железа в х кг конвертерного шлака — 0,512 × х.
Поскольку железо при конвертировании практически полностью переходит в шлак, то справедливо равенство:
36,62 + y × 0,05 = 0,512 × х
Кремнезема поступает в конвертер, кг:
с кварцевым флюсом — 0,587 × y;
с холодными материалами — 2,86 кг;
Всего: 2,86 + 0,587 × y
Количество SiO2 в x кг конвертерного шлака — 0,27 × х.
Поскольку SiO2 полностью переходит в конвертерный шлак, то справедливо равенство:
2,86 + 0,587 × y = 0,27 × х
 Решая
систему уравнений, найдем x
и y:
Решая
систему уравнений, найдем x
и y:
 36,62
+ y × 0,05 =
0,512 × х
36,62
+ y × 0,05 =
0,512 × х
2,86 + 0,587 × y = 0,27 × х
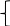 х
= 74,40 кг
х
= 74,40 кг
y = 29,36 кг
Количество FeS. Со штейном и холодными материалам поступает FeS:
34,73 + 28 ×0,0114 = 35,05 кг
С кварцевым флюсом поступает CuFeS2:
29,36 × 0,0259 = 0,76 кг
При его диссоциации образуется Cu2S, FeS, S:
2CuFeS2 → Cu2S + 2FeS + 0,5S2
368 – 160 – 176 – 32
0,76 – x – y – z
x = 0,33 кг
y = 0,36 кг
z = 0,07 кг
Всего вводится в процесс первого периода FeS:
35,05 + 0,36 = 35,41 кг
Часть FeS увлекается со шлаком:
74,40 × 0,0454 = 3,38 кг
Часть FeS расходуется за счет взаимодействия с оксидами:
1) FeS + Cu2O = FeO + Cu2S
88 – 144 – 72 – 160
x – 0,03 – y – z
x = 0,02 кг
y = 0,02 кг
z = 0,04 кг
2) FeS + 3Fe2O3 = 7FeO + SO2
88 – 144 – 72 – 160
x – 1,77 – y – z
x = 0,32 кг
y = 1,85 кг
z = 0,24 кг
 Всего
по указанным реакциям расходуется FeS:
0,02 + 0,32 = 0,34 кг
Всего
по указанным реакциям расходуется FeS:
0,02 + 0,32 = 0,34 кг
При этом образуется FeO: 0,02 + 1,85 = 1,87 кг
В результате потерь FeS со шлаком и реакциями взаимодействия с оксидами выводится FeS: 3,38 + 0,34 = 3,72 кг
Следовательно, необходимо подвергнуть окислению FeS: 35,41 – 3,72 = 31,69 кг
В этом количестве FeS содержится Fe и S:
FeS – Fe – S
88 – 56 – 32
31,69 – x – y
x = 20,17 кг
y = 11,53 кг
Окисление железа и серы.
В конвертерном шлаке содержится железа в форме Fe3O4: 74,40 × 0,1108 = 8,24 кг
В горячем штейне содержится железа в форме Fe3O4: 7,30 кг.
В холодных материалах содержится железа в форме Fe3O4: 28 × 0,1101 = 3,08 кг
Всего в процесс поступает железа в форме Fe3O4: 7,30 + 3,08 = 10,38 кг.
Окисляется Fe до Fe3O4: 10,38 – 8,24 = 2,14 кг
В конвертерном шлаке Fe в форме FeO: 74,40 × 0,3723 = 27,70 кг
С холодными материалами поступает железа в форме FeO: 28 × 0,1407 = 3,94 кг
В результате химических реакций образовалось FeO: 1,87 кг. В этом количестве содержится железа:
FeO – Fe
72 – 56
1,87 – x
x = 1,46 кг
Окисляется железа до FeO: 27,70 – 3,94 – 1,46 = 22,31 кг
Количество кислорода для окисления 2,14 кг железа до Fe3O4:
3Fe + 2O2 = Fe3O4
 168
– 64
168
– 64
2,14 – х1
х1 = 0,81 кг
Количество кислорода для окисления 22,31 кг железа до FeO:
2Fe + O2 = 2FeO
112 – 32
22,31 – x2
x2 = 6,37 кг
Количество цинка, перешедшего в конвертерный шлак из штейна и холодных материалов: 74,40 × 0,0114 = 0,85 кг
На окисление цинка потребуется кислорода:
2Zn + O2 = 2ZnO
130 – 32
0,85 – x3
x3 = 0,21 кг
Поступило цинка со штейном и 28 кг холодных материалов: 3,80 + 0,59 = 4,39 кг
Окислилось цинка: 4,39 – 0,85 = 3,54 кг
На окисление цинка требуется кислорода:
2Zn + O2 = 2ZnO
130 – 32
3,54 – x4
x4 = 0,87 кг
Как показано выше, необходимо окислить 31,69 кг FeS, в которых 11,53 кг серы. Кроме того, в CuFeS2 кварцевого флюса имеется 0,26 кг серы. Количество серы в 3,54 кг цинка, связанного в ZnS:
Zn – S
65 – 32
3,54 – x
x = 1,74 кг
Следовательно, всего окисляется серы: 11,53 + 0,26 + 1,74 = 13,53 кг
Отношение количества серы, окисляющейся до SO2 к количеству серы,
 окисляющейся
до SO3
составляет 6 : 1.
окисляющейся
до SO3
составляет 6 : 1.
Окисляется S
до SO2:
13,53 ×
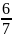 = 11,60 кг
= 11,60 кг
Окисляется S до SO3: 13,53 – 11,60 = 1,93 кг
На окисление S до SO2 требуется кислорода и образуется SO2:
S + O2 = SO2
32 – 32 – 64
11,60 – x5 – y1
x5 = 11,60 кг
y1 = 23,20 кг
С учетом протекающих химических реакций образуется SO2:
23,20 + 0,24 = 23,43 кг
На окисление S до SO3 требуется кислорода и образуется SO3:
S + 1,5O2 = SO3
32 – 48 – 80
1,93 – x6 – y2
x6 = 2,90 кг
y2 = 4,83 кг
Всего на окисление железа, цинка и серы требуется кислорода: x1 + x2 + x3 + x4 + x5 + x6 = 0,81 + 6,37 + 0,21 + 0,87 + 11,60 + 2,90 = 22,77кг
Количество кислорода в объёмных единицах определяется по формуле:
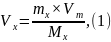
где Vx — объем искомого газа, м3;
mx — масса искомого газа, кг;
Vm — молярный объем газа, Vm = 22,4 м3/кмоль;
Mx — молярная масса искомого газа, кг/кмоль.

При использовании кислорода в ванне конвертера 95% практически требуется кислорода:
22,77 : 0,95 = 23,96 кг (16,78 м3)
Избыток кислорода составляет: 23,96 – 22,77 = 1,20 кг (0,84 м3)
 При
применении воздуха с 25% кислорода
количество дутья потребуется: 16,78 : 0,25
= 67,10 м3
При
применении воздуха с 25% кислорода
количество дутья потребуется: 16,78 : 0,25
= 67,10 м3
Обогащенное дутьё изготавливается из атмосферного воздуха (21%O2) и технологического кислорода (96,5%O2).
 Определение
количества атмосферного воздуха (x)
и технологического кислорода (y):
Определение
количества атмосферного воздуха (x)
и технологического кислорода (y):
x × 0,21 + y × 0,965 = 16,78
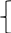 x
+ y = 67,10
x
+ y = 67,10
x = 63,55 м3
y = 3,56 м3
В атмосферном воздухе:
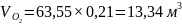

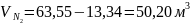

В технологическом кислороде содержится:


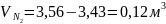

В составе газов I периода конвертирования будут пары воды и углекислый газ из флюсов (таблица 2):
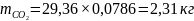
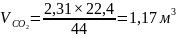
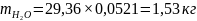

Состав газов I периода конвертирования приведен в таблице 5.
 Таблица
5 — Состав газов I
периода
Таблица
5 — Состав газов I
периода
Газы |
Масса, кг |
Объём, м3 |
%(об.) |
SO2 |
23,43 |
8,20 |
12,86 |
SO3 |
4,83 |
1,35 |
2,12 |
O2 |
1,20 |
0,84 |
1,31 |
N2 |
62,91 |
50,33 |
78,89 |
H2O |
1,53 |
1,90 |
2,98 |
CO2 |
2,31 |
1,17 |
1,84 |
Всего: |
96,21 |
63,80 |
100,00 |
Расчет количества белого матта.
В конвертер поступает медь:
1) с горячим штейном (30 кг);
2) с холодными материалами (4,82);
3) с кварцевым флюсом (0,29).
Всего меди: 30 + 4,82 + 0,29 = 35,11 кг
С конвертерным шлаком уходит меди: 74,40 × 0,018 = 1,34 кг
В белый матт переходит меди: 35,11 – 1,34 = 33,77 кг
Эта медь связывает серы в Cu2S:
2Cu – S
128 – 32
33,77 – x
x = 8,44 кг
При содержании меди в белом матте 76,0% количество белого матта составит: 33,77 : 0,76 = 44,43 кг
В нём прочих: 44,43 – 33,77 – 8,44 = 2,22 кг
Составление материального баланса I периода конвертирования.
Выход пыли составляет 3,5% от массы шихты:
(100 + 28 + 29,36) × 0,035 = 5,51 кг
Со штейном и холодными материалами поступило цинка:
3,80 + 0,59 = 4,39 кг
В шлак уходит цинка 1,14 кг. Следовательно, в пыли содержится цинка: 4,39 – 1,14 = 3,25 кг
Цинк находится в форме ZnO, а значит, связывает кислорода:
ZnO
65 – 16
3,25 – x
 x
= 0,80 кг
x
= 0,80 кг
Прочих в пыли: 5,51 – 3,25 – 0,80 = 1,46 кг
Уточнение состава конвертерного шлака производится по разности между массой компонентов в приходе и массой компонентов в белом матте, газе и пыли.
Материальный баланс I периода приведен в таблице 6.
Таблица 6 — Материальный баланс I периода конвертирования
Материал |
∑ |
Cu |
Zn |
Fe |
S |
SiO2 |
CaO |
Al2O3 |
O |
N |
H2O |
CO2 |
прочие |
ПОСТУПИЛО |
|||||||||||||
Штейн горячий |
100,00 |
30,00 |
3,80 |
29,40 |
22,00 |
— |
— |
— |
2,78 |
— |
— |
— |
12,02 |
Холодные материалы |
28,00 |
4,82 |
0,59 |
7,22 |
1,01 |
2,86 |
0,67 |
0,90 |
2,30 |
— |
— |
— |
7,64 |
Кварцевый флюс |
29,36 |
0,29 |
— |
1,47 |
0,26 |
17,23 |
2,94 |
2,64 |
0,53 |
— |
1,53 |
2,31 |
0,15 |
Воздух |
81,82 |
— |
— |
— |
— |
— |
— |
— |
19,06 |
62,75 |
— |
— |
— |
Технологический кислород |
5,06 |
— |
— |
— |
— |
— |
— |
— |
4,90 |
0,16 |
— |
— |
— |
Всего |
100,00 |
30,00 |
3,80 |
29,40 |
22,00 |
— |
— |
— |
2,78 |
— |
— |
— |
12,02 |
ПОЛУЧЕНО |
|||||||||||||
Белый матт |
44,43 |
33,77 |
— |
— |
8,44 |
— |
— |
— |
— |
— |
— |
— |
2,22 |
Шлак конвертерный |
98,08 |
1,34 |
1,14 |
38,09 |
1,18 |
20,09 |
3,61 |
3,54 |
12,96 |
— |
— |
— |
16,13 |
Газы: |
|
||||||||||||
SO2 |
23,43 |
— |
— |
— |
11,72 |
— |
— |
— |
11,72 |
— |
— |
— |
— |
SO3 |
4,83 |
— |
— |
— |
1,93 |
— |
— |
— |
2,90 |
— |
— |
— |
— |
O2 |
1,20 |
— |
— |
— |
— |
— |
— |
— |
1,20 |
— |
— |
— |
— |
N2 |
62,91 |
— |
— |
— |
— |
— |
— |
— |
— |
62,91 |
— |
— |
— |
H2O |
1,53 |
— |
— |
— |
— |
— |
— |
— |
— |
— |
1,53 |
|
— |
CO2 |
2,31 |
— |
— |
— |
— |
— |
— |
— |
— |
— |
|
2,31 |
— |
Всего газов |
96,21 |
— |
— |
— |
13,65 |
— |
— |
— |
15,81 |
62,91 |
1,53 |
2,31 |
— |
Пыль |
5,51 |
|
3,25 |
— |
— |
— |
— |
— |
0,80 |
— |
— |
— |
1,46 |
Всего |
244,23 |
35,11 |
4,39 |
38,09 |
23,27 |
20,09 |
3,61 |
3,54 |
29,58 |
62,91 |
1,53 |
2,31 |
19,81 |
