
Российский Химико-Технологический Университет
им. Д.И. Менделеева
Кафедра технологии основного органического и нефтехимического синтеза
Реакция Виттига
Выполнил: Филатов И.Е.
Гр. П-32
Проверил: Сапунов В.Н.
Москва 2014
Содержание
Введение. |
3 |
История открытия |
3 |
Механизм реакции |
5 |
Модификации метода |
6 |
Промышленное использование |
8 |
Литература. |
12 |
Введение.
Реакция Виттига — химическая реакция альдегидов или кетонов с илидами фосфора (которые иногда называют «реагентами Виттига»), которая приводит к образованию алкенов или алленов и оксида трифенилфосфина.

Реакция была открыта в 1954 году Георгом Виттигом. За открытие этой реакции он был награжден Нобелевской премией в области химии в 1979 году.
Реакции Виттига широко используется в органическом синтезе для получения алкенов.
История открытия.
В 1940-х гг. немецкий ученый Георг Виттиг в своих работах исследовал способы получения соединений, в молекулах которых органические группы соединялись ковалентной связью с элементами V группы периодической таблицы, такими, как азот, фосфор и мышьяк. Теоретически это считалось возможным, однако синтезировать их еще никому не удавалось. Г.Виттиг и его коллеги в основном эту задачу решили, но они не смогли синтезировать соединения, молекулы которого содержали пятивалентный азот. Однако главным достижением в исследованиях Виттига в области синтеза пентаарилпроизводных элементов V группы принято считать открытие карбонилолефина (1953), который в дальнейшем сыграет значительную роль во многих важных промышленных процессах. Это случайно сделанное открытие, известное в настоящее время как реакция Виттига, имело большее научное значение, чем решение первоначально поставленной задачи – синтез пентафенилфосфора.
В 1945 г. Виттиг для получения пентаарилпроизводных V группы периодической системы использовал илиды*. В илидах четвертичная соль элемента V группы, содержащая четыре органические группы и присоединенный галоген, вместо того, чтобы приобрести пятую органическую группу при действии, например фениллития, согласно его исследованиям, теряла протон из одной органической группы:
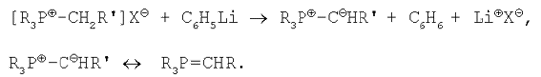
Столь необычный механизм течения реакции не был признан научным сообществом, и на его доказательство ученому потребовалось восемь лет. Только в 1953 г. ему удалось представить наглядные и убедительные факты, которые подтверждали такое направление течения вышеуказанной реакции и наличие в последней стадии перегруппировки. В дальнейшем эту реакцию назовут его именем.
Рассказывая об этом открытии Виттига, конечно, необходимо упомянуть Германа Штаудингера и Карла С.Марвела, которые уже в 1920-е гг. независимо друг от друга осуществили значительную подготовительную работу в этой области. По сути дела, Штаудингер описал первый фосфорный илид еще в 1919 г. Однако большая часть их работы не была в то время опубликована и вряд ли оказала влияние на проведенные Виттигом исследования.
Причину своего успеха Виттиг, как это ни покажется странным, объяснял ограниченностью своих знаний о работах предшественников по этой теме. И действительно, если бы Виттиг знал о результатах, достигнутых Марвелом, он ограничился бы получением соединений, содержащих пятивалентный фосфор, и новая химическая реакция (реакция Виттига) не была бы открыта. По иронии судьбы в начале 1940-х гг. Штаудингер и Виттиг были коллегами по Фрейбургскому университету. Но к этому времени Штаудингер уже прекратил исследования производных фосфора и не мог дать Виттигу никакой новой информации в этой области исследований.
В 1953 г. Виттиг при изучении открытых и синтезированных им илидов обнаружил, что последние свободно вступают в реакцию с карбонильными соединениями (альдегидами и кетонами, молекулы которых содержат углерод-кислородную двойную связь). В результате этой реакции образуется олефин с новой углерод-углеродной двойной связью вместо карбонильной группы. Ниже представлена схема синтеза на примере реакции трифенилфосфинметилена(I) с ацетоном(II). На промежуточной стадии реакции образуется биполярное соединение (IIIa), соответствующее переходному состоянию (IIIб); при нагревании (IIIа) распадается на трифенилфосфиноксид (IV) и олефин (V).
Схема синтеза олефинов (реакция Виттига)
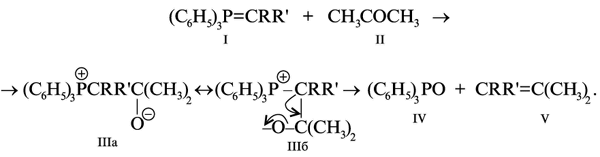
По-видимому, в реакции Виттига сначала образуется связь между электроотрицательным углеродным атомом трифенилфосфинметилена (I) и электроположительным углеродным атомом карбонильной группы ацетона (II). В образующемся биполярном промежуточном соединении (IIIа) существуют благоприятные условия для атаки отрицательно заряженного атома кислорода на положительно заряженный атом фосфора с одновременным разрывом связей фосфор–углерод и углерод–кислород, которое происходит в переходном состоянии четырехцентрового типа (IIIб).
Реакция Виттига в отношении асимметрического атома фосфора оказалась стереоспецифичной, т. к. в дальнейшем было найдено, что оптически активная фосфониевая соль (IIIб) дает оптически активный фосфиноксид (IV). В соответствии с представленным механизмом реакция должна сопровождаться сохранением пространственной конфигурации, что подтвердили экспериментальные исследования.
