
- •Конкретные задачи
- •Вопросы для самоподготовки
- •Этапы занятия и контроль усвоения знаний
- •Основные направления реакционной способности углеводородов в зависимости от их электронного строения
- •Ковалентная связь
- •Циклоалканы
- •Циклопропан с3н6
- •Транс-1,4-диметилциклогексан цис-1,4-диметилциклогексан
- •1. Гидрирование:
- •Пропен пропан
- •2. Галогенирование:
- •3. Гидрогалогенирование:
- •6. Полимеризация:
- •Алкадиены Это углеводороды, содержащие две двойные связи. Общая формула Сn h2n-2.
- •1. Гидрирование:
- •2. Гидрогалогенирование:
- •Ароматические углеводороды (арены)
- •Химические свойства
- •1. Галогенирование:
- •2. Нитрование:
- •3.Сульфирование:
- •4. Алкилирование:
- •Тема 2. Спирты. Фенолы. Нафтолы. Тиолы
- •Вопросы для самоподготовки
- •Этапы занятия и контроль усвоения знаний
- •Кислотность и основность органических соединений
- •Кислоты тон
- •Одноатомные спирты
- •Дегидрирование альдегид
- •Дегидрирование кетон
- •Многоатомные спирты
- •Спирты высшей атомности
- •Свойства фенолов как ароматических соединений. Реакции электрофильного замещения
- •Нафтолы
- •Ароматические спирты
- •Тема 3. Альдегиды и кетоны
- •Пиридоксаль пиридоксальфосфат
- •Этапы занятия и контроль усвоения знаний
- •I. Реакции нуклеофильного присоединения
- •4. Взаимодействие с галогенсодержащими реагентами
- •II. Реакции за счет -сн2-звена
- •Галогенирование:
- •III. Реакции, характерные только для альдегидов
- •Тема 4. Карбоновые кислоты и их функциональные производные
- •Конкретные задачи
- •Вопросы для самоподготовки
- •Этановая кислота 2-метилпропановая бутен-3-овая кислота
- •Малеиновая фумаровая кислота
- •Линолевая кислота
- •2. Реакции нуклеофильного замещения (sn ):
- •Двухосновные карбоновые кислоты
- •Трехосновные кислоты
- •Ноос–сн2–с–сн2–соон лимонная 3-гидрокси – 3-карбокси -
- •Специфические реакции двухосновных кислот
- •Тема 5. Липиды
- •Конкретные задачи
- •Вопросы для самоподготовки
- •Этапы занятия и контроль усвоения знаний
- •Омыляемые липиды
- •Омыляемые липиды
- •Жирные кислоты
- •Простые омыляемые липиды
- •Сложные омыляемые липиды
- •Ф осфолипиды
- •Глицерофосфо- сфингофосфо-
- •Гликолипиды
- •Цереброзиды ганглиозиды
- •Цереброзиды
- •Ганглиозиды
- •Неомыляемые липиды
- •Стероиды
- •Классификация стероидов
- •Эстрадиол
- •Тема 6. Соединения со смешанными функциями
- •Конкретные задачи
- •Вопросы для самоподготовки
- •Этапы занятия и контроль усвоения знаний
- •Содержание этапов занятия
- •Оксокислоты
- •2. Кето-енольная таутомерия -оксокислот.
- •Оксокислоты
- •Стереоизомерия
- •(Оптические,
- •Энантиомеры
- •Тема 7. Аминокислоты.
- •III. Биологически важные реакции - аминокислот
- •Тема 8. Углеводы
- •Вопросы для самоподготовки
- •Этапы занятия и контроль усвоения знаний
- •Тема 8-1. Углеводы. Моносахариды Теория
- •Стереоизомерия моносахаридов
- •Важнейшие природные моносахариды а льдопентозы
- •Альдогексозы Кетогексоза
- •Цикло-цепные таутомеры моносахаридов
- •Перспективные формулы Хеуорса
- •Цикло-цепная таутомерия моносахаридов – это существование в водном растворе смеси таутомерных форм, способных превращаться друг в друга через открытую таутомерную форму:
- •3. Мутаротация сахаров При растворении кристаллической таутомерной формы углевода в воде наблюдается явление мутаротации.
- •4. Конформации моносахаридов
- •5. Эпимеризация
- •6. Химические свойства моносахаридов
- •Реакции, характерные для цепной формы углеводов
- •Кислоты
- •Реакции циклических таутомерных форм моносахаридов
- •Тема 8-2. Ди – и полисахариды
- •Дисахариды
- •Цикло-цепная таутомерия дисахаридов
- •Реакция «серебряного зеркала»:
- •Полисахариды
- •Тема 9. Гетероциклические соединения
- •Конкретные задачи
- •Вопросы для самоподготовки
- •Этапы занятий и контроль усвоения знаний
- •Содержание этапов занятия
- •Электронное строение «пиррольного» атома азота
- •Шестичленные гетероциклические системы с одним гетероатомом
- •Электронное строение «пиридинового» атома азота
- •Химические свойства
- •Пятичленные гетероциклы с двумя гетероатомами
- •Химические свойства
- •Шестичленные гетероциклические соединения с двумя гетероатомами п иримидин
- •Производные пиримидина
- •Полициклические гетероциклы
- •Триптофан
- •Хинолин и изохинолин
- •Нуклеиновые кислоты
- •Общая схема построения нуклеиновых кислот
- •Нуклеиновые кислоты
- •Нуклеотиды
- •Методические разработки по биоорганической химии
- •Методические разработки по биоорганической химии Санкт-Петербург
6. Полимеризация:
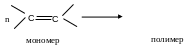
( С С ) n
![]()
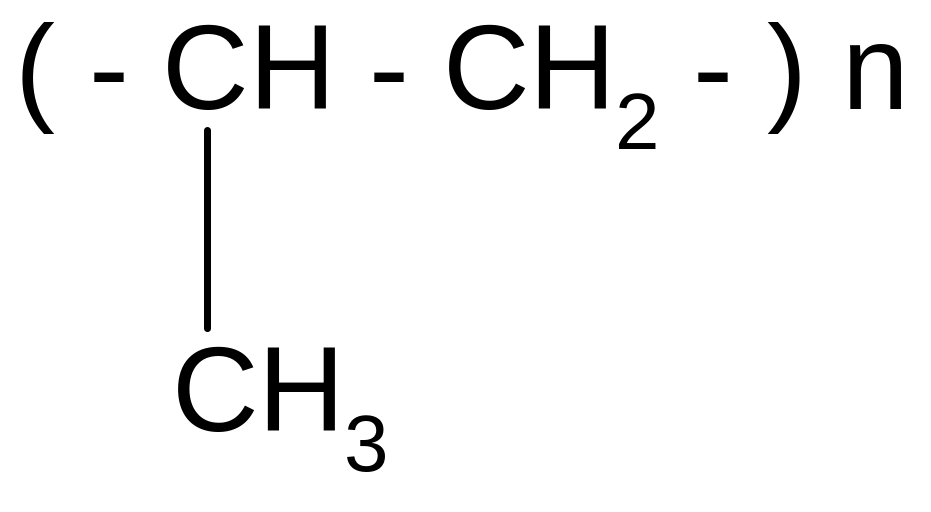
пропилен полипропилен
Алкадиены Это углеводороды, содержащие две двойные связи. Общая формула Сn h2n-2.
Наибольший интерес представляют сопряженные алкадиены – соединения с чередующимися двойными и одинарными связями.
Название |
Структурная формула |
Брутто– формула |
Бутадиен (дивинил) 2–Метилбутадиен–1,3 (изопрен) |
СН2 = СН – СН = СН2 СН2 = С– СН=СН2 СН3 |
С4Н6 С5Н8 |
Сопряженные алкадиены имеют специфическое электронное строение. Все 4 атома углерода находятся в sp2 – гибридизации, а следовательно, - остов молекулы, образованный sp2 – гибридизованными орбиталями лежит в одной плоскости.

Негибридизованные - орбитали каждого атома углерода перпендикулярны плоскости - остова и параллельны друг другу. При этом перекрывание происходит не только между 1 и 2, 3 и 4, но и между 2 и 3 -орбиталями. При этом происходит перераспределение (делокализация) электронной плотности по всей системе - связей, приводящее к образованию единого сопряженного электронного облака.
Химические свойства
Для алкадиенов наиболее характерны реакции АЕ, так же как и для алкенов, но проявляются особенности, связанные с сопряжением Присоединение 1 молекулы реагента возможно в разные положения: 1,2; 3,4 и 1,4.
1. Гидрирование:
1,2 – присоединение
 СН3–СН2–СН=СН2
СН3–СН2–СН=СН2
Кат.
СН2 = СН – СН = СН2 + Н2−
1,4 – присоединение
СН3–СН=СН-СН3
2. Гидрогалогенирование:
Сl
1,2 – присоединение СН3-С-СН=СН2


1 2 3 4 СН3
С Н2=С-СН
= СН2 + HСl
Сl
Н2=С-СН
= СН2 + HСl
Сl
3,4 – присоединение

 СН3
СН2=С-СН-СН3
СН3
СН2=С-СН-СН3
СН3
1,4- присоединение
 Н3С-С=СН-СН2-Сl
Н3С-С=СН-СН2-Сl
CH3
3. Полимеризация: идет аналогично присоединению:
CH3
1,2-

 СН2 – С
n
СН2 – С
n
CH=CH2
1 2 3 4
n СН2=С-СН=СН2 3,4-
CH-CH2 n
СН3
CH3-C =CH2
1,4-
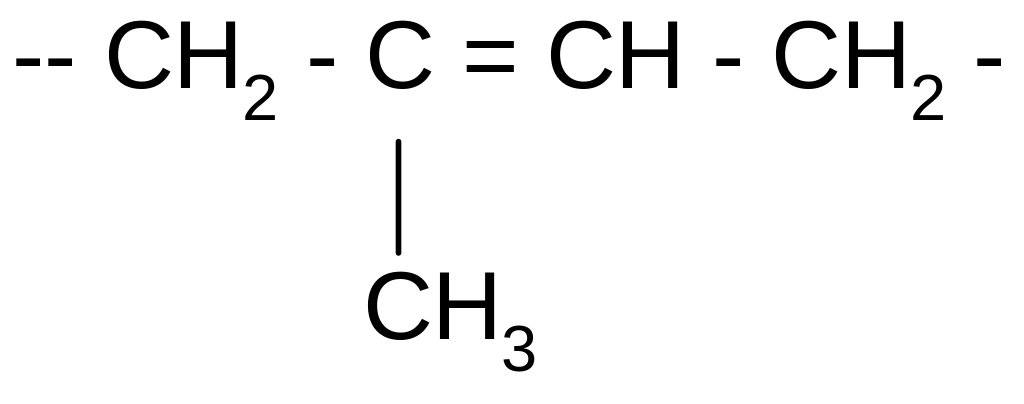 n
n
Кроме природного каучука, который, как известно, является 1,4-полимером изопрена, существует большая группа веществ (углеводородов и их производных), которые можно разделить на n скелетных фрагментов изопрена. Они называются терпенами.
