
- •Конкретные задачи
- •Вопросы для самоподготовки
- •Этапы занятия и контроль усвоения знаний
- •Основные направления реакционной способности углеводородов в зависимости от их электронного строения
- •Ковалентная связь
- •Циклоалканы
- •Циклопропан с3н6
- •Транс-1,4-диметилциклогексан цис-1,4-диметилциклогексан
- •1. Гидрирование:
- •Пропен пропан
- •2. Галогенирование:
- •3. Гидрогалогенирование:
- •6. Полимеризация:
- •Алкадиены Это углеводороды, содержащие две двойные связи. Общая формула Сn h2n-2.
- •1. Гидрирование:
- •2. Гидрогалогенирование:
- •Ароматические углеводороды (арены)
- •Химические свойства
- •1. Галогенирование:
- •2. Нитрование:
- •3.Сульфирование:
- •4. Алкилирование:
- •Тема 2. Спирты. Фенолы. Нафтолы. Тиолы
- •Вопросы для самоподготовки
- •Этапы занятия и контроль усвоения знаний
- •Кислотность и основность органических соединений
- •Кислоты тон
- •Одноатомные спирты
- •Дегидрирование альдегид
- •Дегидрирование кетон
- •Многоатомные спирты
- •Спирты высшей атомности
- •Свойства фенолов как ароматических соединений. Реакции электрофильного замещения
- •Нафтолы
- •Ароматические спирты
- •Тема 3. Альдегиды и кетоны
- •Пиридоксаль пиридоксальфосфат
- •Этапы занятия и контроль усвоения знаний
- •I. Реакции нуклеофильного присоединения
- •4. Взаимодействие с галогенсодержащими реагентами
- •II. Реакции за счет -сн2-звена
- •Галогенирование:
- •III. Реакции, характерные только для альдегидов
- •Тема 4. Карбоновые кислоты и их функциональные производные
- •Конкретные задачи
- •Вопросы для самоподготовки
- •Этановая кислота 2-метилпропановая бутен-3-овая кислота
- •Малеиновая фумаровая кислота
- •Линолевая кислота
- •2. Реакции нуклеофильного замещения (sn ):
- •Двухосновные карбоновые кислоты
- •Трехосновные кислоты
- •Ноос–сн2–с–сн2–соон лимонная 3-гидрокси – 3-карбокси -
- •Специфические реакции двухосновных кислот
- •Тема 5. Липиды
- •Конкретные задачи
- •Вопросы для самоподготовки
- •Этапы занятия и контроль усвоения знаний
- •Омыляемые липиды
- •Омыляемые липиды
- •Жирные кислоты
- •Простые омыляемые липиды
- •Сложные омыляемые липиды
- •Ф осфолипиды
- •Глицерофосфо- сфингофосфо-
- •Гликолипиды
- •Цереброзиды ганглиозиды
- •Цереброзиды
- •Ганглиозиды
- •Неомыляемые липиды
- •Стероиды
- •Классификация стероидов
- •Эстрадиол
- •Тема 6. Соединения со смешанными функциями
- •Конкретные задачи
- •Вопросы для самоподготовки
- •Этапы занятия и контроль усвоения знаний
- •Содержание этапов занятия
- •Оксокислоты
- •2. Кето-енольная таутомерия -оксокислот.
- •Оксокислоты
- •Стереоизомерия
- •(Оптические,
- •Энантиомеры
- •Тема 7. Аминокислоты.
- •III. Биологически важные реакции - аминокислот
- •Тема 8. Углеводы
- •Вопросы для самоподготовки
- •Этапы занятия и контроль усвоения знаний
- •Тема 8-1. Углеводы. Моносахариды Теория
- •Стереоизомерия моносахаридов
- •Важнейшие природные моносахариды а льдопентозы
- •Альдогексозы Кетогексоза
- •Цикло-цепные таутомеры моносахаридов
- •Перспективные формулы Хеуорса
- •Цикло-цепная таутомерия моносахаридов – это существование в водном растворе смеси таутомерных форм, способных превращаться друг в друга через открытую таутомерную форму:
- •3. Мутаротация сахаров При растворении кристаллической таутомерной формы углевода в воде наблюдается явление мутаротации.
- •4. Конформации моносахаридов
- •5. Эпимеризация
- •6. Химические свойства моносахаридов
- •Реакции, характерные для цепной формы углеводов
- •Кислоты
- •Реакции циклических таутомерных форм моносахаридов
- •Тема 8-2. Ди – и полисахариды
- •Дисахариды
- •Цикло-цепная таутомерия дисахаридов
- •Реакция «серебряного зеркала»:
- •Полисахариды
- •Тема 9. Гетероциклические соединения
- •Конкретные задачи
- •Вопросы для самоподготовки
- •Этапы занятий и контроль усвоения знаний
- •Содержание этапов занятия
- •Электронное строение «пиррольного» атома азота
- •Шестичленные гетероциклические системы с одним гетероатомом
- •Электронное строение «пиридинового» атома азота
- •Химические свойства
- •Пятичленные гетероциклы с двумя гетероатомами
- •Химические свойства
- •Шестичленные гетероциклические соединения с двумя гетероатомами п иримидин
- •Производные пиримидина
- •Полициклические гетероциклы
- •Триптофан
- •Хинолин и изохинолин
- •Нуклеиновые кислоты
- •Общая схема построения нуклеиновых кислот
- •Нуклеиновые кислоты
- •Нуклеотиды
- •Методические разработки по биоорганической химии
- •Методические разработки по биоорганической химии Санкт-Петербург
Тема 8-1. Углеводы. Моносахариды Теория
Углеводы широко распространены в природе. В организме животных на углеводы приходится до 2 %, а в растениях – до 90 % сухого вещества.
В зависимости от строения углеводы классифицируют на моно-, олиго- и полисахариды.
Моносахариды (монозы) – это многоатомные альдегидо- и кетоноспирты, не гидролизующиеся до более простых.
По числу атомов углерода моносахариды подразделяют на тетрозы (С4 ), пентозы (С5), гексозы (С6) и т.д.
Моносахариды, содержащие альдегидную группу, называют альдозами; кетонную – кетозами.
Стереоизомерия моносахаридов
Для представления пространственного строения моносахаридов Э. Фишер предложил использовать проекционные формулы.
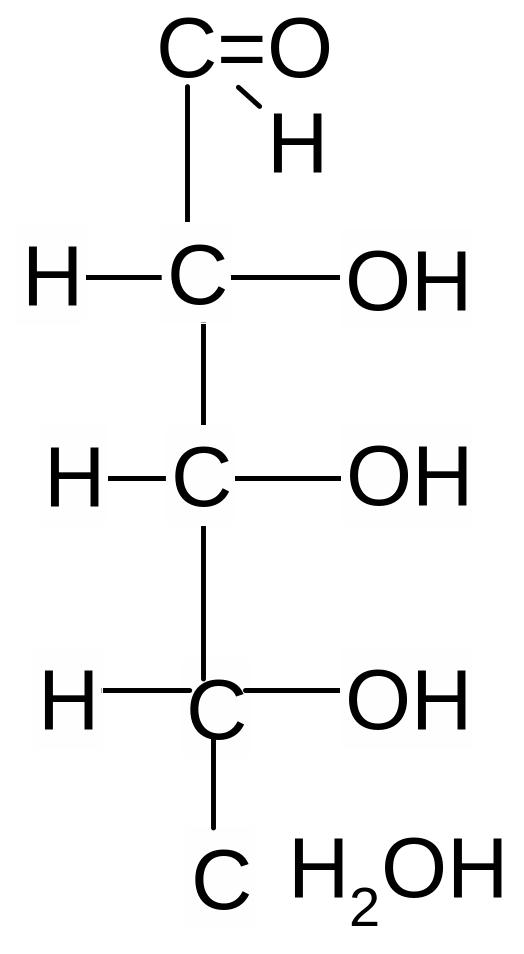
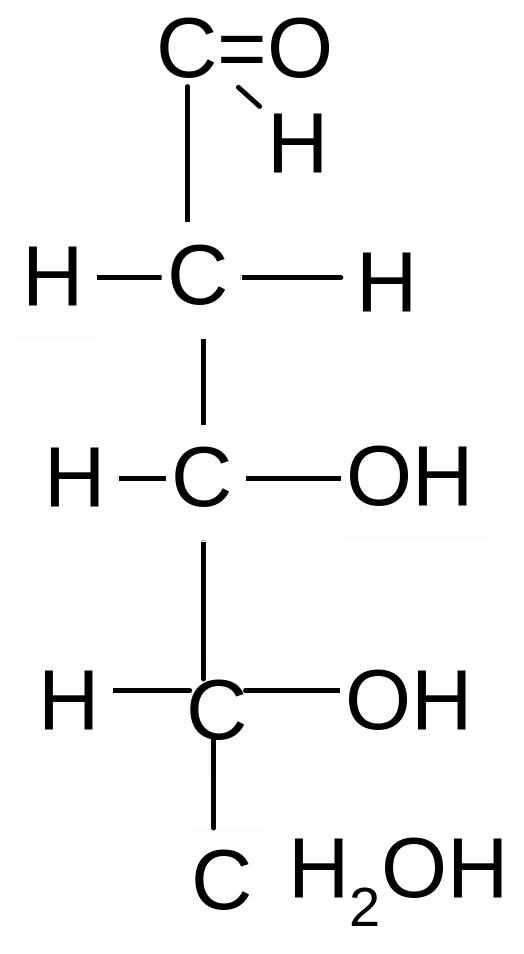
Важнейшие природные моносахариды а льдопентозы
*
*
*
D-рибоза 2–дезокси-D–рибоза D–ксилоза
Альдогексозы Кетогексоза

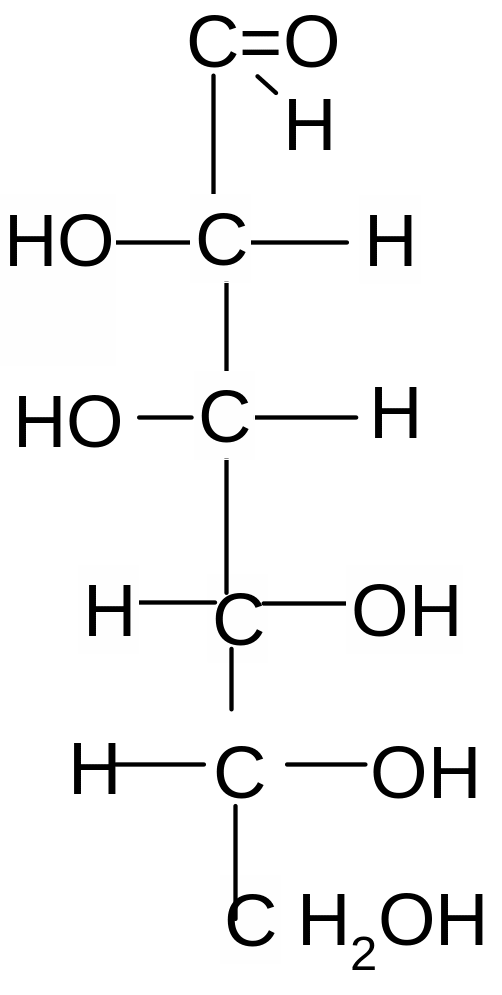
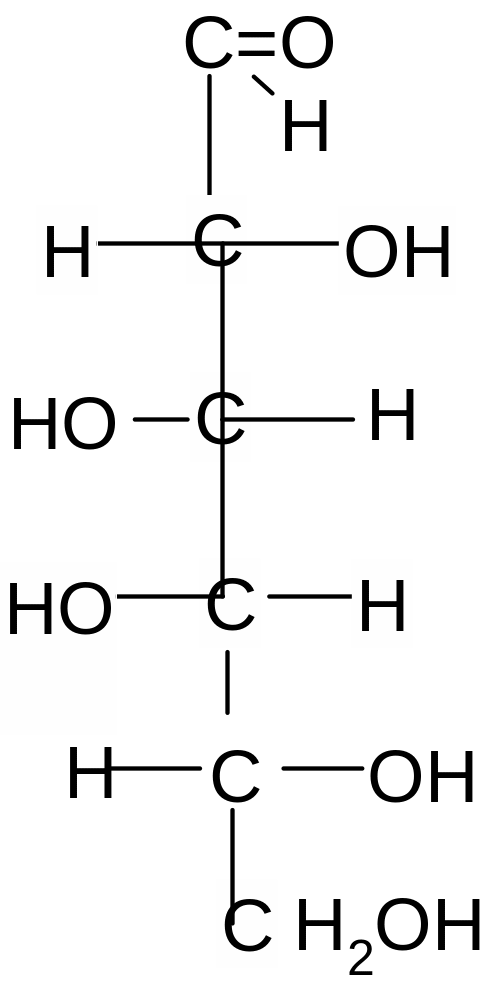
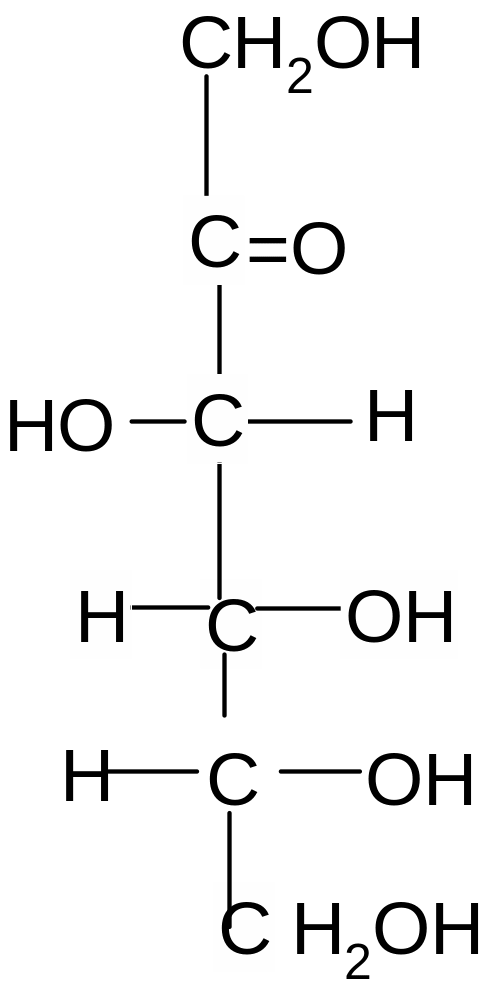
D- глюкоза D-манноза D-галактоза D-фруктоза
Кроме перечисленных выше пентоз и гексоз существуют и их пространственные изомеры, общее число которых вычисляется по формуле N=2n , где n – число асимметрических атомов углерода. Так, число возможных альдопентоз, стереоизомеров D-рибозы, составляет N=23 =8 , т.к. в этой молекуле 3 асимметрических атома углерода (см. формулу выше).
Например:
1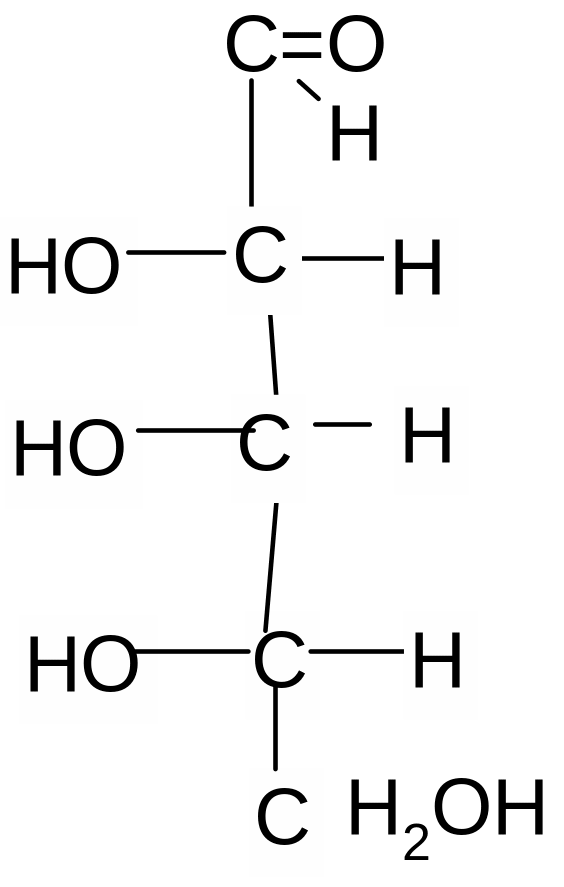
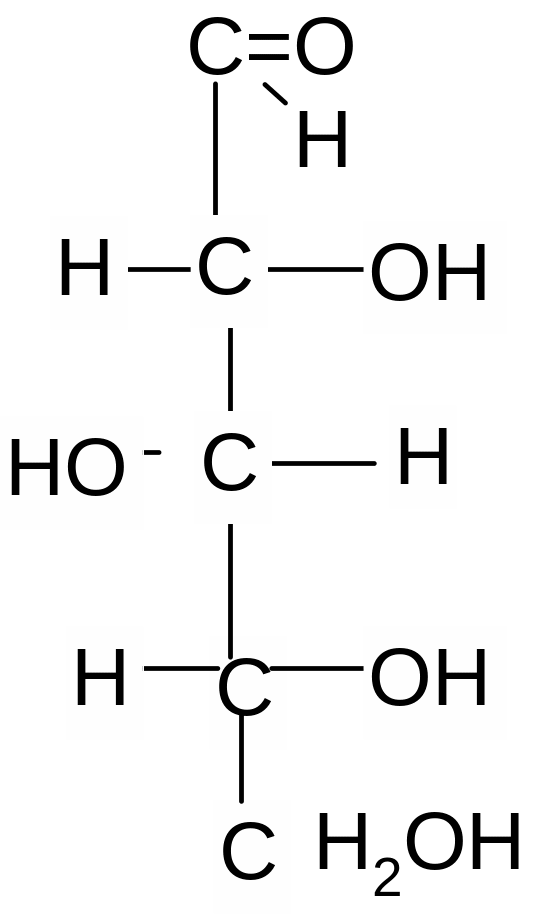
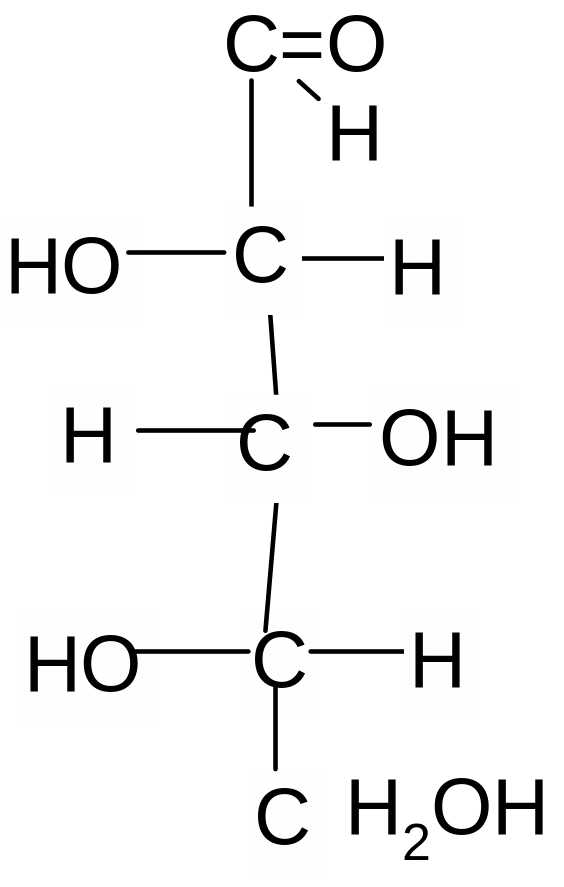 .
2. 3.
4.
.
2. 3.
4.
D-рибоза L-рибоза D-ксилоза L–ксилоза
1 и 2, 3 и 4 – это энантиомеры; 1 и 3; 1 и 4; 2 и 3; 2 и 4 – диастереомеры.
Напишите формулы недостающих стереоизомеров D–рибозы. Выделите среди них энантио - и диастереомеры.
В природе наиболее распространены углеводы D–ряда. Из природных моносахаридов L-ряда выделены: L-арабиноза (свекла), L-рамноза (растительные гликозиды), L-фукоза (пентозаны).
Принадлежность моносахарида к L- или D- ряду определяется по конфигурации его нижнего хирального атома углерода, конфигурация которого остается без изменения при переходе от эталона конфигурации - глицеринового альдегида с помощью оксинитрильного синтеза Килиани–Фишера.

Сравнивая конфигурацию нижнего хирального центра углевода с конфигурацией глицеринового альдегида, определяют стереохимический ряд: L- или D-.
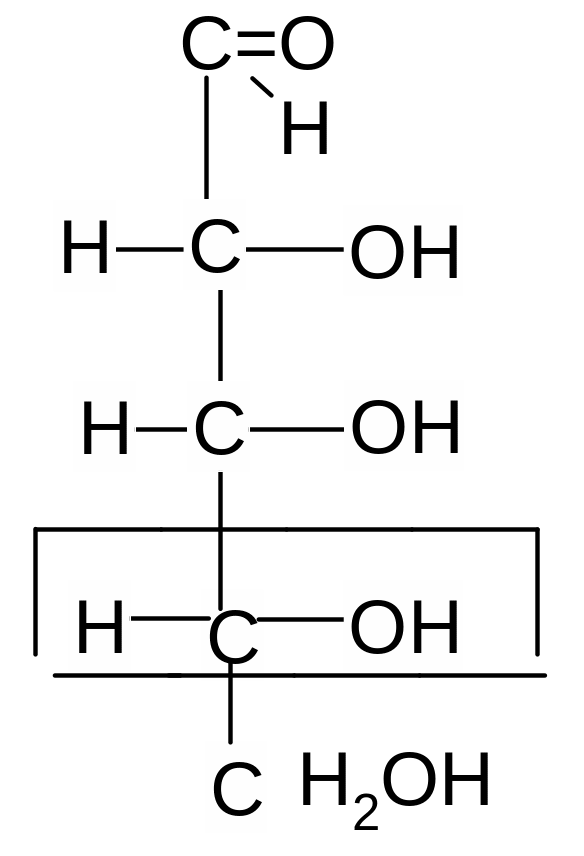
*
* *
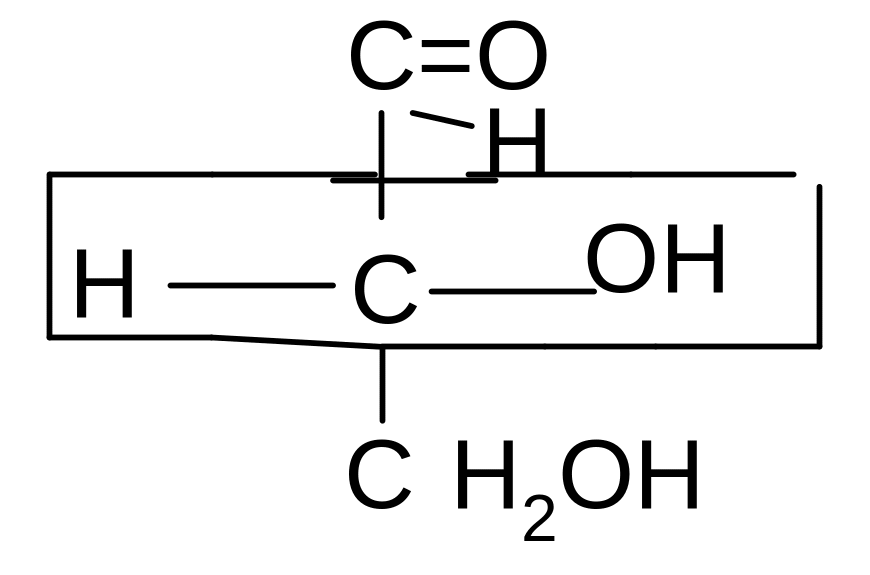
*
D-глицериновый D-рибоза
альдегид
Отнесите написанные вами стереоизомеры D–рибозы к D- или L– рядам.
