
- •Конкретные задачи
- •Вопросы для самоподготовки
- •Этапы занятия и контроль усвоения знаний
- •Основные направления реакционной способности углеводородов в зависимости от их электронного строения
- •Ковалентная связь
- •Циклоалканы
- •Циклопропан с3н6
- •Транс-1,4-диметилциклогексан цис-1,4-диметилциклогексан
- •1. Гидрирование:
- •Пропен пропан
- •2. Галогенирование:
- •3. Гидрогалогенирование:
- •6. Полимеризация:
- •Алкадиены Это углеводороды, содержащие две двойные связи. Общая формула Сn h2n-2.
- •1. Гидрирование:
- •2. Гидрогалогенирование:
- •Ароматические углеводороды (арены)
- •Химические свойства
- •1. Галогенирование:
- •2. Нитрование:
- •3.Сульфирование:
- •4. Алкилирование:
- •Тема 2. Спирты. Фенолы. Нафтолы. Тиолы
- •Вопросы для самоподготовки
- •Этапы занятия и контроль усвоения знаний
- •Кислотность и основность органических соединений
- •Кислоты тон
- •Одноатомные спирты
- •Дегидрирование альдегид
- •Дегидрирование кетон
- •Многоатомные спирты
- •Спирты высшей атомности
- •Свойства фенолов как ароматических соединений. Реакции электрофильного замещения
- •Нафтолы
- •Ароматические спирты
- •Тема 3. Альдегиды и кетоны
- •Пиридоксаль пиридоксальфосфат
- •Этапы занятия и контроль усвоения знаний
- •I. Реакции нуклеофильного присоединения
- •4. Взаимодействие с галогенсодержащими реагентами
- •II. Реакции за счет -сн2-звена
- •Галогенирование:
- •III. Реакции, характерные только для альдегидов
- •Тема 4. Карбоновые кислоты и их функциональные производные
- •Конкретные задачи
- •Вопросы для самоподготовки
- •Этановая кислота 2-метилпропановая бутен-3-овая кислота
- •Малеиновая фумаровая кислота
- •Линолевая кислота
- •2. Реакции нуклеофильного замещения (sn ):
- •Двухосновные карбоновые кислоты
- •Трехосновные кислоты
- •Ноос–сн2–с–сн2–соон лимонная 3-гидрокси – 3-карбокси -
- •Специфические реакции двухосновных кислот
- •Тема 5. Липиды
- •Конкретные задачи
- •Вопросы для самоподготовки
- •Этапы занятия и контроль усвоения знаний
- •Омыляемые липиды
- •Омыляемые липиды
- •Жирные кислоты
- •Простые омыляемые липиды
- •Сложные омыляемые липиды
- •Ф осфолипиды
- •Глицерофосфо- сфингофосфо-
- •Гликолипиды
- •Цереброзиды ганглиозиды
- •Цереброзиды
- •Ганглиозиды
- •Неомыляемые липиды
- •Стероиды
- •Классификация стероидов
- •Эстрадиол
- •Тема 6. Соединения со смешанными функциями
- •Конкретные задачи
- •Вопросы для самоподготовки
- •Этапы занятия и контроль усвоения знаний
- •Содержание этапов занятия
- •Оксокислоты
- •2. Кето-енольная таутомерия -оксокислот.
- •Оксокислоты
- •Стереоизомерия
- •(Оптические,
- •Энантиомеры
- •Тема 7. Аминокислоты.
- •III. Биологически важные реакции - аминокислот
- •Тема 8. Углеводы
- •Вопросы для самоподготовки
- •Этапы занятия и контроль усвоения знаний
- •Тема 8-1. Углеводы. Моносахариды Теория
- •Стереоизомерия моносахаридов
- •Важнейшие природные моносахариды а льдопентозы
- •Альдогексозы Кетогексоза
- •Цикло-цепные таутомеры моносахаридов
- •Перспективные формулы Хеуорса
- •Цикло-цепная таутомерия моносахаридов – это существование в водном растворе смеси таутомерных форм, способных превращаться друг в друга через открытую таутомерную форму:
- •3. Мутаротация сахаров При растворении кристаллической таутомерной формы углевода в воде наблюдается явление мутаротации.
- •4. Конформации моносахаридов
- •5. Эпимеризация
- •6. Химические свойства моносахаридов
- •Реакции, характерные для цепной формы углеводов
- •Кислоты
- •Реакции циклических таутомерных форм моносахаридов
- •Тема 8-2. Ди – и полисахариды
- •Дисахариды
- •Цикло-цепная таутомерия дисахаридов
- •Реакция «серебряного зеркала»:
- •Полисахариды
- •Тема 9. Гетероциклические соединения
- •Конкретные задачи
- •Вопросы для самоподготовки
- •Этапы занятий и контроль усвоения знаний
- •Содержание этапов занятия
- •Электронное строение «пиррольного» атома азота
- •Шестичленные гетероциклические системы с одним гетероатомом
- •Электронное строение «пиридинового» атома азота
- •Химические свойства
- •Пятичленные гетероциклы с двумя гетероатомами
- •Химические свойства
- •Шестичленные гетероциклические соединения с двумя гетероатомами п иримидин
- •Производные пиримидина
- •Полициклические гетероциклы
- •Триптофан
- •Хинолин и изохинолин
- •Нуклеиновые кислоты
- •Общая схема построения нуклеиновых кислот
- •Нуклеиновые кислоты
- •Нуклеотиды
- •Методические разработки по биоорганической химии
- •Методические разработки по биоорганической химии Санкт-Петербург
Стереоизомерия
Стереоизомеры отличаются друг от друга пространственным расположением атомов или групп атомов.
Стереоизомеры
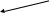

Энантиомеры Диастереомеры
(Оптические,
или зеркальные,
изомеры)
Знание стереоизомерии очень важно для изучения строения природных соединений (биорегуляторов и лекарственных средств – гормонов, витаминов, антибиотиков), так как все они существуют в строго определенных пространственных формах и их биологическая активность тесно связана с пространственным строением.
Так, для построения белковой молекулы используется один вид энантиомеров – L– аминокислоты, а в классе углеводов большее распространение имеют D–сахара. Из двух энантиомерных форм гормона адреналина большей фармакологической активностью обладает D(-)–форма. Стереоспецифично протекают многие биохимические реакции, так как они катализируются ферментами – белковыми молекулами.
Приведем некоторые примеры значения диастереомерии.
Так, бутендиовая кислота существует в виде двух геометрических изомеров (цис- и транс-), но только один из них – фумаровая кислота (транс–изомер) – служит субстратом для действия фермента.
Ретинол с транс–расположением всех двойных связей более эффективен в процессах зрения, чем его цис–изомер.
В липиды клеточных мембран в качестве структурных составляющих входят также только цис-формы высших жирных кислот.
Энантиомерия осуществляется у так называемых «хиральных» молекул. Хиральными, или асимметрическими, молекулами называются те, которые не могут быть совмещены со своим зеркальным отражением:



Термин «хиральность» произошел от греческого слова «хиро» – рука;
Самым простым наглядным примером хиральных объектов являются правая и левая руки.
Хиральность связана с отсутствием плоскости симметрии.
Атом углерод с четырьмя различными группами называется асимметрическим, или хиральным, центром.
Молекулы, содержащие такой центр (при отсутствии плоскости симметрии), являются хиральными.
Для изображения энантиомеров на плоскости используются проекционные формулы Фишера, называемые проекциями Фишера:
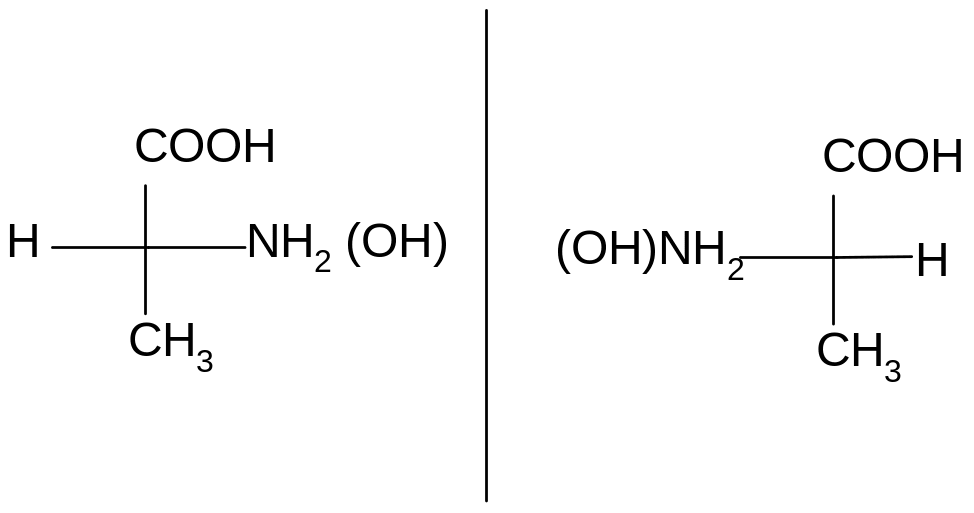
Энантиомеры
Относительная и абсолютная конфигурация. Определение абсолютной конфигурации стало возможным только с появлением современных физико-химических методов (рентгеноструктурного анализа) в 50-х годах. Однако нет необходимости устанавливать ее для каждого соединения. Можно охарактеризовать их путем сравнения конфигураций с абсолютной конфигурацией эталонных (ключевых) соединений, т. е. определить их относительную конфигурацию.
За такой эталон условно принят глицериновый альдегид, предложенный в 1906 г. Н.А. Розановым:
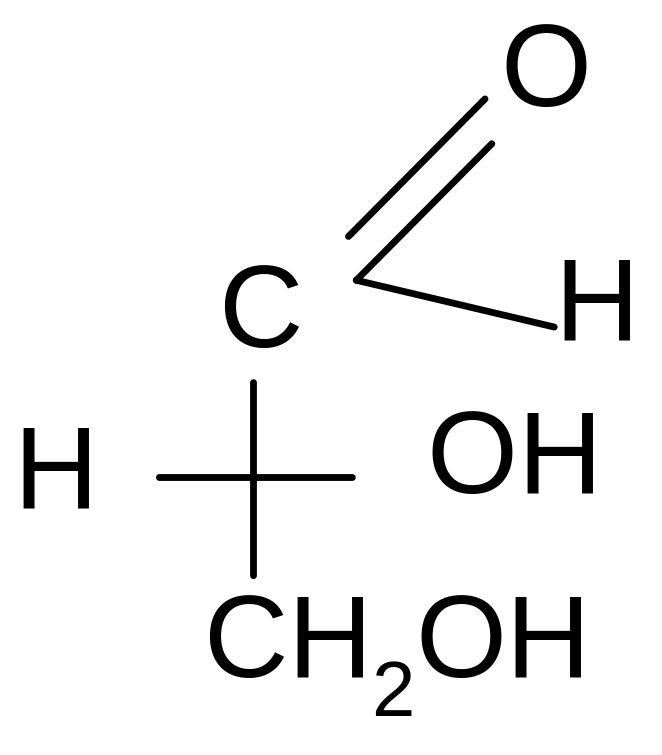
D- глицериновый L-глицериновый
альдегид альдегид
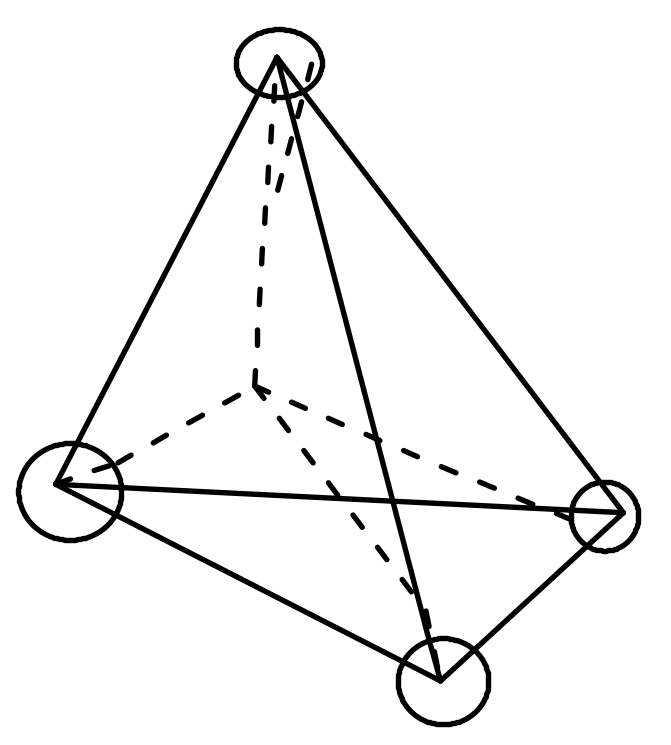
Считается, что все вещества, родственные глицериновому альдегиду по конфигурации хирального центра, т.е. с расположением групп – ОН, -NH2 , - Hal справа, относятся к D–ряду, слева – к L– ряду.
Например:

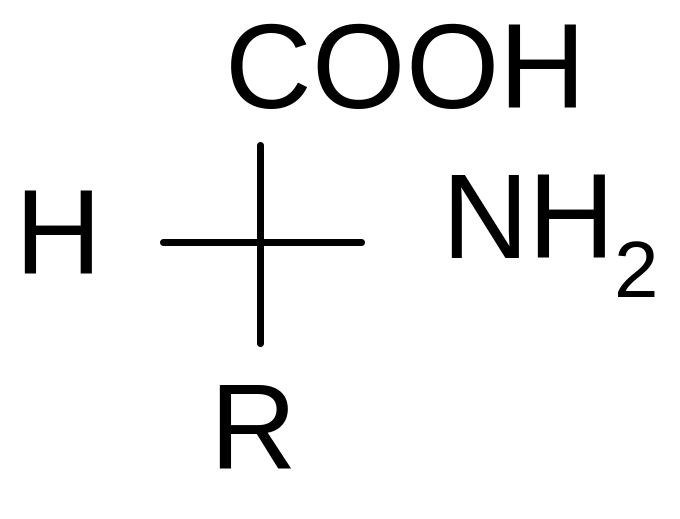
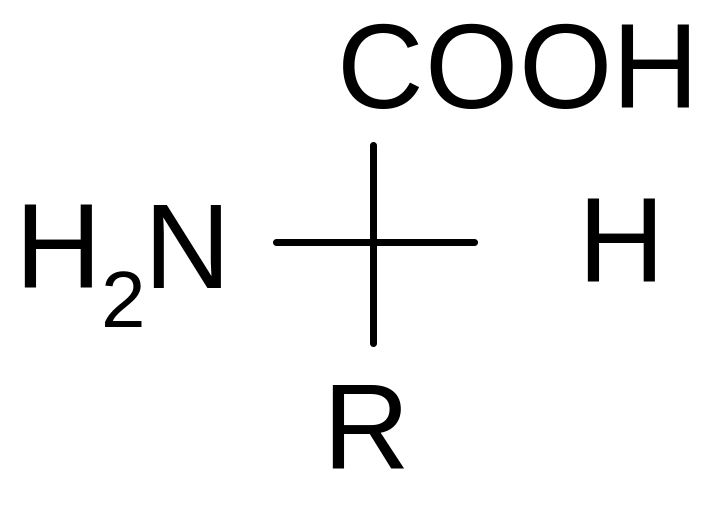
D - аминокислота L – аминокислота
Запомним, что D и L указывают на относительную конфигурацию молекулы. Познакомимся с некоторыми свойствами подобных молекул.
Хиральным соединениям свойственна способность вращать плоскость поляризованного света вправо (+) или влево (-), что называется оптической активностью. Отсюда и другое название энантиомеров – оптические изомеры.
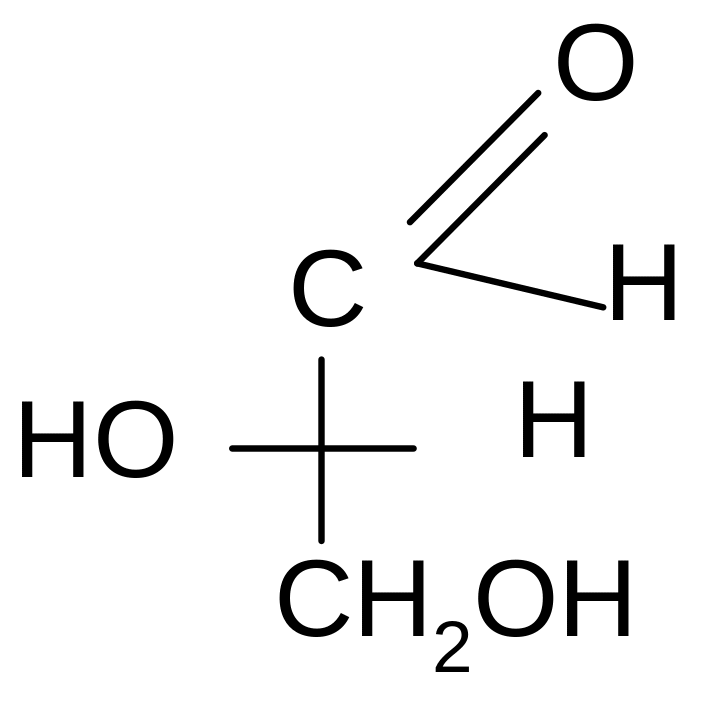
Мерой оптической активности является D -удельный угол вращения. Знак вращения (+) или (-) не связан с конфигурацией D и L и определяется только инструментально на приборе – поляриметре или сахариметре. Например,

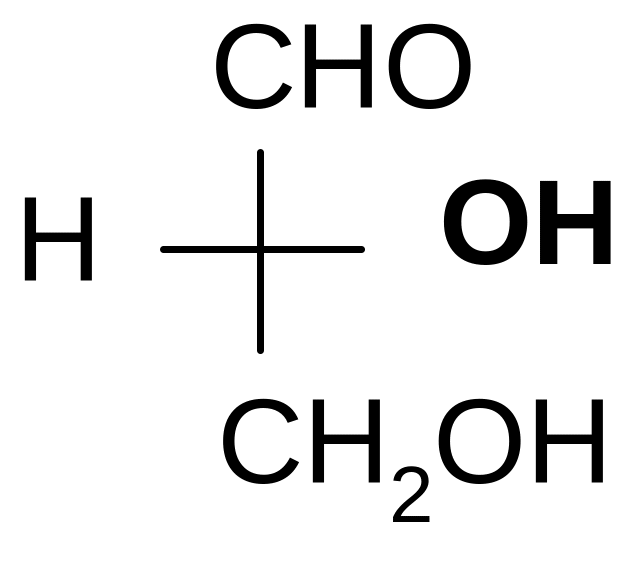
D(-) – молочная D(+)- глицериновый
кислота альдегид
Многие биологически важные вещества содержат в молекуле более одного центра хиральности. Подсчет числа стереоизомеров производится по формуле N= 2n, где n – число хиральных центров.
Представителем соединений с двумя центрами хиральности служит винная кислота. Рассмотрим этот пример подробнее.
У винной кислоты n=2, т.е. N= 22 = 4.

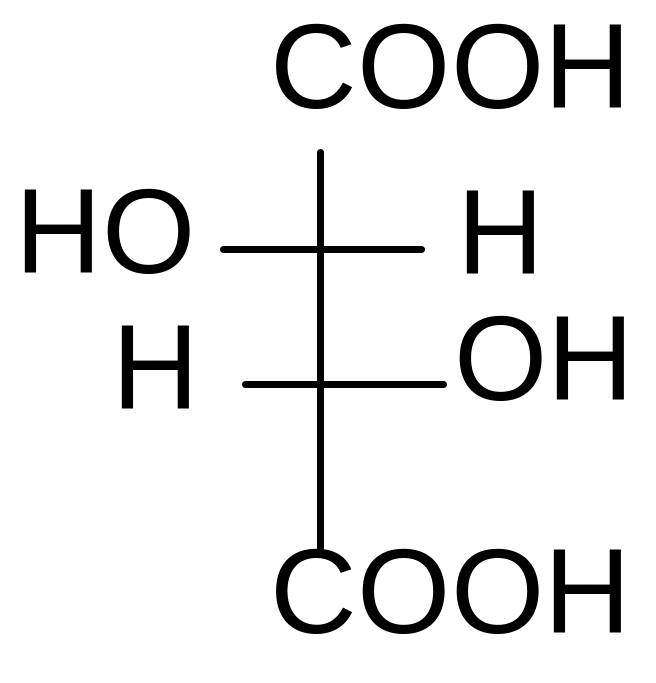
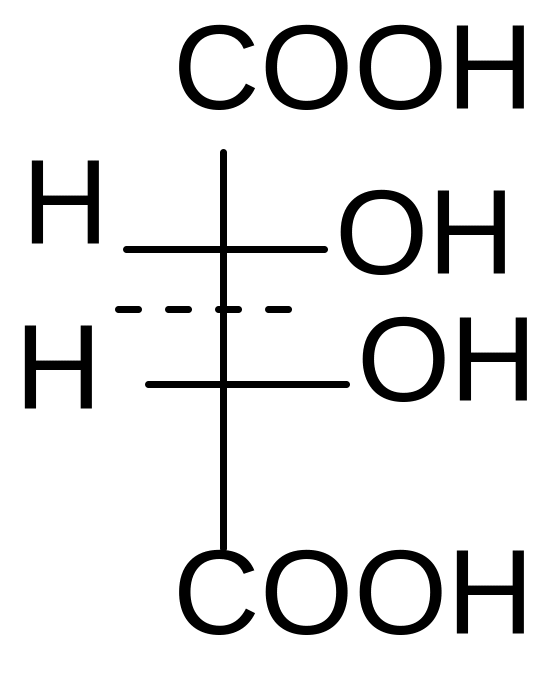
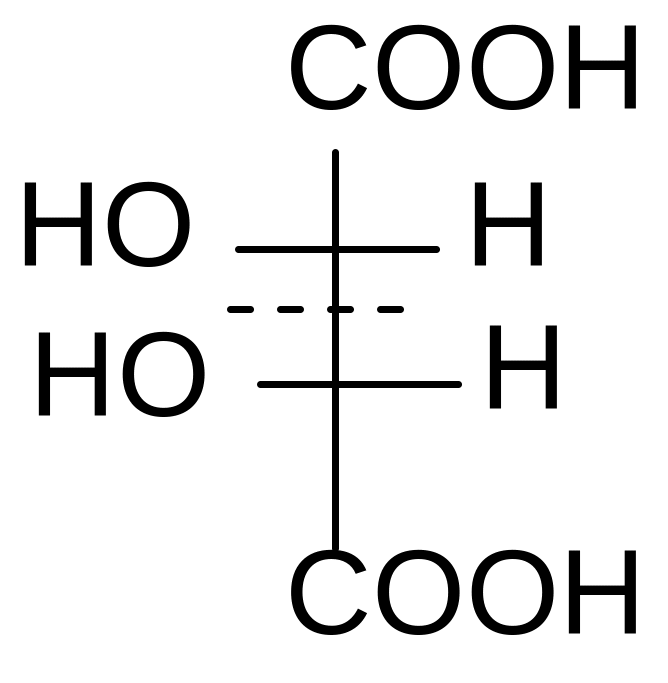
1 2 3 4
D–винная кислота; 2. L-винная кислота; 3, 4 – мезовинная кислота
1 и 2 – это энантиомеры (D и L). Они отличаются не по физическим и химическим свойствам, а только знаком вращения плоскости поляризованного света. Формулы 3 и 4 являются идентичными. Формулы 1 и 3, 2 и 3 являются пространственными изомерами, но не зеркальными, это диастереомеры. Они отличаются по физическим и химическим свойствам.
При отнесении энантиомеров к D– или L-ряду пользуются «оксикислотным ключом», т.е. сравнивают со стандартом тот хиральный центр, который остался без изменения при переходе от него. В данном случае это верхний хиральный центр (приведите путь превращения глицеринового альдегида в винную кислоту).
D– и L- энантиомеры проявляют оптическую активность. Мезовинная кислота – типичный пример молекулы, содержащей центры хиральности, но в целом являющейся ахиральной из-за наличия плоскости симметрии и потому не проявляющей оптическую активность.
Рацемат– это смесь равных количеств энантиомеров, не обладающая оптической активностью, вследствие компенсации вращения. Таким образом, у винной кислоты существуют 4 формы: 2 энантиомера (D- и L-), 1 мезо-форма и 1 рацемическая смесь. Рацемические смеси получаются синтетическим путем.
Поскольку природные источники не могут удовлетворить потребности современной биоорганической и биологической химии в разнообразных оптически активных соединениях, то либо расщепляют рацематы, либо ведут асимметрический синтез.
Существует несколько способов расщепления рацематов:
а) механический отбор кристаллов по их форме – исторически первый метод, примененный Луи Пастером;
б) биохимический (ферментативный) метод;
в) химический – через диастереомеры;
г) хроматографический на оптически активных сорбентах.
