
- •Техническая термодинамика
- •Часть 1
- •Иваново 2006
- •Научный редактор
- •Введение техническая термодинамика как теоретическая основа теплоэнергетики
- •1. Общие определения и понятия
- •1.1. Термодинамическая система
- •1.2. Термодинамические параметры состояния
- •Основные термические параметры состояния
- •Удельный объем
- •Давление
- •Соотношения единиц измерения давления
- •Температура
- •1.3.2. Уравнение состояния термодинамической системы
- •1.3.3. Термические коэффициенты
- •1.3.4. Термодинамический процесс
- •2. Первый закон термодинамики для закрытой системы
- •2.1. Работа изменения объема
- •2.2. Теплота, теплоемкость, энтропия
- •2.3. Внутренняя энергия
- •2.4. Первый закон термодинамики для закрытой системы
- •2.4.1. Аналитические выражения первого закона термодинамики.
- •2.4.2. Энтальпия
- •3. Газы и газовые смеси
- •3.1. Законы идеальных газов
- •3.1.1. Внутренняя энергия идеального газа
- •3.1.2. Теплоемкости газов
- •Удельные теплоемкости
- •Теплоемкости процессов
- •Теплоемкости идеальных газов
- •Теплоемкость реальных газов
- •Отношение изобарной и изохорной теплоемкостей
- •3.1.3. Энтальпия идеальных газов
- •3.1.4. Энтропия идеальных газов
- •3.2. Газовые смеси
- •Основные характеристики смеси газов
- •Теплоемкости газовых смесей
- •4. Газовые процессы
- •4.1. Политропные процессы
- •4.2. Частные случаи политропных процессов
- •Уравнения процессов, расчетные выражения их теплоты, работы, изменения внутренней энерги, энтальпии и энтропи
- •4.3. Изображение политропных процессов в р,V и t,s- диаграммах Политропа в р,V- диаграмме
- •Политропа в t,s- диаграмме
- •4.4. Установление показателя политропы по опытным данным
- •4.5. Качественный и количественный анализ политропных процессов в р,V- и t,s- диаграммах
- •4.6. Определение термодинамических свойств идеальных газов с учетом влияния температуры на их изобарную и изохорную теплоемкости
- •Определение энергетических параметров идеальных газов с учетом влияния температуры на cp и cv
- •5. Реальные газы и пары
- •5.1. Термические свойства реальных газов
- •5.2. Уравнения состояния реальных газов. Энергетические свойства реальных газов
- •6. Термодинамические свойства воды и водяного пара
- •6.1. Фазовые состояния и превращения воды
- •6.2. Фазовые диаграммы р,t-, р,V- и t,s для н2о
- •6.3. Жидкость на линии фазового перехода
- •6.4. Сухой насыщенный пар
- •6.5. Влажный насыщенный пар
- •6.6. Перегретый пар
- •6.7. Таблицы термодинамических свойств воды и водяного пара
- •6.8. Диаграмма t,s для воды и водяного пара
- •6.9. Диаграмма h,s для воды и водяного пара
- •6.10. Основные процессы изменения состояния водяного пара
- •Адиабатный процесс
- •Изохорный процесс
- •Изобарный процесс
- •Изотермический процесс
- •7. Влажный воздух
- •7.1. Основные характеристики влажного воздуха
- •7.2. Характеристики атмосферного влажного воздуха
- •Психрометр
- •Область ненасыщенного влажного воздуха
- •Область перенасыщенного влажного воздуха
- •Изображение в h,d- диаграмме изотерм меньше 0 оС и особенности характеристик влажного воздуха при отрицательных температурах
- •Пример пользования h,d- диаграммой
- •Изображение процессов влажного воздуха в h,d- диаграмме
- •8. Второй закон термодинамики
- •8.1. Замкнутые процессы (циклы)
- •8.1.1. Коэффициенты, характеризующие тепловую экономичность обратимых циклов
- •8.1.2. Цикл Карно
- •8.1.3. Обратный цикл Карно
- •8.1.4. Регенеративный (обобщенный) цикл Карно
- •8.1.5. Теорема Карно
- •8.1.6. Термодинамическая шкала температур.
- •8.2. Энтропия реальных тел и ее изменение в необратимых
- •8.3. Изменение энтропии изолированной системы
- •8.3.1. Изменение энтропии изолированной системы
- •8.3.2. Изменение энтропии изолированной системы
- •8.3.3. Принцип возрастания энтропии изолированной системы
- •8.4. Получение работы в изолированной системе. Эксергия в объеме и ее потери
- •8.4.1. Эксергия в объеме
- •8.4.2. Практическое значение эксергии
- •8.4.2.1. Определение эксергии источников работы, имеющих
- •8.4.2.2. Определение влияния необратимости на полезную работу в изолированной системе
- •Необратимый теплообмен
- •Необратимость, обусловленная преобразованием работы в теплоту путем трения
- •Необратимость при расширении газа в вакуум
- •Необратимость при диффузионном смешении газов с одинаковыми температурами и давлениями
- •Изменение энтропии газов в этом процессе будет определяться выражением
- •Необратимое преобразование теплоты в работу при источнике работы с постоянной температурой
- •Необратимое преобразование теплоты в работу при источнике работы с конечной теплоемкостью
- •Методы оценки тепловой экономичности реальных циклов тепловых машин
- •Заключение
- •Библиографический список
- •Оглавление
- •1.3.2. Уравнение состояния термодинамической системы……...……. 15
- •1.3.3. Термические коэффициенты……………………………………….. 17
- •Чухин Иван Михайлович
- •Часть 1
- •153003, Г. Иваново, ул. Рабфаковская, 34.
- •153025, Г. Иваново, ул. Дзержинского, 39.
6.10. Основные процессы изменения состояния водяного пара
Для расчета процессов изменения состояния водяного пара не используются имеющиеся для него уравнения состояния, ввиду их сложности и ограничений применимости в зависимости от области параметров состояния водяного пара (в различных областях используются различные уравнения). Применение таких уравнений оправдано, когда они заложены в современные ЭВМ и машина сама считает параметры по любой известной паре параметров по специальной программе.
Практически расчет процессов изменения состояния воды и водяного пара осуществляется с использованием таблиц их термодинамических свойств и диаграмм. Из диаграмм наибольшее применение нашли h,s- диаграммы.
Наиболее простым и наглядным является метод расчета паровых процессов с использованием h,s- диаграммы. Здесь не нужно выяснять, в какой области протекает процесс, есть ли переход из зоны перегретого пара в зону влажного пара или наоборот. Все это видно по графику процесса. Расчет сводится к чтению диаграммы и при необходимости к подсчету по полученным из диаграммы данным работы, теплоты и изменений параметров и функций состояния. Когда процесс выходит за пределы рабочей h,s- диаграммы, расчет проводится с использованием таблиц термодинамических свойств воды и водяного пара.
Диаграммы Р,v и T,s служат для иллюстрации особенностей процессов и могут быть применены для графического изображения в виде площадей энергетических величин q, , u , характеризующих данный процесс.
В практике теплоэнергетики наиболее часто встречаются: изохорный процесс (растопка котла при повышении давления), изобарный процесс (установившийся режим работы котла, процессы в подогревателях и конденсаторах пара), адиабатный процесс (в паровой турбине и насосе), изотермический процесс (испарение воды в реакторе кипящего типа).
Рассмотрим подробно эти процессы, считая их обратимыми.
Адиабатный процесс
В тепловых машинах, таких как турбина или насос, процесс протекает очень быстро и теплообмен с внешней средой очень незначителен, им можно пренебречь. Поэтому обратимым процессом в таких машинах является идеальная адиабата (изоэнтропа).
На рис. 6.24, 6.25, 6.26 изображен обратимый адиабатный процесс расширения пара 12 в Р,v-, T,s- и h,s- диаграммах.
В Р,v- диаграмме адиабата представляет собой кривую гиперболического характера с переменным показателем адиабаты "к". Необходимо отметить, что показатель адиабаты "к" для воды и пара никакого отношения к коэффициенту Пуассона cp/cv не имеет. Он рассчитывается только по параметрам обратимого адиабатного процесса вблизи какой - либо фиксированной точки по формуле
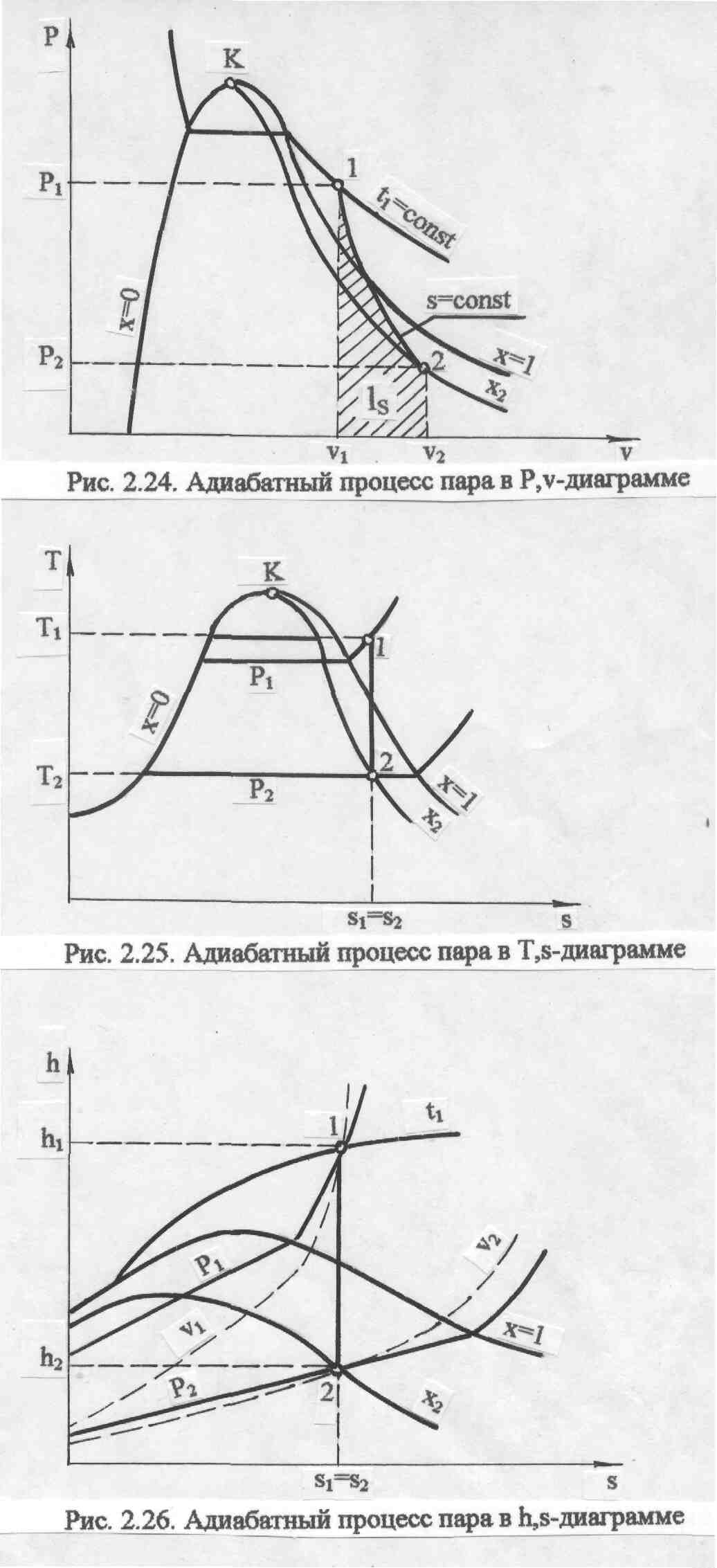
Рис.
6.24. Адиабатный процесс пара в P,v
- диаграмме

 .
(6.30)
.
(6.30)
Показателем адиабаты в расчетах процесса пользуются крайне редко ввиду того, что он – величина переменная. Его численные значения сильно отличаются друг от друга в различных точках адиабатного процесса: чем дальше расположены точки, тем больше разница. При переходе процесса из области перегретого пара в область влажного насыщенного эта разница еще больше увеличивается.
Площадь под процессом 12 в Р,v- диаграмме есть работа расширения, а поскольку qs = 0, то работа расширения адиабатного процесса равна изменению внутренней энергии с обратным знаком и может быть подсчитана как
s = u1 - u2 = (h1 - h2) - (Р1v1 - Р2v2) . (6.31)
В формуле (6.31) при расчетах следует обратить внимание на соответствие единиц измерения энтальпий и произведений Pv.
В Т,s- и h,s- диаграммах обратимый адиабатный процесс представляет вертикальную прямую (s=const – изоэнтропа). Представление энергетических характеристик (s, u) в Т,s- и h,s- диаграммах возможно с помощью дополнительных построений, но это не имеет практической ценности. В h,s- диаграмме разность энтальпий адиабатного процесса представляет работу изменения давления в потоке о = h1 - h2 (техническая работа в турбине, насосе и т.п.). С понятием этой работы познакомимся позднее при изучении процессов теплоэнергетических установок.
