- •382 Глава 13
- •Глава 14
- •384 Глава 14
- •386 Глава 14
- •388 Глава 14
- •390 Глава 14
- •392 Глава 14
- •Если аминокислоты: триптофан, тирозин, фенилаланин и гистидин—перемещаются в менее полярное окружение, Хмакс и є возрастают. Следовательно:
- •394 Глава 14
- •Абсорбционная спектроскопия 395
- •400 Глава 14
- •402 Глава 14
- •404 Глава 14
- •406 Глава 14
- •408 Глава 14
- •410 Глава 14
- •412 Глава 14
- •414 Глава 14
- •Глава 15
НЖ,.
14-u.
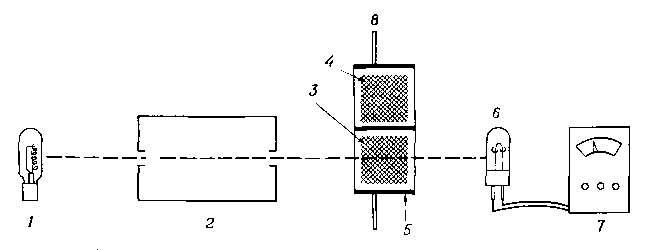
Схематическое
устройство спектрофотометра.
Свет
от лампы 1
проходит через монохроматор 2
для выделения пучка света с определенной
длиной волны. Образец 3
и растворитель 4
содержатся в двух кюветах, помещенных
в держатель кювет 5. Свет проходит через
кювету и падает на фотоэлемент 6, выходной
сигнал которого регистрируется
измерительным прибором 7. Держатель
кюветы находится на направляющих 8,
так что каждая кювета может быть
независимо помещена в пучок лучей.
дующий:
измеряют при одной длине волны
интенсивность света, прошедшего через
растворитель (который может быть
буфером), затем следует измерение
интенсивности света, прошедшего через
'раствор изучаемого вещества в том же
растворителе. Далее фиксируется
изменение в интенсивности света, по
которому можно судить о поглощении
растворенного вещества. На практике
прибор настраивают таким образом,
чтобы он показывал нулевое поглощение
при измерении одного растворителя (это
называется настройкой прибора на нуль).
Осуществив такую настройку, можно
снимать показания, соответствующие
непосредственно поглощению образца.
Для получения спектра эта операция
повторяется при многих длинах волн.
Некоторые приборы, называемые
автоматическими двухлучевыми
регистрирующими спектрофотометрами,
позволяют осуществлять развертку длин
волн и одновременно измерять поглощение
образца и растворителя (которые находятся
в различных кюветах) и фиксировать с
помощью электронного оборудования
суммированный поток излучений. При
этом на самописце вычерчивается спектр.
Эти приборы очень дорогие, но они
оправдывают себя при проведении большого
количества спектральных анализов.
Параметры,
измеряемые в абсорбционной спектроскопии
На
рис. 14-6 показаны спектры, снятые в
видимой и УФ-областях для двух
биологических молекул. Обычно определяются
величины D
или ε. Длина волны, соответствующая
максимуму погло-388 Глава 14
АБСОРБЦИОННАЯ
СПЕКТРОСКОПИЯ 389
ЩЄНИЯ,
называется
λмакс,
и
именно при этой длине волны обычно
определяют ε. Некоторые
полосы поглощения состоят из
многочисленных пиков, и часто
регистрируют длины волн, соответствующие
пикам, имеющим меньшие молярные
коэффициенты погашения. Эти длины
волн иногда также называют макс или
указывают, ЧТО
вещество
имеет максимумы поглощения при λ1,
λ2... ...λn,
Иногда
измеряют ширину полосы, хотя и не
обязательно.
В
табл. 14-1 * Приведен СПИСОК
величин
λмакс
и е
хромофоров, часто встречающихся в
биологических объектах.
ТАБЛИЦА
14-1
Максимумы
поглощения λмакс и молярные
коэффициенты погашения е
различных
веществ при нейтральных значениях pH,
используемых для биологических
исследований
Отметим,
что длина волны выражается в нанометрах
(нм). В более ранней литературе, а иногда
и сейчас используют миллимикроны
(ммк). Некоторые старые приборы
прокалиброваны в ангстремах (А). 1 нм
=1 ммк= = 10А=10-9 м.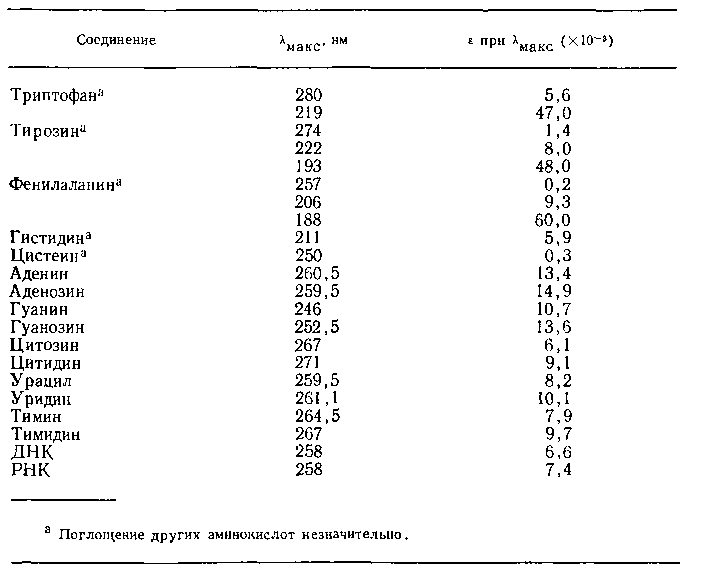
Рис.
14-6.
Сравнение
спектров поглощения двух биологических
молекул: флавинмононуклеотида
(а)
и фикоцианина (б). Спектры можно
использовать для идентификации
соединения.
Факторы,
влияющие на абсорбционные свойства
хромофора
Спектр
поглощения хромофора определяется в
первую очередь химической структурой
молекулы. Однако λмакс
и
ε претерпевают заметные изменения
и под влиянием окружения. Имеется в
виду влияние pH, полярности растворителя
или соседних молекул и относительная
ориентация соседних хромофоров. Именно
эти факторы лежат в основе использования
абсорбционной спектроскопии для
характеристики макромолекул.
Влияние
окружения состоит в следующем.
Эффект
pH.
pH раствора определяет ионную форму
ионизуемых хромофоров. На рис. 14-7
показан пример, иллюстрирующий
влияние pH на спектр тирозина.
Эффект
полярности.
В случае полярных хромофоров часто
справедливо (особенно если молекула
содержит О, N
или S),
что λмакс наблюдается при более коротких
длинах волн в полярных растворителях,
содержащих гидроксил (Н2О,
спиртах), чем в неполярных. Пример
приведен на рис. 14-8.
Эффекты
ориентации.
Величины λмакс
и є
существенно
зависят от геометрических особенностей
молекул. Наиболее известна гипохромия
нуклеиновых кислот, т. е. понижение
коэффициента погашения нуклеотида,
при условии, что нуклеотид входит в
состав одноцепочечного полинуклеотида,
в котором нуклеиновые основания сближены
и расположены друг над другом. Дальней-390 Глава 14
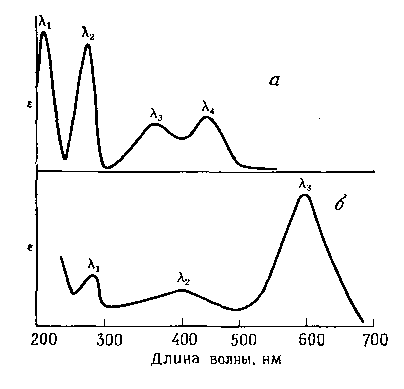
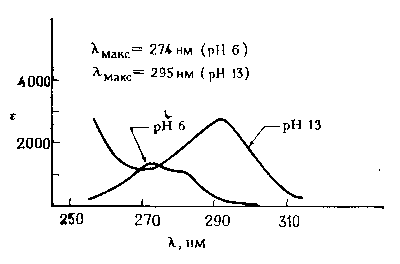
РИС.
14-7.
Спектр
поглощения тирозина при pH 6 и 13. Отметим,
что, как λмакс,
так и ε
возрастают при диссоциации ОН-группы
фенольного остатка.
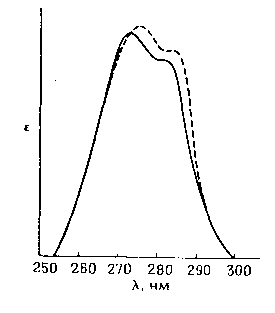
РИС.
14-8.
Влияние
полярности растворителя на спектр
поглощения тирозина.
Растворители:
вода (сплошная линия) и 20%-ный этиленгликоль
(штриховая линия). Отчетливо видно
возрастание λмакс в менее полярном
растворителе.
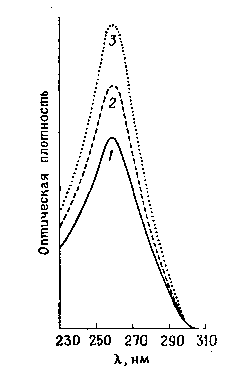
РИС.
14-9.
Спектры
поглощения ДНК фага Т7 в двухцепочечной
(1)
и одноцепочечной (2)
формах, а также после гидролиза до
свободных нуклеотидов (■?), показывающие
понижение оптической плотности (гипо-
хромию), которое сопровождает образование
более упорядоченной структуры. Спектры
получены при одинаковой концентрации.
АБСОРБЦИОННАЯ
СПЕКТРОСКОПИЯ 391