
- •Царенко с. В. Нейрореаниматология. Интенсивная терапия черепно-мозговой травмы
- •Аннотация
- •Оглавление
- •Глава 1. Методология оценки эффективности лечебных мероприятий
- •Глава 2. Травматические поражения мозга: теоретические предпосылки и принципы лечения
- •Глава 3. Экстрацеребральная патология при чмт - теоретические предпосылки и принципы лечения
- •Глава 4. Нейромониторинг
- •Глава 5. Диагностика и мониторинг экстрацеребральной патологии
- •Глава 6. Мероприятия интенсивной терапии
- •Вступление
- •Глава 1. Методология оценки эффективности лечебных мероприятий
- •Глава 2. Травматические поражения мозга: теоретические предпосылки и принципы лечения
- •2.1. Доктрина профилактики вторичного повреждения мозга
- •2.2. Повышение доставки кислорода и нутриентов
- •2.2.1. Увеличение перфузии и оксигенации
- •2.2.2. Изменение тонуса церебральных сосудов
- •2.2.3.Увеличение текучести крови
- •2.3. Снижение потребностей мозга
- •2.4. Особенности реализации доктрины профилактики вторичного повреждения мозга – физиологические факторы
- •2.4.1. Центральная регулирующая роль мозга и экстрацеребральные нарушения
- •2.4.2. Гематоэнцефалический барьер и осмотическое давление
- •2.5. Особенности доктрины профилактики вторичного повреждения мозга – анатомические факторы. Доктрина Монро-Келли
- •2.6. Противоречия доктрин
- •2.6.1. Гипервентиляция
- •2.6.2. Седативные препараты, наркотические анальгетики и миорелаксанты
- •2.6.3. Гиперосмоляльные препараты и салуретики
- •2.6.4. Артериальная гипертензия: концепция Лунда или вазоконстрикторный каскад?
- •2.6.5. Отек мозга – формы и стадии
- •2.6.6. Предупреждение гибели нейронов
- •Глава 3. Экстрацеребральная патология при чмт - теоретические предпосылки и принципы лечения
- •3.1. Водно-электролитные расстройства
- •3.1.1. Механизмы нарушения регуляции водно-электролитного обмена при чмт
- •3.1.2. Нарушения содержания натрия
- •3.1.3. Нарушения содержания калия
- •3.1.4. Другие электролитные нарушения
- •3.2. Нарушения кислотно-основного состояния
- •3.2.1. Респираторный алкалоз
- •3.2.2. Респираторный ацидоз
- •3.2.3. Метаболический алкалоз
- •3.2.4. Метаболический ацидоз
- •3.2.5. Комплексные (двойные и тройные) расстройства кос
- •3.3. Нарушения центральной гемодинамики
- •3.3.1. Поддержание объема циркулирующей крови
- •3.3.2. Артериальное давление
- •3.4. Острая дыхательная недостаточность
- •3.4.1. Основные причины дыхательных расстройств
- •3.4.2. Основные синдромы дыхательных расстройств
- •3.5. Острая почечная недостаточность
- •3.5.1. Преренальная опн
- •3.5.2. Истинная опн
- •3.5.3. Постренальная опн
- •3.5.4. Полиурия при чмт
- •3.5.5. Олигурия при чмт
- •3.6. Нарушения функции желудочно-кишечного тракта
- •3.7. Белково-энергетическая недостаточность
- •3.8. Нарушения системы гемостаза и тромбоэмболические осложнения
- •3.9. Гнойно-септические и иммунные нарушения
- •Глава 4. Нейромониторинг
- •4.1. Оценка неврологического статуса
- •4.2. Методы нейровизуализации.
- •4.3. Методы оценки мозгового кровотока.
- •4.4. Методики контроля внутричерепной гипертензии.
- •4.5. Методы оценки метаболизма мозга.
- •4.6. Нейрофизиологические методы.
- •Глава 5. Диагностика и мониторинг экстрацеребральной патологии
- •5.1. Диагностика сочетанных повреждений
- •5.2. Мониторинг гемодинамики
- •5.2.1. Измерение центрального венозного давления, давления в легочной артерии, давления заклинивания легочной артерии
- •5.2.2. Измерение сердечного выброса
- •5.2.3. Эхокардиография и электрокардиография
- •5.2.4. Ферментная диагностика
- •5.3. Мониторинг дыхания (респираторный мониторинг)
- •5.4. Лабораторный мониторинг: клинические и биохимические исследования
- •5.5. Мониторинг микрофлоры
- •Глава 6. Мероприятия интенсивной терапии
- •6.1. Периоды черепно-мозговой травмы
- •6.2.Нейрореанимационный период
- •6.2.1. Коррекция центральной гемодинамики
- •6.2.2. Обеспечение функции внешнего дыхания
- •6.2.2.1. Обеспечение проходимости дыхательных путей
- •6.2.2.2. Режимы ивл
- •6.2.2.3. Параметры ивл.
- •6.2.3. Коррекция внутричерепной гипертензии
- •6.2.4. Лечение и предупреждение судорог
- •6.2.5. Лечение внечерепных и внутричерепных гнойно-септических осложнений
- •6.2.6. Нутритивная поддержка
- •6.2.7. Мероприятия по уходу
- •6.3. Этап гнойно-септических осложнений и органной недостаточности
- •6.3.1. Коррекция гемодинамики
- •6.3.2. Респираторная поддержка
- •6.3.3. Поддержание оксигенации тканей
- •6.3.4. Противосудорожные препараты
- •6.3.5. Профилактика и лечение внечерепных гнойно-септических осложнений
- •6.3.6. Профилактика и лечение внутричерепных нагноений
- •6.3.7. Нутритивная поддержка
- •6.3.8. Хирургическое лечение
- •6.3.9. Мероприятия по уходу
- •6.4. Нейрореабилитационный этап
- •6.4.1. Принципы нейрореабилитации
- •6.4.2. Коррекция центральной гемодинамики
- •6.4.3. Респираторная поддержка
- •6.4.8. Мероприятия по уходу
- •6.5. Протоколы и алгоритмы лечебно-диагностических мероприятий на различных этапах чмт
- •6.5.1. Протокол диагностических мероприятий при поступлении в отделении реанимации Обязательные мероприятия
- •6.5.2. Протокол диагностических мероприятий при дальнейшем пребывании в отделении реанимации
- •6.5.3. Протокол выполнения кт головного мозга
- •6.5.4. Протоколы мониторинга и цели лечения в нейрореанимационном периоде
- •6.5.5. Алгоритм мероприятий при ухудшении неврологического статуса и (или) повышении вчд более 25 мм рт.Ст.
- •6.5.6. Алгоритм поиска и лечения гнойно-септических осложнений
- •6.5.7. Примерный суточный лист назначений в нейрореанимационном периоде (5-е сутки чмт)
- •6.5.8. Примерный суточный лист назначений в периоде гнойно-септических осложнений и органных нарушений (10-е сутки чмт)
- •6.5.9. Примерный суточный лист назначений в реабилитационном периоде (20-е сутки чмт)
- •6.6. Ятрогенные осложнения
- •6.6.1. Осложнения назо-и оротрахеальной интубации
- •6.6.2. Осложнения трахеостомии
- •6.6.3. Осложнения установки и использования желудочного зонда
- •6.6.4. Осложнения катетеризации мочевого пузыря
- •6.6.5. Осложнения катетеризации центральных и периферических вен
- •6.6.6. Осложнения нейромониторинга
- •6.6.7. Осложнения люмбальной пункции, катетеризации люмбального и вентрикулярного пространств
- •6.6.8. Недостатки ухода за кожей
- •Заключение
- •Приложение 1. Рекомендательный протокол оказания помощи на догоспитальном этапе при тяжелой чмт
- •Мероприятия на месте происшествия
- •Мероприятия при транспортировке
- •Приложение 2. Принципы оснащения нейрохирургической реанимации (в расчете на 10-коечное отделение)
- •Список литературы
2.6.4. Артериальная гипертензия: концепция Лунда или вазоконстрикторный каскад?
Наиболее распространенным методом приблизительной оценки церебрального кровотока является расчет церебрального перфузионного давления. Величину ЦПД рассчитывают как разницу между средним АД и ВЧД. Артериальное давление обеспечивает приток крови к мозгу, а ВЧД является фактором, препятствующим этому процессу. В соответствии с такими представлениями, повышение артериального давления должно быть одной из важных целей интенсивной терапии. Однако среди исследователей нет единства взглядов на эту проблему.
Ученые из университета г. Лунд (Швеция) считают, что избыточное давление крови в головном мозге может быть опасным. Согласно их взглядам, необходимо не повышение перфузионного давления, а ограничение ЦПД величиной 60 мм рт.ст. Авторы концепции рассматривают артериальную гипертензию как пусковой фактор вазогенного отека мозга из-за развития феномена "роскошной перфузии" и избыточного гидростатического давления в сосудах мозга. Эти исследователи предполагают, что избыточный кровоток в церебральных сосудах может приводить к транскапиллярному переходу жидкой части крови в интерстициальное пространство, развитию отека и дислокации мозга. Фактически эта гипотеза представляет собой механический перенос классической концепции Э.Старлинга для периферических сосудов на мозговой кровоток.
Немного физиологии. Концепция Старлинга основана на следующих теоретических представлениях (рис. 2.15).
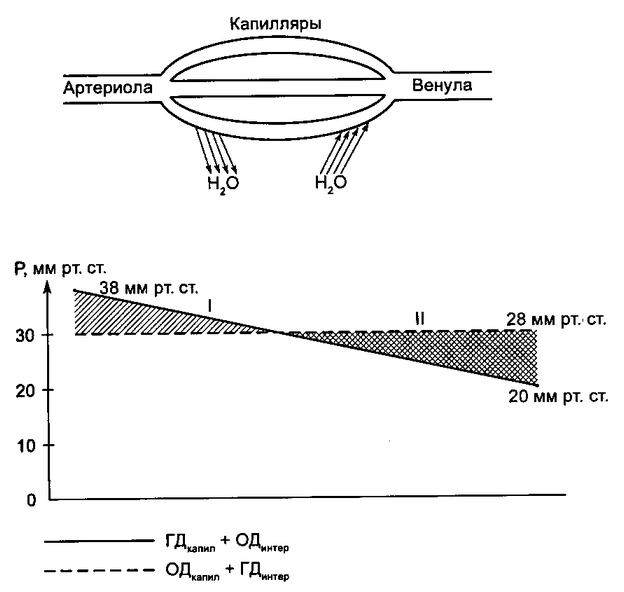
Рис. 2.15. Концепция Старлинга. I - вода поступает из сосуда в интерстициально пространство; II - вода поступает из интерстициального пространства в сосуд.
Перемещение жидкости через сосудистую стенку определяется влиянием гидростатического и онкотического давлений внутри и вне капилляра. Внутри капилляра гидростатическое давление (ГДкапил) перемещает жидкость из капилляра в интерстициальное пространство, а онкотическое давление (ОДкапил) удерживает воду в сосудистом русле. Вне капилляра – наоборот. Гидростатическое давление интерстициальной жидкости (ГДинтер) перемещает ее в капилляр, а онкотическое давление интерстиция (ОДинтер) удерживает в нем воду. Суммарное давление (Дсумм) определяется по следующей формуле:
Дсумм = K1 · (ГДкапил - ГДинтер) – K2 · (ОДкапил - ОДинтер),
где K1 – это коэффициент фильтрации, являющийся мерой способности сосудистой стенки к обмену воды, а K2 – коэффициент отражения, являющийся мерой способности стенки сосуда противодействовать прохождению через нее белка.
Для простоты можно считать, что ОДкапил, ОДинтер и ГДинтер – величины постоянные, а ГДкапил меняется на протяжении капилляра, постепенно снижаясь. На артериальном конце капилляра за счет высокого ГДкапил суммарное давление положительное, поэтому жидкость перемещается в интерстициальное пространство. На венозном конце суммарное давление отрицательное, так как онкотическое давление выше гидростатического, и поэтому жидкость поступает в сосуд. При патологических условиях коэффициенты K1 и K2 могут широко изменяться.
С целью снижения гидростатического капиллярного давления и транскапиллярной фильтрации концепция Лунда предполагает применение гипотензивных средств – β1-блокатора метопролола и α2-агониста клонидина (P.O. Grande, C.-H. Nordstrom, 1998).
Более широко приняты взгляды M.J. Rosner et al. (1992), которые считают минимально допустимым уровнем ЦПД 70 мм рт.ст. и не ограничивают верхний предел АД. Основанием для такого рода взглядов служит так называемая гипотеза "вазоконстрикторного каскада", согласно которой повышение системного АД включает механизмы ауторегуляции.
Немного физиологии. Ауторегуляцией мозгового кровотока называется механизм, которых обеспечивает его неизменность при колебаниях АД в определенных предела.
Повышение системного АД приводит к сужению сосудов мозга. При этом кровоток в мозге не меняется, кровенаполнение снижается. Снижение АД приводит к увеличению кровенаполнения также при неизменном мозговом кровотоке.
Мозговой кровоток в норме остается стабильным при колебаниях ЦПД от 70 до 170 мм рт.ст. (границы ауторегуляции). При гипертонической болезни обе эти границы смещаются вверх – от 90 до 180 мм рт.ст. Снижение ЦПД ниже границы ауторегуляции приводит к уменьшению и кровотока, и кровенаполнения. При превышении ЦПД верхней границы ауторегуляции увеличиваются и кровенаполнение, и кровоток. При нарушении ауторегуляции повышение ЦПД сопровождается повышением кровенаполнения мозга и церебрального кровотока (рис. 2.16).
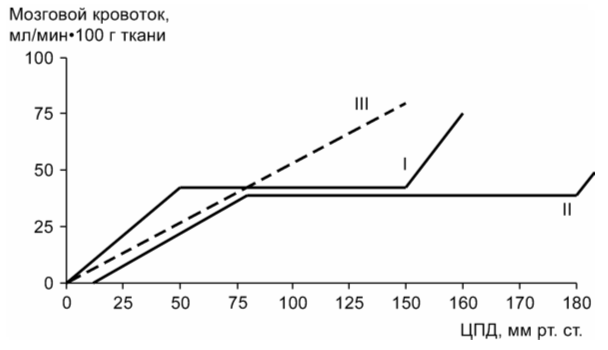
Рис. 2.16. Ауторегуляция мозгового кровотока при изменениях церебрального перфузионного давления (концепция Rosner). I - нормальная кривая (границы ауторегуляции 50 и 150 мм рт. ст.); II - изменение ауторегуляции при гипертонической болезни (границы 80 и 180 мм рт. ст.); III - нарушение ауторегуляции (линейная зависимость кровотока от ЦПД)
Существует и другие соображения о небезопасности предлагаемого шведскими исследователями ограничения верхнего предела АД. Здесь уместна аналогия с сосудистыми поражениями, например реноваскулярной гипертензией или ишемической болезнью сердца. При стенозах сосудов почек или сердца развивается системная артериальная гипертензия для обеспечения достаточного кровотока в наиболее ранимом месте – за суженным участком сосудистого русла. Для всего организма артериальное давление является избыточным, а для участка почки или сердца, кровоснабжаемого сосудами ниже места стеноза, едва достаточным. Если снизить системное АД, возникнет инфаркт миокарда или почки. Аналогично, при ЧМТ возможно наличие разной степени сужения сосудов из-за сдавливания их отечным мозгом или гематомой. В связи с этим тот уровень АД, который является избыточным для одних участков мозга, может быть минимально достаточным для обеспечения кровотока в других.
В настоящее время неясно, какая из гипотез, Rosner или Lund, ближе к истине. Более того, непонятно, имеют ли они обе клиническое значение. Наш опыт нейромониторинга свидетельствует, что ближе к реальной клинической практике мнение E.W. Lang (1998). Автор считает, что при повышении ЦПД под воздействием вазопрессоров возможны три типа реакций изменений кровенаполнения мозга, которые отражаются на величине ВЧД (рис. 2.17):
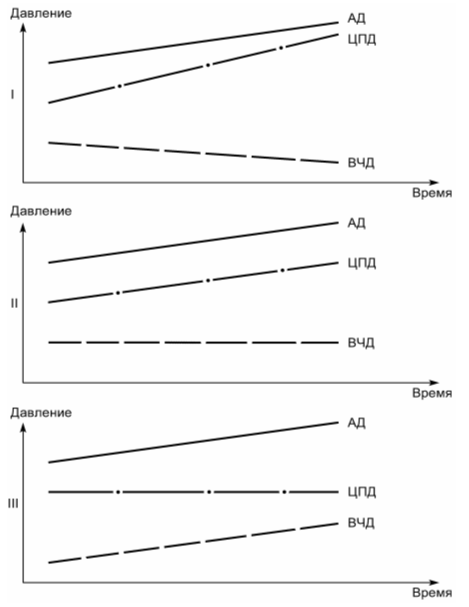
Рис. 2.17. Изменения ВЧД при повышении системного АД (по E. W. Lang и собственные данные). I - сохраненная ауторегуляция. Повышение АД приводит к снижению ВЧД, ЦПД нарастает. II - частично нарушенная ауторегуляция. Повышение АД не изменяет ВЧД, ЦПД нарастает; III - полностью нарушенная ауторегуляция. Повышение АД вызывает повышение ВЧД, ЦПД не изменяется
• Повышение ЦПД сопровождается снижением ВЧД. В этом случае сохранена ауторегуляция мозгового кровотока в ответ на изменения артериального давления.
• Повышение ЦПД не влияет на ВЧД. В данной ситуации судить об ауторегуляции трудно. Вероятнее всего она частично сохранена, так как ВЧД не повышается. Однако оно и не снижается, возможно, из-за наличия дополнительных факторов, вызывающих внутричерепную гипертензию.
• Повышение ЦПД вызывает увеличение ВЧД. Ауторегуляция нарушена, происходит увеличение внутричерепного объема крови с ростом ВЧД.
Наш опыт свидетельствует, что I тип реакции ВЧД наблюдается при положительной динамике ЧМТ, II тип – при стабильно тяжелом состоянии больных, III тип – при крайней тяжести состояния пациентов, близком к терминальному.
