
- •Вступ План
- •Рекомендована література:
- •1. Значення металів та сплавів в промисловості
- •2. Роль предмету та зв’язок з іншими предметами
- •2. Бялик о.М., Черненко в.С., Писаренко в.М., Москаленко ю.Н. Металознавство м. ”Политехника”, 2002
- •3. Лахтин ю.М. „Металловедение” и „Термическая обработка металлов”; м „Металлургия”; 1979
- •1. Основні поняття
- •2. Природа сил міжатомного зв'язку
- •3. Іонний зв'язок
- •4. Атомно-кристалічна будова металів
- •5. Характеристики кубічної та гексагональної систем
- •Тема: 1.2. Кристалізація металів та будова злитку. План
- •Рекомендована література:
- •1. Самохоцкий а.Н. „Металловедение”, изд. Металургія, 1990, м.
- •2. Бялик о.М., Черненко в.С., Писаренко в.М., Москаленко ю.Н. Металознавство м. ”Политехника”, 2002
- •3. Лахтин ю.М. „Металловедение” и „Термическая обработка металлов”; м „Металлургия”; 1979
- •1 . Енергетичні умови процесу кристалізації
- •2 . Механізм кристалізації
- •3. Кінетика кристалізації
- •4. Форма і розміри кристалів
- •5. Будова металевого зливка
- •6. Ліквація, усадка при кристалізації
- •Тема: 1.3 Поліморфізм металів. План
- •Рекомендована література:
- •1. Самохоцкий а.Н. „Металловедение”, изд. Металургія, 1990, м.
- •2. Бялик о.М., Черненко в.С., Писаренко в.М., Москаленко ю.Н. Металознавство м. ”Политехника”, 2002
- •3. Лахтин ю.М. „Металловедение” и „Термическая обработка металлов”; м „Металлургия”; 1979
- •1. Анізотропія кристалів
- •2. Поліморфізм металів
- •2.1. Поліморфізм заліза
- •3. Дефекти кристалічної будови
- •3.1 Точкові дефекти
- •3.2 Дислокації
- •3.3 Поверхневі дефекти
- •3.4 Об'ємні дефекти
2.1. Поліморфізм заліза
У рівноважному стані залізо має дві температури поліморфного перетворення: 911 і 1392°С. Воно кристалізується при температурі 1539°С (мал. 1.14) з утворенням кристалічної комірки об'ємноцентрованого куба Feα. При температурі 1392°С внаслідок вторинної кристалізації об'ємноцентрована ґратка Feα переходить у гранецентровану Feγ, а при 911°С — знову в об'ємноцентровану ґратку Feα. Критична температура 768°С не пов'язана з вторинною кристалізацією, а лише зі змінами в міжелектронній взаємодії, внаслідок чого залізо під час охолодження набуває магнітних властивостей. При температурах, вищих за 768°С, залізо немагнітне.
Зміна типу кристалічної будови у твердому стані відбувається шляхом зародження центрів нових кристалів і подальшого їх росту. Такий процес іноді називають вторинною кристалізацією на відміну від кристалізації первинної, що відбувається у рідині. Під час вторинної кристалізації зародки нових кристалів найчастіше виникають на границях зерен старих кристалів. Під час росту нових кристалів протягом певного часу зберігається когерентний зв'язок між новою і старою ґратками в площині, де атоми обох ґраток є спільними.
Х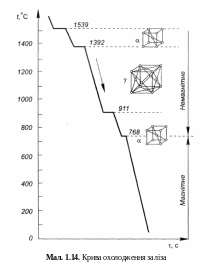 арактерною
особливістю вторинної кристалізації
є можливість досягти значного
переохолодження, внаслідок чого вдається
практично призупинити перебудову ґратки
завдяки зниженню швидкості самодифузії
атомів, необхідної для росту нових
кристалів. Збільшуючи переохолодження
до граничного значення, можна закріпити
термодинамічно нестійкий високотемпературний
стан і зберегти його протягом тривалого
часу при кімнатній температурі.
Поліморфні перетворення супроводжуються
стрибкоподібною зміною властивостей
металу і лежать в основі зміцнювальних
і знеміцнювальних термообробок.
арактерною
особливістю вторинної кристалізації
є можливість досягти значного
переохолодження, внаслідок чого вдається
практично призупинити перебудову ґратки
завдяки зниженню швидкості самодифузії
атомів, необхідної для росту нових
кристалів. Збільшуючи переохолодження
до граничного значення, можна закріпити
термодинамічно нестійкий високотемпературний
стан і зберегти його протягом тривалого
часу при кімнатній температурі.
Поліморфні перетворення супроводжуються
стрибкоподібною зміною властивостей
металу і лежать в основі зміцнювальних
і знеміцнювальних термообробок.
Різновидом поліморфізму є алотропія, тобто здатність одного елемента існувати у вигляді різних простих речовин.
Алотропічні перетворення (в металах) — зміни, що відбуваються в будові і властивостях металів під час їхнього нагрівання і охолодження.
Алотропічні перетворення призводять до утворення різних кристалічних форм або різної кількості атомів хім. елемента в молекулі простої речовини. При переході металу з однієї модифікації в ін. спостерігаються тепловий і об'ємний ефекти, причому кристалічні ґратки змінюються стрибкоподібно (не існує безперервного переходу). Об'ємний ефект алотропічного перетворення у різних металів різний і може змінюватися в широких межах. Напр., перехід білого β-олова (ґратки тетрагональні, об'ємноцентровані) в сіре α-олово (ґратки алмазного типу) супроводжується зміною об'єму на 26%. Під впливом внутрішніх напружень, що виникають при цьому, компактний метал перетворюється в порошок («олов'яна чума»). Також прикладом алотропічного перетворення є перебудова кристалічної ґратки графіту в кристалічну ґратку алмазу при надвисокому тиску і підвищеній температурі.
Серед металів алотропія виявлена (при температурі, вищій за кімнатну) у заліза, марганцю, кобальту, титану, цирконію, радію, талію, лантану, церію, урану.
Застосовуючи апаратуру високих тисків і температур, одержали модифікації легкоплавких металів (кадмій, церій, миш'як, галій, вісмут).
Експериментально доведено наявність низькотемпературного поліморфізму у натрію, літію, цезію, берилію. Найчастіше Алотропічні перетворення спостерігаються у металів, розміщених в середній частині періодичної таблиці.
