- •Нуклеиновые кислоты, строение и обмен Строение нуклеиновых кислот
- •Азотистые основания нуклеиновых кислот Пиримидиновые
- •Пуриновые
- •Моносахариды нуклеиновых кислот
- •Лабораторная работа № 10 «гидролиз нуклеопротеидов дрожжей»
- •Задания для домашней работы
- •Код белкового синтеза (мРнк)
- •Варианты заданий для домашней работы
- •Контрольная работа № 3 «пуриновые и пиримидиновые основания, нуклеозиды, нуклеотиды. Структура и свойства нуклеиновых кислот»
- •Углеводы
- •Лабораторная работа № 11 «углеводы»
- •1. Открытие крахмала в зеленых листьях растений
- •2. Реакция на восстанавливающие свойства сахаров (реакция Троммера)
- •3. Определение восстанавливающих (редуцирующих) веществ в вытяжке из лука
- •4 . Определение глюкозы в крови по методу Хагедорна и Иенсена
- •Содержание сахара по результатам титрования тиосульфатом
- •Лабораторная работа № 12 «количественное определение гликозилированного гемоглобина в крови человека»
- •1. Приготовление рабочих буферных растворов
- •6. Проведение анализа
- •7. Консервация микроколонок
- •Задания для домашней работы
- •Варианты заданий для домашней работы
- •Контрольная работа № 4 “обмен белков и нуклеиновых кислот. Углеводы и их обмен”
- •Липиды и их обмен
- •Л ипиды
- •Простые липиды
- •Сложные липиды
- •Фосфолипиды
- •Гликолипиды
- •Лабораторная работа № 13 "липиды"
- •1. Определение холестерина по методу Илька
- •Содержание холестерина
- •2. Определение йодного числа жиров
- •3. Определение кислотного числа жиров
- •4. Определение числа омыления жиров
- •Задания для домашней работы
- •Варианты заданий для домашней работы
- •Контрольная работа № 5 «липиды и их обмен»
- •Список использованной и рекомендуемой литературы
- •Кустова Татьяна Петровна кочетова Людмила Борисовна практикум по биологической химии
Нуклеиновые кислоты, строение и обмен Строение нуклеиновых кислот
Нуклеиновые кислоты – это биополимеры, состоящие из нуклеотидов, соединенных фосфодиэфирной связью.
Нуклеиновые кислоты являются многоосновными кислотами, которые при мягком гидролизе щелочами распадаются на мононуклеотиды. Мононуклеотиды при нагревании до 145 С с водным аммиаком теряют остаток фосфорной кислоты с образованием нуклеозидов. Нуклеозиды в условиях кислотного гидролиза распадаются на азотистые основания и сахара. Таким образом, при полном гидролизе нуклеиновых кислот образуются: 1) пуриновые и пиримидиновые азотистые основания; 2) моносахариды – рибоза или дезоксирибоза (пентозы); 3) фосфорная кислота.
Азотистые основания нуклеиновых кислот Пиримидиновые
|
|
|
|
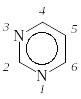
пиримидин, родоначальник ряда |
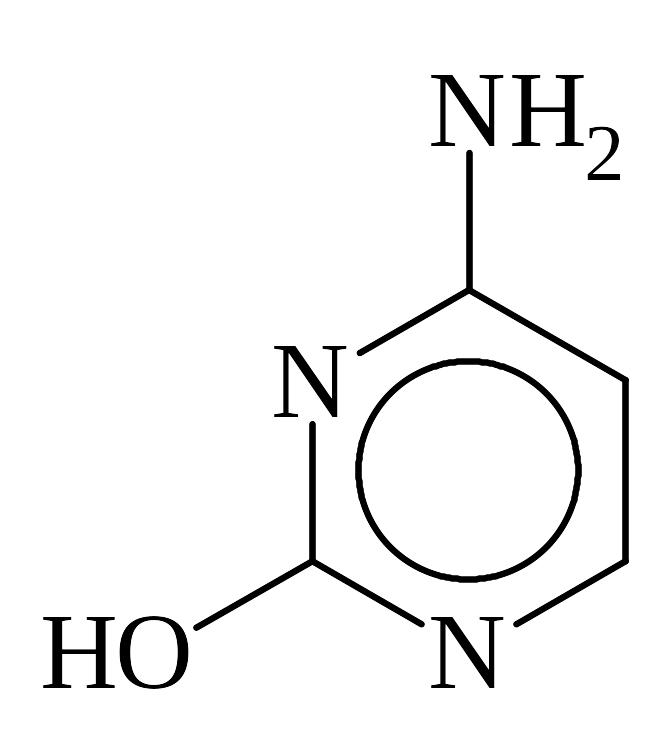
цитозин (Ц или С), 2-гидрокси-4-амино--пиримидин |
урацил (У или U), 2,4-дигидрокси-пиримидин |
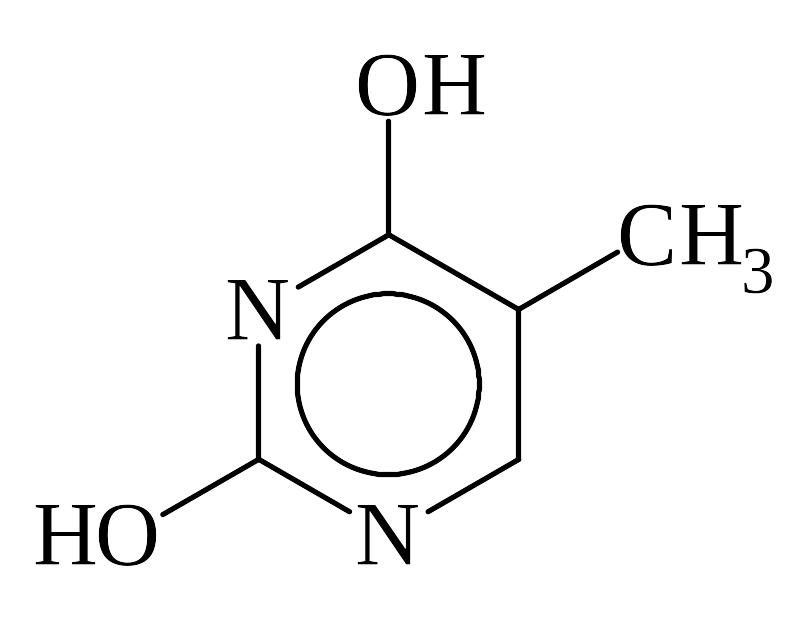
тимин (Т), 2,4-дигидрокси- 5-метилпиримидин |
Пуриновые
|
|
|
пурин, родоначальник ряда |
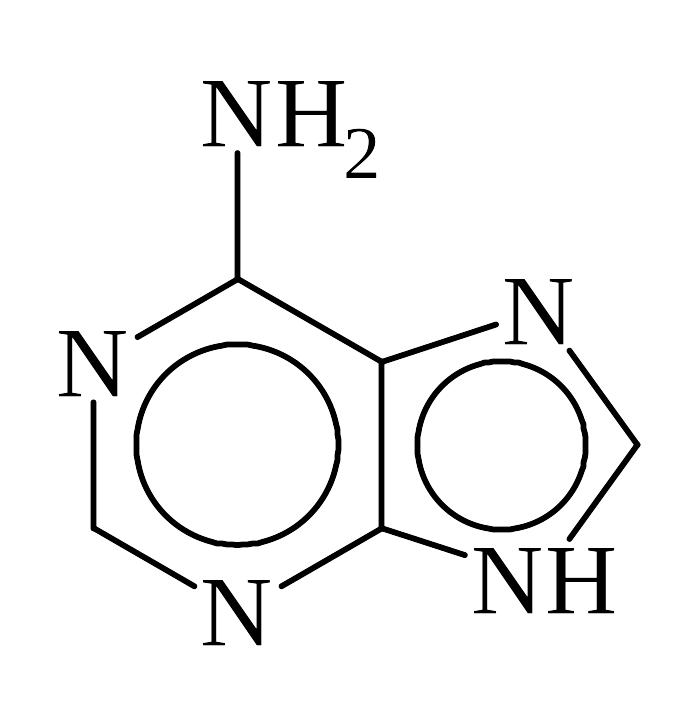
аденин (А), 6-аминопурин |
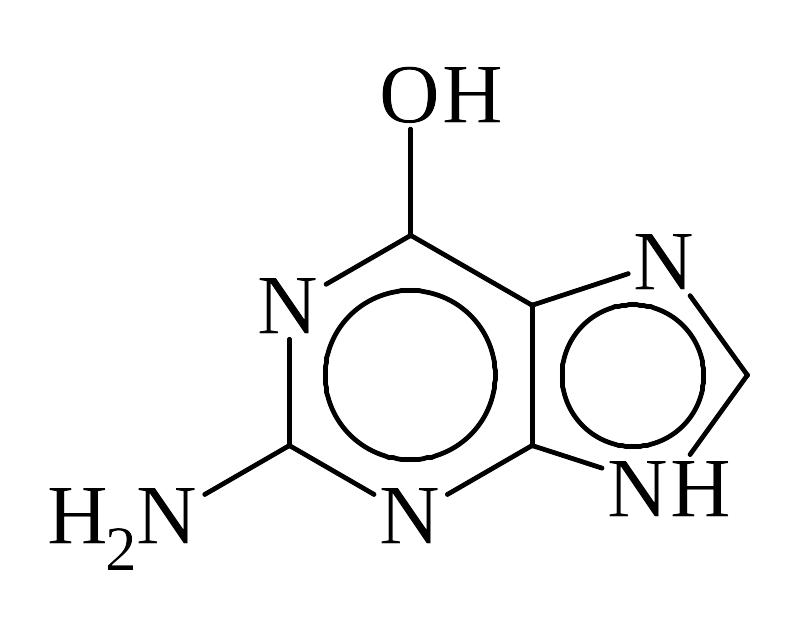
гуанин (Г или G), 2-амино-6-гидрокси-пурин |
В относительно небольших количествах при гидролизе нуклеиновых кислот обнаруживаются 5-гидроксиметилцитозин, 1-метиладенин, 2-метиладенин, 1-метилгуанин и 7-метилгуанин. Это минорные (иногда встречающиеся) азотистые основания.
Кето-енольная таутомерия азотистых оснований:

Моносахариды нуклеиновых кислот
Моносахариды – пентозы – в нуклеиновых кислотах присутствуют всегда в -D-фуранозной форме:
|
|
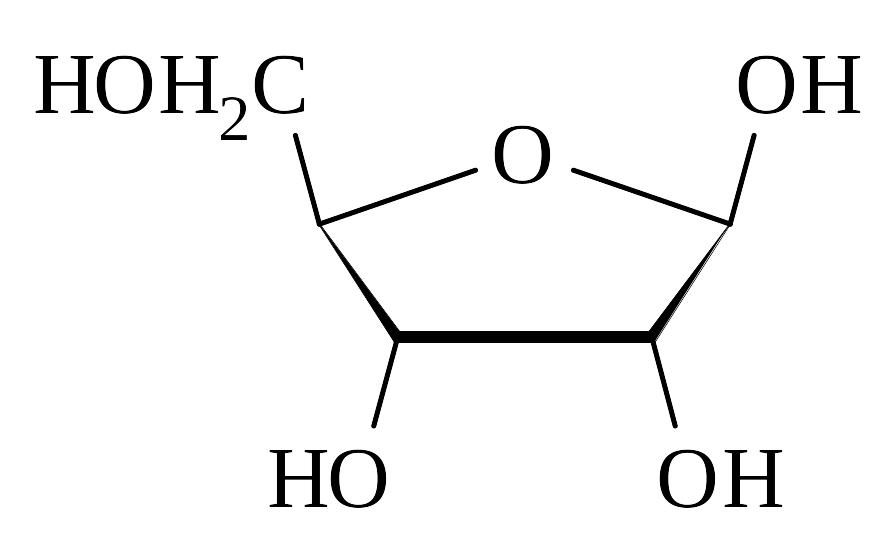
-D-рибоза (-D-рибофураноза) |
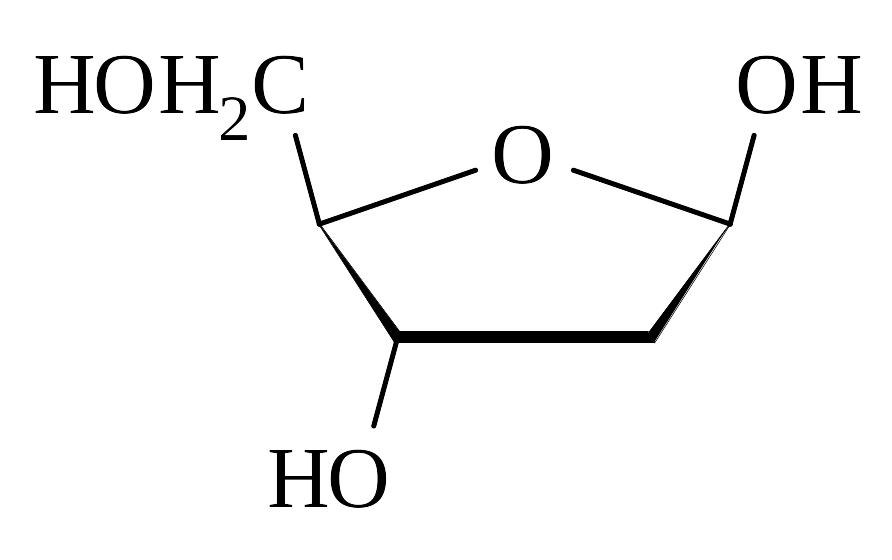
-D-дезоксирибоза (-D-дезоксирибофураноза) |
Недавно выяснено, что в состав ДНК может входить и глюкоза (выделена из некоторых фагов и раковых клеток).
Лабораторная работа № 10 «гидролиз нуклеопротеидов дрожжей»
Для изучения химического состава нуклеопротеидов проводят кислотный гидролиз дрожжей, поскольку они очень богаты нуклеопротеидами. Специфическими реакциями для каждого вещества открывают продукты гидролиза – полипептиды, пуриновые основания, пентозу и фосфорную кислоту.
Реактивы, оборудование и исследуемый материал: H2SO4 – 10 %-й раствор, NaOH – 10 %-й раствор, CuSO4 – 1 %-й раствор, аммиак конц, AgNO3 – 2 %-й раствор, молибденовый реактив, H2SO4 конц, тимол – 1 %-й спиртовой раствор, -нафтол – 0,2 %-й спиртовой раствор, лакмус, дифениламиновый реактив – 1 %-й раствор, круглодонная колба с воздушным холодильником, воронка с фильтром, мерный цилиндр на 50 мл, дрожжи пекарские.
Х о д р а б о т ы. Помещают 2,5 г пекарских дрожжей и 20 мл 10 %-го раствора H2SO4 в круглодонную колбу с воздушным холодильником для гидролиза. Гидролиз дрожжей проводят при нагревании в течение 1 часа с момента закипания жидкости. После охлаждения гидролизат фильтруют и с фильтратом проделывают качественные реакции на составные части нуклеопротеидов.
1. Биуретовая реакция на полипептиды: к 5 каплям гидролизата приливают 10 капель 10 %-го раствора NaOH до отчетливой щелочной реакции (по лакмусу), затем 2 капли CuSO4. Появляется розовая или розово-фиолетовая окраска.
2. Серебряная проба на пуриновые основания: к 10 каплям продукта гидролиза дрожжей добавляют по каплям крепкий раствор аммиака (приблизительно 10 капель) до щелочной реакции (по лакмусу), затем добавляют 10 капель 2 %-го аммиачного раствора AgNO3. Пробирку помещают в водяную баню на 5 мин. Образуется светло-коричневый осадок солей пуриновых оснований.
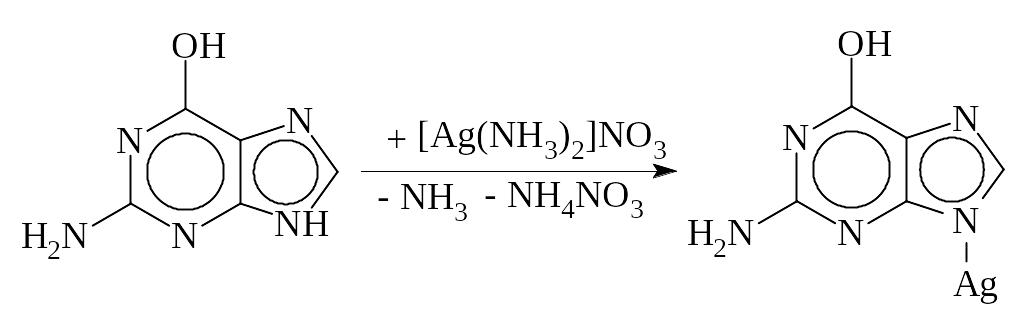
3. Качественная реакция на пентозу (Молиша): к 10 каплям гидролизата дрожжей добавляют 3 капли 1 %-го раствора тимола, перемешивают и по стенке пробирки осторожно приливают 20–30 капель H2SO4 (конц). При встряхивании на дне пробирки образуется продукт конденсации фурфурола с тимолом красного цвета.
Cхема реакции:

альдопентоза фурфурол

тимол
4. Качественная реакция на углевод: к 5 каплям гидролизата дрожжей приливают 3 капли 0,2 %-го спиртового раствора -нафтола и 20 капель H2SO4 (конц). Появляется розово-фиолетовое окрашивание.
5. Реакция на рибозу и дезоксирибозу: дифениламин с дезоксирибозой дает синее окрашивание, а с рибозой – зеленое. К 5 каплям гидролизата дрожжей добавляют 20 капель 1 %-го раствора дифениламина и кипятят на водяной бане 15 мин. Образуется сине-зеленое окрашивание.
6. Молибденовая проба на фосфорную кислоту: к 10 каплям гидролизата прибавляют 20 капель молибденового реактива и кипятят. При этом жидкость окрашивается в лимонно-желтый цвет (не осадок). Пробирку сразу охлаждают холодной водой. На дне появляется кристаллический лимонно-желтый осадок фосфорномолибденовокислого аммония.
H3PO4
+ 12 (NH4)2MoO4
+ 21 HNO3
![]()
(NH4)3PO4·12 MoO3 + 21 NH4NO3 + 12 H2O