
- •Указания к составлению отчёта Полученные результаты надо записать в виде таблицы:
- •Ферменты, коферменты и витамины
- •Лабораторная работа № 7 «изучение общих свойств ферментов»
- •1. Термолабильность ферментов
- •2. Влияние pH среды на активность ферментов
- •3. Дейстие активаторов и ингибиторов на активность амилазы слюны
- •4. Количественное определение амилазы слюны и мочи по методу Вольгемута
- •Лабораторная работа № 8 «биологическое окисление»
- •I. Качественная реакция на каталазу
- •II. Количественное определение каталазы
- •Витамины
- •II . Жирорастворимые витамины
- •III . Количественное определение витаминов
- •Содержание витамина с в распространенных фруктах и овощах
- •Задания к лабораторной работе «Качественные реакции на витамины и их количественное определение»
- •Варианты заданий к лабораторной работе № 9
- •Задания для домашней работы
I. Качественная реакция на каталазу
Реактивы: перекись водорода, кровь.
Х о д р а б о т ы. В две пробирки берут по 1 мл воды, добавляют 2 капли крови и одну пробирку кипятят 10 мин для дезактивации каталазы. После охлаждения в обе пробирки добавляют 5–10 капель 3 %-го раствора перекиси водорода, содержимое пробирок встряхивают. В какой из пробирок наблюдается выделение пузырьков кислорода? Объясните полученный результат.
II. Количественное определение каталазы
В основе этого метода лежит определение количества перекиси водорода, разложенной ферментом за определенный промежуток времени, по следующему уравнению:
KMnO4 + H2O2 + H2SO4 KHSO4 + MnSO4 + H2O + O2
(Напишите полуреакции, укажите окислитель и восстановитель.) Активность каталазы выражается с помощью каталазного числа.
Каталазное число – это количество миллиграммов перекиси водорода, которое разлагается одним микролитром крови.
Количество расщепленной перекиси водорода определяют по разности количества KMnO4, израсходованного на титрование пробы крови до и после действия каталазы.
Реактивы: перекись водорода, 1 %-й раствор, серная кислота, 10 %-й раствор, KMnO4 0,1 н раствор, кровь, разведенная в 1000 раз.
Х о д р а б о т ы. В мерной колбе на 100 мл разводят цельную кровь в 1000 раз. Разведенную кровь взбалтывают, пипеткой наливают в 2 конические колбы по 1 мл, приливают по 7 мл дистиллированной воды, в опытную (1) колбу добавляют 2 мл 1 %-го раствора Н2О2, а в контрольную (2) – 5 мл 10 %-го раствора H2SO4. Действие каталазы в кислой среде в колбе (2) прекращается, т. к. этот фермент действует при pH = 7,4. Колбы оставляют при комнатной температуре на 30 минут. Затем приливают в опытную (1) колбу 5 мл 10 %-го раствора H2SO4, а в контрольную (2) – 2 мл 1 %-го раствора Н2О2. Содержимое каждой колбы титруют 0,1 н раствором KMnO4 до розовой окраски. Рассчитывают каталазное число (КЧ) по формуле:
КЧ = 1,7· (А - В),
где А и В – количество мл 0,1 н раствора KMnO4, пошедшее на титрование контрольной пробы (2) и опытной пробы (1) соответственно, 1,7 – коэффициент перевода.
Норма каталазного числа колеблется от 10 до 15 единиц. Снижение каталазного числа наблюдается при анемии, туберкулезе, раке. Определение активности каталазы крови имеет значение для диагностики этих заболеваний.
Витамины
Витаминами (лат. vita – жизнь) называют низкомолекулярные органические соединения, необходимые для нормальной жизнедеятельности организмов и выполняющие in vivo каталитические и регуляторные функции. В соответствии с Международной химической номенклатурой (1956 г.) витамины подразделяются на 3 группы:
жирорастворимые (А, Д, Е, К),
водорастворимые (почти все витамины группы В, а также С, Н, Р, N, n-аминобензойная кислота),
витаминоподобные соединения (Q, F, В15, U).
Суточная потребность человека в витаминах 0,1–0,2 г. При отсутствии (длительном или полном) в пище одного из витаминов развивается авитаминоз. При недостаточном поступлении в организм витаминов – гиповитаминоз, при избытке витаминов в пищевом рационе – гипервитаминоз.
Лабораторная работа № 9
«КАЧЕСТВЕННЫЕ РЕАКЦИИ НА ВИТАМИНЫ
И ИХ КОЛИЧЕСТВЕННОЕ ОПРЕДЕЛЕНИЕ»
I . Водорастворимые витамины
1 . Качественная
реакция на витамин В1
. Качественная
реакция на витамин В1
тиамина хлорид (витамин B1)
Реактивы: диазореактив (5 капель 1 %-го раствора сульфаниловой кислоты в 2 %-м растворе соляной кислоты + 5 капель раствора NaNO2), Na2CO3 – 10 %-й раствор.
Х о д р а б о т ы. Диазореактив готовится непосредственно перед опытом. К 10 каплям диазореактива прибавляют 2–4 капли витамина и 5–7 капель раствора Na2CO3. Жидкость окрашивается в оранжевый или красный цвет.
2 . Качественная реакция на витамин В2
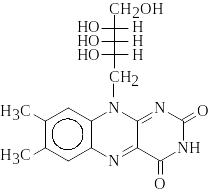
рибофлавин
Реактивы: НСl (конц), Zn (пыль), витамин В2 – 0,025 %-й раствор.
Х о д р а б о т ы. В пробирку наливают 10 капель раствора витамина В2, добавляют 5 капель соляной кислоты и немного цинковой пыли. Начинается выделение водорода, жидкость постепенно розовеет, затем обесцвечивается. Напишите уравнение реакции.
3 . Качественная
реакция на витамин В5
(PP)
. Качественная
реакция на витамин В5
(PP)
никотиновая кислота
|
амид никотиновой кислоты
|
Реактивы: (CH3COO)2Cu – 2 %-й раствор, витамин В5 – 1 %-й раствор, CH3COOH конц.
Х о д р а б о т ы. В ампулу с 1 %-м раствором витамина В5 добавляют 1 каплю концентрированной уксусной кислоты, все перемешивают. Затем из ампулы в пробирку набирают 20 капель раствора и нагревают до кипения, при этом мутный раствор становится прозрачным. Взболтав 2 %-й раствор ацетата меди, приливают 20 капель его к нагретому раствору витамина В5. Затем содержимое пробирки доводят до кипения и сразу охлаждают в токе холодной воды, на дне пробирки образуется синий осадок медной соли никотиновой кислоты. Напишите уравнение реакции.
4 . Качественная реакция на витамин С
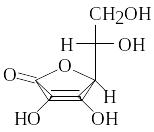
аскорбиновая кислота (витамин С)
Реактивы: 0,01 %-й раствор 2, 6-дихлорфенолиндофенола.
Х о д р а б о т ы. В пробирку наливают 10 капель 0,01 %-го раствора 2,6-дихлорфенолиндофенола. По каплям добавляют вытяжку из шиповника. Жидкость обесцвечивается, т. к. 2,6-дихлорфенол-индофенол окисляется аскорбиновой кислотой. Напишите уравнение реакции.

