
- •Гідрологія Лабораторні роботи
- •1 Відбір проб та їх консервація
- •1.1 Відбір проб води для лабораторного дослідження
- •2 Хімічний посуд
- •1.1 Визначення вмісту сухого залишку (з додаванням соди).
- •1.2 Визначення сухого залишку без додавання соди (проводиться в день добору води)
- •5.1 Визначення лужності
- •5.1.1 Визначення вільної лужності (р)
- •5.1.2 Визначення загальної лужності (m)
- •5.2 Визначення хлоридів
- •5.3 Визначення сульфатів
- •5.4 Визначення загальної жорсткості води
- •5.4 Визначення кальцію
- •5.5 Визначення магнію
- •5.6 Перевірка результатів аналізу сольового складу води
5.5 Визначення магнію
Загальна жорсткість (мг-екв)/дм3 - вміст Ca2+ (мг-екв)/дм3 = вміст Mg2+ (мг-екв)/дм3 . Для виразу результатів у мг/дм3 знайдене число (мг-екв)/дм3 помножують на 12,16 (еквівалент Ca2+).
5.6 Перевірка результатів аналізу сольового складу води
Як уже відзначалося, визначення сольового складу води звичайно зводиться до визначення катіонів: Са2+ і Мg2+ і аніонів: НСО3-, Cl-, і SO42-.
Лужні метали визначають розрахунковим шляхом як різницю між сумою еквівалентів всіх аніонів і катіонів
![]() (5.12)
(5.12)
Для виразу результатів у мг помножують на умовну еквівалентну вагу лужних металів, на 25.
Взагалі, різниця в зазначеному вище виразі, завжди повинна бути позитивною, тому що в будь-якій природній воді містяться лужні метали. Результати аналізу можуть також контролюватися величиною сухого залишку, одержуваного практично. Ясно, що сума катіонів і аніонів (мг) не може перевищувати цієї величини:
![]() <
величини сухого залишку
<
величини сухого залишку
У сухий залишок, окрім мінеральних речовин, входять і органічні речовини, що не враховуються. Внаслідок розкладання органічних речовин і гідрокарбонатів при нагріванні, величина сухого залишку взагалі є дуже хитливою.
Найбільш схожі результати виходять, якщо розрахунок вести на сухий прожарений залишок, приймаючи в розрахунок не НСО3-, а СО32- (половину лужності), у виді розкладання НСО3- за схемою:
2НСО3- СО32- + Н2О + СО2
Для усунення помилки, викликаної розкладанням карбонатів при високій температурі (СаСО3 СаО + СО2), прожарений залишок можна змочити розчином вуглекислого амонію і додатково прожарити при невисокій температурі (400 ˚С).
Отриману аналітичним шляхом суму катіонів і аніонів називають мінералізацією вод.
Контрольні питання
1 Назвіть чинники, що впливають на формування хімічного складу природних вод.
2 Які Ви знаєте класифікації природних вод за хімічним складом?
3 Як класифікують води за мінералізацією, жорсткістю?
4 Які бувають річкові води за ступенем їх мінералізації?
5 Як типізуються озера за хімічним складом води?
6 Яким чином графічно можна зобразити дані про хімічний склад води?
7 Які Ви знаєте способи для позначення концентрацій розчинів?
8 Охарактеризуйте гідрохімічну зональність природних вод.
9 Чому при тій же самій масі солі Mg більше впливають на жорсткість, ніж солі кальцію?
10 Як зміниться співвідношення лужних катіонів при забрудненні природних вод стоками з полів, де застосовували комплексні мінеральні добрива?
11 Вмістом яких сполук зумовлена лужність води?
12 Який метод аналізу використовується при визначенні лужності води? В яких одиницях вимірюється лужність води?
13 Яке значення лужності рекомендовано ДСанПіН для питної води? При яких процесах обробки води має значення величина її лужності?
14 Які солі обумовлюють жорсткість води? Чому катіони лужних металів не впливають на жорсткість води (на прикладі мила)?
15 Які є види жорсткості води? Яка допустима жорсткість питної води?
16 Що таке окислюваність води, в яких одиницях вимірюється? Назвіть головні види окислюваності.
17 Як за значенням окислюваності оцінити ступінь забруднення води?
Техніка безпеки при виконанні лабораторних робіт
Під час роботи в хімічній лабораторії необхідно суворо дотримуватися таких загальних правил безпеки:
1 Студенти обов’язково повинні працювати в халатах, вони зобов’язані підтримувати чистоту й порядок на робочому місці в лабораторії.
2 Слід точно дотримуватись порядку й послідовності операцій, вказаних у даних методичних вказівках. Не дозволяється приступати до виконання лабораторної роботи доти, доки студент не опанує всієї техніки її проведення.
3 Склянки з реактивами загального користування повинні знаходитись на визначеному місці; забороняється їх переносити на робочі столи. Слідкуйте за тим, щоб на всіх банках з реактивами були етикетки з написом назви речовини та її концентрації. Перед і після використання скляного посуду, його слід ретельно вимити.
4 Працювати в лабораторії слід обережно, не проливати і не просипати реактиви. Надлишки реактивів суворо забороняється зсипати чи зливати назад у склянку з чистими реактивами.
5 Досліди з легкозаймистими, леткими, вогненебезпечними, токсичними речовинами, або речовинами, які мають неприємний запах, слід проводити подалі від відкритого полум’я і у витяжній шафі.
6 Забороняється зливати в раковину залишки кислот, лугів, вогненебезпечні рідини й рідини з сильним запахом; їх треба зливати в спеціальні склянки.
7 Категорично забороняється смакувати, нюхати хімічні речовини, або пити воду з хімічного посуду.
8 Забороняється під час нагрівання рідин і твердих речовин у пробірках спрямовувати їх отвором на себе, або в бік студентів, які знаходяться поряд; забороняється нахилятись над склянками, або заглядати в пробірку зверху, щоб уникнути нещасного випадку в разі можливого викиду нагрітої речовини або уламків скла.
9 Прилади, які необхідно нагрівати, або з яких будуть виділятися гази не слід залишати закритими.
10 Категорично забороняється вмикати без дозволу викладача будь-які прилади й рубильники.
11 При всіх роботах, коли можливе розбризкування їдких речовин (переливання кислот, лугів, або подрібнення чи розтирання в ступках, сплавлення та ін.) необхідно одягати захисні окуляри.
12 Для попередження бурхливого закипання і викиду рідини, яка нагрівається до кипіння, необхідно користуватись «кипілками» (шматочками подрібненого фарфору або скляні кільки). «Кипілки» забороняється додавати в нагріту до кипіння рідину, їх слід вносити тільки в холодну рідину.
13 Під час розведення концентрованих кислот, особливо сульфатної, слід лити її у воду, а не навпаки.
14 У разі виникнення непорозумінь стосовно виконання дослідів лабораторної роботи необхідно припинити роботу й звернутися до викладача.
15 На робочому місці категорично забороняється вживати їжу та пити воду.
16 По закінченню роботи необхідно привести в порядок своє робоче місце і як слід вимити руки.
17 У разі нещасного випадку слід негайно звернутися до викладача.
Необхідно стежити за вентиляцією лабораторії і у витяжній шафі, не допускати роботи при поганій вентиляції.
В лабораторії в доступному місці встановлюють аптечку, в якій повинні бути індивідуальні пакети, вата, борна кислота кристалічна і в розчині (2 %-ний), йодна настойка, клей БФ-6, марганцевокислий калій, розчин оцтової кислоти (2 %-ний), лейкопластир, мазь від опіків, розчин двовуглекислої соди (5 %-ний), нашатирний спирт, пінцет, ножиці, склянка для промивання очей тощо.
Робота зі склом. Хімічний посуд здебільшого тонкостінний, тому потребує уважного ставлення для запобігання можливому пораненню. Хімічний посуд треба тримати в руках, не стискуючи сильно пальцями. Треба обережно мити посуд йоршами чи скляними паличками, щоб не пробити дно або стінки.
При розрізанні скляних трубок, паличок, відкриванні ампул руки треба захищати рушником. У випадку невеликого порізу склом треба вилучити осколки скла, змити кров навколо рани ватним тампоном, змоченим розчином марганцевокислого калію, змазати йодом і зав'язати бинтом або заклеїти лейкопластиром. При невеликих порізах ранку покривають клеєм БФ-6 (для обробки мікротравм).
При глибоких артеріальних ранах після вилучення скла треба міцно перев'язати руку вище порізу джгутом, витерти кров навколо рани, накласти кілька шарів стерильної марлі, потім товстий шар гігроскопічної вати і викликати лікаря.
Робота з електроприладами. При роботі з електроприладами (електроплитка, освітлювальні прилади, рН-метри) не допускати іскріння контактів, ретельно ізолювати дроти, не допускати потрапляння на них води. Під електроплитку підкладають азбест чи керамічну пластинку. Всі несправності усувають, лише слід попередньо виключити прилади з мережі. Якщо зникає електричне живлення, в лабораторії слід вимкнути всі електроприлади. Залишають включеною лише одну контрольну лампочку.
Робота з реактивами. Дуже важливо знати особливості хімічних сполук, з якими гідрохіміку доводиться мати справу.
При роботі з рідкими кислотами треба пам’ятати, що вони можуть спричинювати важкі, погано заживаючі хімічні опіки. Особливо обережним треба бути при переливанні кислот з великих бутилів.
Великі пляшки з кислотами та іншими рідинами мають зберігатися в плетених корзинах і на спеціальних стояках. При переливанні і розведенні великих кількостей димлячих кислот (хлорна, нітратна) слід одягати респіратор, або ж обв’язувати ніс і рот марлевою пов’язкою, змоченою розчином соди, при цьому обов’язково використовувати запобіжні окуляри. Переливання малих кількостей кислот роблять лише у витяжній шафі.
Розбавляти кислоти потрібно лише певним чином — лити кислоту у воду, а не навпаки.
При попаданні сильних кислот (азотна, соляна, сірчана, хромова суміш) на тіло слід обмити місце спочатку великою кількістю води, а потім 5 %-ним розчином двовуглекислої соди. В разі опіків плавиковою кислотою пошкоджене місце промивають водою протягом 4—6 год., доки побіліла поверхня опіку не почервоніє. Потім на обпечене місце прикладають свіжо приготовану пасту окису магнію в гліцерині.
При опіці лугами також треба обмити вражене місце великою кількістю води, а потім 2 %-ним розчином оцтової кислоти.
При розчиненні лугів у воді спостерігається сильне розігрівання, тому луги треба розчиняти в порцеляновому посуді — спочатку концентровані розчини, а після охолодження розбавити до потрібної концентрації.
При попаданні в рот лужного розчину йодистого калію порожнину рота промивають спочатку водою, а потім 2 %-ним розчином борної кислоти до усунення мильного присмаку в роті і знову водою. Потім порожнину рота змазують харчовим жиром.
Якщо в порожнину рота потрапив розчин азотнокислого срібла, необхідно промити рот великою кількістю розчину хлористого натрію.
Випадки отруєння реактивами в лабораторії, де передбачені всі заходи з техніки безпеки, надзвичайно рідкісні, але вони не виключені, і тому необхідно знати прийоми надання першої допомоги до прибуття лікаря. При отруєнні необхідно ввести потерпілому в шлунок відповідні речовини.
При отруєнні кислотами (хлорною, сірчаною, оцтовою) вводяться мильна вода, магнезія, сода, вапнякова вода, молоко, рідке мучне тісто, слизисті відвари.
При отруєнні лугами (їдкі луги, поташ, аміак, сода) вводяться лимонна кислота, 5 %-на оцтова.
При отруєнні солями (азотнокисле срібло, нітрати, мідна сіль, ртутна, свинцева) вводиться яєчний білок, велика кількість молока.
При отруєнні йодом вводиться крохмаль з водою, в'яжучі настойки, міцний чай або кофе.
Під час роботи з реактивами і розчинами треба завжди пам'ятати, що піпетку наповнюють розчинами кислот, лугів та інших речовин лише за допомогою груші або використовують піпетки з кулькою.
Всю роботу зі шкідливими та отруйними речовинами необхідно проводити лише під тягою, дотримуючись усіх заходів безпеки.
Робота з нагрівальними приладами. Всі нагрівальні прилади встановлюють на теплоізоляційній підставці. При необережній роботі можливі опіки приладом, нагрітим скляним посудом, тиглями тощо, тому не можна брати гарячий посуд голими руками. Звичайно нагріті предмети беруть щипцями, колботримачами, джгутом з рушника, але зручніше користуватись спеціальними короткими гумовими трубками з поздовжніми розрізами для захисту пальців від опіку. Необхідно уважно стежити за роботою нагрівальних приладів, не залишаючи їх без нагляду.
В приміщенні лабораторії завжди повинні бути наготові протипожежні засоби: вогнегасники, азбест, пісок та пожежний водопровідний кран. Треба пам’ятати, що гасити водою можна лише такі речовини чи матеріали, які розчиняються у воді чи важчі за неї. Зовсім недопустимо гасити водою масло, керосин, бензин тощо.
У випадку опіків першого ступеня (почервоніння) обпечене місце треба занурити в розчин марганцевокислого калію, концентрація якого тим більша, чим сильніший опік. Можна скористатися мазями від опіків.
При опіках другого ступеня (пухирі) обпечене місце обробляють марганцевокислим калієм чи 5 %-ним розчином тоншу.
При опіках третього ступеня (руйнування тканин) рану покривають стерильною пов'язкою і викликають лікаря.
Допомога при термічних і хімічних опіках. У разі термічного опіку (полум'ям пальника або нагрітими предметами) уражене місце необхідно негайно протерти ватою, намоченою етиловим спиртом або розчином перманганату калію. В разі сильного опіку потрібно накласти стерильну пов’язку або накрити обпечене місце чистою тканиною і обов’язково звернутись до лікаря.
Концентровані кислоти (хлорна, сульфатна, нітратна тощо) та луги (їдкий натрієм, їдкий калі) при потраплянні на шкіру або в очі можуть завдати дуже тяжкі хімічні опіки. При опіках шкіри кислотою уражене місце слід негайно промити великою кількістю води, потім 3–5 %-ним розчином питної соди (гідрокарбонатом натрію) і знову ретельно промити водою. При потраплянні кислот або кислотної пари в очі, або до ротової порожнини, треба багаторазово промити їх струменем води, потім розчином питної соди та знову водою. При опіках шкіри їдкими лугами слід добре промити вражене місце водою (до зникнення відчуття слизькості), а потім 3–5 %–ним розчином оцтової (або борної) кислоти. В разі опіку очей лугом треба їх промивати під струменем води не менше 15 хвилин і негайно звернутися до лікаря.
Література
Базова
1 Загальна гідрологія. Підручник / за ред. С.М. Лисогора – К.: Фітосоціоцентр, 2000. – 264 с.
2 Акимова Т.А., Хаскин В.В. Экология. Человек – Экономика – Биота – Среда: Учебник для вузов. 2-е изд., перераб. и доп.. – М.: ЮНИТИ-ДАНА, 2001. – 566 с.
Інформаційні ресурси
База нормативних документів Режим доступу http://csm.kiev.ua/nd/nd.
1 ДСТУ ISO 5667-3-2001 Якість води. Відбирання проб. Частина 3. Настанови щодо зберігання та поводження з пробами (ISO 5667-3:1994, IDT)
2 ДСТУ ISO 5667-6:2009 Якість води. Відбирання проб. Частина 6. Настанови щодо відбирання проб з річок і струмків (ISO 5667-6:2005, IDT)
3 ДСТУ ISO 5667-8:2007 Якість води. Відбирання проб. Частина 8. Настанови щодо відбирання проб вологих опадів (ISO 5667-8:1993, IDT)
4 ДСТУ 4077-2001 Якість води. Визначання pH (ISO 10523:1994, MOD)
5 ДСТУ 4079-2001 Якість води. Визначання загального вмісту хлоридів. Титрування нітратом срібла із застосуванням хромату як індикатора (метод Мора) (ISO 9297:1989, MOD)
6 ДСТУ ISO 9963-1:2007 Якість води. Визначення лужності. Частина 1. Визначення загальної та часткової лужності (ISO 9963-1:1994, IDT)
7 ДСТУ ISO 6059-2003 Якість води. Визначання сумарного вмісту кальцію та магнію. Титрометричний метод із застосовуванням етилендіамінтетраоцтової кислоти (ISO 6059:1984, IDT)
8 ДСТУ ISO 6058-2003 Якість води. Визначання кальцію. Титрометричний метод із застосовуванням етилендіамінтетраоцтової кислоти (ISO 6058:1984, IDT)
9 ДСТУ ISO 6060-2003 Якість води. Визначання хімічної потреби в кисні (ISO 6060:1989, IDT)
10 ДЕРЖАВНІ САНІТАРНІ НОРМИ ТА ПРАВИЛА "Гігієнічні вимоги до води питної, призначеної для споживання людиною"
(ДСанПіН 2.2.4-171-10)/ затверджено Наказ Міністерства охорони здоров’я України 12.05.2010 N 400 Режим доступу: http://zakon4.rada.gov.ua/laws/show/z0452-10
Додаток А
Форма звіту за лабораторну роботу
Кафедра екології
Прізвище студента Група
Назва роботи Дата виконання
Звіт за лабораторну роботу
Мета роботи
Теоретичні відомості
Обладнання та матеріали:
Короткий план проведення роботи
Результати досліджень, розрахунки
Висновки
Додаток Б
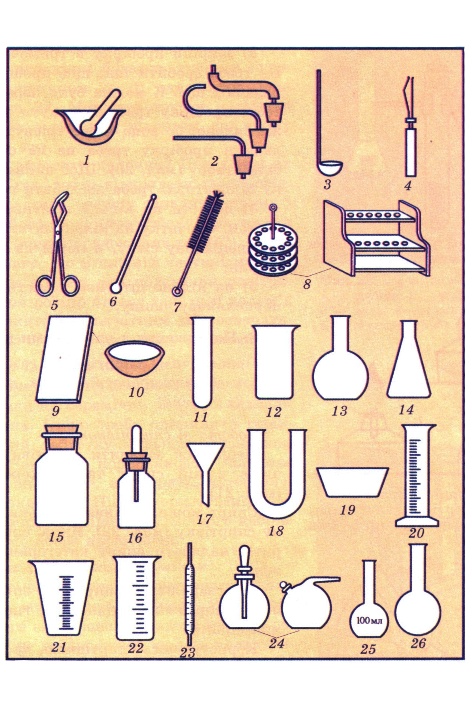
Рисунок Б.1 - Хімічний посуд та інше лабораторне обладнання
1 - ступка з товкачиком; 2- газовідвідні трубки з пробками; 3 - ложка для спалювання речовин; 4 - пробіркотримач; 5 - тигельні щипці; 6 - скляна паличка; 7 - йоржик; 8 - штативи для пробірок; 9 - скляна пластинка; 9 - чашка для випарювання; 10 - пробірка; 11 - хімічна склянка; 13 - колба плоскодонна; 14 - колба конічна; 15 - банка; 16 - склянка з піпеткою; 17 - лійка; 18 - U-подібна трубка; 19 - каталізатор; 20 - мірний циліндр; 21 - мензурка; 22- мірна склянка; 23- піпетка градуйована; 24 - крапельниці; 25 - мірна колба; 26 - круглодонна колба.
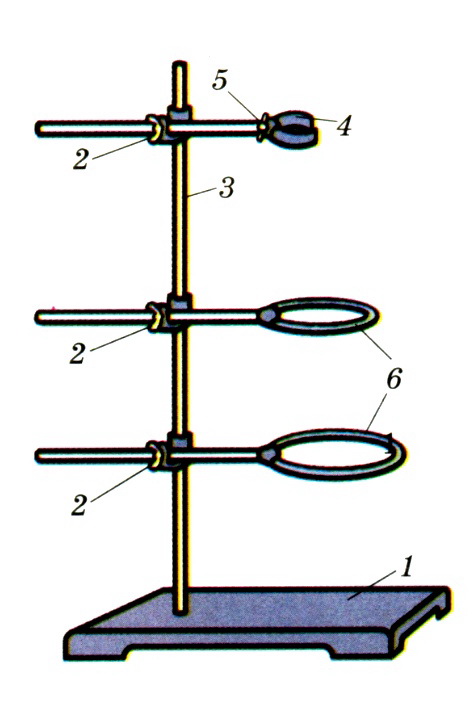
Рисунок Б.2 - Лабораторний штатив
1 - підставка; 2. - муфта; 3 - стержень; 4 - тримач; 5 - гвинт тримача; 6 - кільце.
