
- •Методи вимірювання параметрів навколишнього середовища
- •1. Сучасні екологічні дослідження і їх комплексний характер
- •2. Екологічний моніторинг і його елементи
- •3. Процедури і операції технологічного циклу екоаналітичного контролю забруднення навколишнього середовища
- •Питання для самоконтролю
- •Методи контролю за станом навколишнього середовища основні вимоги до методів і засобів екоаналітичного контролю
- •1. Основні вимоги до методів і засобів екоаналітичного контролю
- •1.1. Вимоги до результатів екоаналітичних робіт
- •1.2. Вимоги до засобів вимірювань
- •1.3. Вимоги до допоміжного обладнання
- •1.4. Вимоги до випробувального обладнання
- •1.5. Вимоги до засобів метрологічного забезпечення
- •1.6. Вимоги до методик виконання вимірювань
- •1.7. Вимоги до засобів пробовідбору
- •1.8. Вимоги до технічної компетентності екоаналітичних лабораторій
- •Питання для самоконтролю
- •Класифікація і основні характеристики екоаналітичних засобів
- •Питання для самоконтролю
- •Сучасні методи дослідження стану навколишнього середовища
- •1. Якісний аналіз стану довкілля
- •Питання для самоконтролю
- •2. Кількісні методи аналізу
- •Методи визначення деяких хімічних інгредієнтів у
- •2.1. Хімічні методи
- •2.2. Фізико - хімічні методи
- •Колориметрія
- •Фотоколориметрія
- •Спектрофотометрія
- •Фотоколориметри
- •Фотоколориметр кфк - 2
- •Спектрофотометри
- •Спектрофотометр сф – 46
- •Спектрофотометр сф – 14
- •Молекулярна спектроскопія
- •Рефрактометрія. Рефрактометри
- •Поляриметрія. Прилади для поляриметричних вимірювань Поляриметрія
- •Прилади для поляриметричних вимірювань
- •Стилоскопи
- •Потенціометрія
- •Потенціометри і рН-метри
- •Кондуктометрія
- •Вольтамперомерометрія (полярографія)
- •Прилади для кулонометричних вимірювань
- •Кулонометрія при постійному контрольованому потенціалі
- •Кулонометрія при постійній контрольованій силі струму (кулонометричне титрування)
- •Електролізери
- •Хроматографічний аналіз
- •Питання для самоконтролю
- •Використана література Основна
- •Допоміжна
Вольтамперомерометрія (полярографія)
Метод полярографії грунтується на вимірюванні величини струму, який виникає при відновленні або окисненні речовин на електродах. Якщо в розчин з речовиною занурити ртутний капельний електрод і електрод порівняння і накласти на них постійний потенціал (на Нg), поступово підвищуючи його від 0 до -2 В, то при певному потенціалі на ртутному електроді починається електрохімічне відновлення речовини. Струм, що протікає через комірку, при цьому збільшується (фарадеївський струм) до повного відновлення йонів речовини в біля електродному шарі. Потім струм стабілізується і його величина визначається швидкістю дифузії йонів з розчинів до електроду і їх концентрацією (дифузний струм) (рис. 2.34).
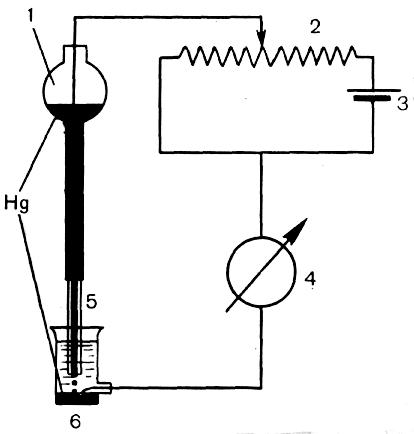
Рис. 2.34. Схема полярографічної установки
1 - балон з ртуттю; 2 - реостат; 3 - батарея; 4 - реєстратор струму;
5 - електрод; 6 – полярографічна комірка
Ділянка, на якій відбувається зростання струму, називається полярографічною хвилею. Положення полярографічної хвилі на полярограмі характеризується потенціалом середньої точки хвилі і називається потенціалом напівхвилі Е1/2. Кожна полярографічно активна речовина внаслідок своїх структурних особливостей відновлюється (або окиснюється) при певній величині Е1/2. Потенціал напівхвилі речовини змінюється в залежності від типу електроліта, в якому розчинена речовина, рН середовища, матеріалу електрода. При полярографуванні суміші речовин на полярограмах спостерігається декілька напівхвиль (рис. 21).
Висота хвилі h (величина струму І) пропорційна концентрації речовини С:
І = k ∙ С
Чим більша концентрація речовини, тим більша висота хвилі (більший струм). Потенціали, при яких проходять ці процеси, відрізняються від рівноважних (стандартних) потенціалів. Це явище називається поляризацією електродів, у зв'язку з чим метод називається полярографією. Поляризація виникає на електродах з малою поверхнею, через яку проходять значні струми. Це змінює потенціал електрода.
Полярографічний аналіз проводять на спеціальних приладах - полярографах, які складаються із полярографічної комірки, приєднаної до пристрою для подачі потенціалу і реєстратора. Полярографічна комірка (див. рис. 2.34) являє собою скляну посудину з розчином електроліту (фоновий розчин) в якому розчинено речовину. У комірку введені два електроди – робочий з малою поверхнею і електрод порівняння з великою поверхнею. В якості робочого використовують звичайно ртутний крапельний електрод, який має постійно чисту малу поверхню, що сприяє збільшенню поляризації електрода і більш чіткому спостереженню полярограм. В якості електрода порівняння в полярографії застосовують хлорсрібний, каломельний або інший електрод з великою поверхнею, часто - шар ртуті на дні комірки.
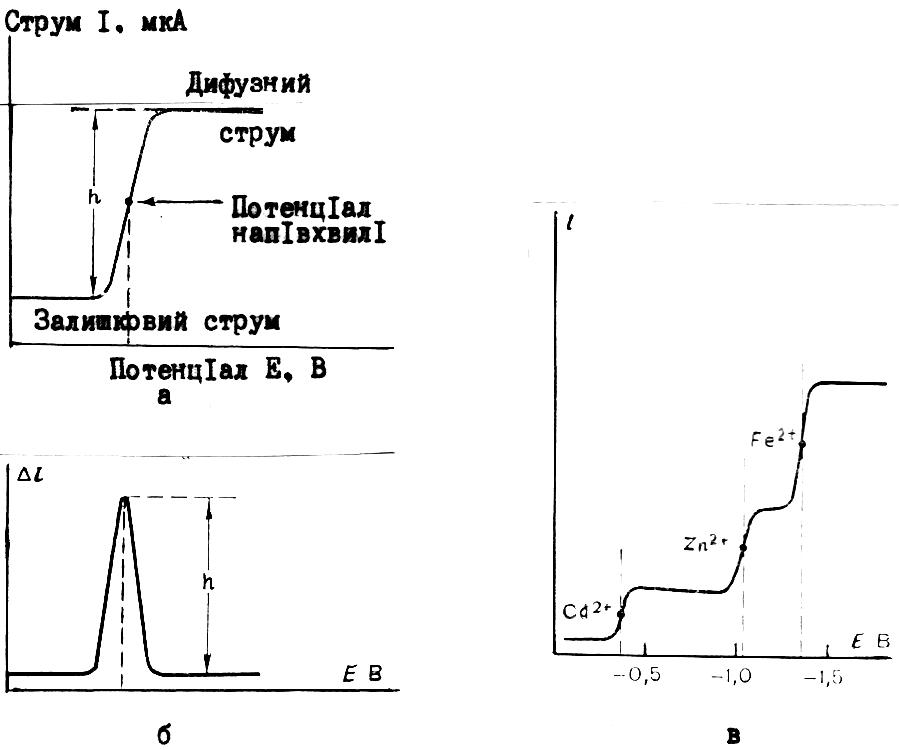
Рис. 2.35. Полярограми
а – полярографічна хвиля (h – висота хвилі); б – диференціальна полярограма;
в – полярограма суміші катіонів
Розчини речовин, які піддають полярографічному аналізу, готують на буферних розчинах або на розчинах електролітів, які відновлюються при високих потенціалах (-1,7В і вище). Це забезпечує високу електропровідність розчину і виключає вплив його опору, що дозволяє реєструвати на приладі тільки електродні процеси.
Ртутний капельний електрод працює в межах Е1/2 від + 0,2 ÷ 0,4 В до - 1,7 ÷ - 2,5 В. На ньому визначають тільки полярографічно активні речовини, які відновлюються при Е1/2 від 0 до - 1,7 ÷ - 2,5 В або окиснюються при Е1/2 до + 0,2 ÷ + 0,4 В. Визначенню речовин з потенціалом відновлення більше - 1,7 ÷ - 2,5 В заважає хвиля відновлення фонового електроліту. Речовини окиснення з потенціалом окиснення вище + 0,2 ÷ 0,4 В на ртутному електроді не визначають внаслідок виникнення електроокиснення ртуті (Нg0→Hg22+→Hg2+). Потенціали напівхвиль деяких йонів мають значення: Fе2+, Е1/2 = - 1,3 В (в 0,1 н. КCІ, Fе2+→ Fе0); Fе3+, Е1/2 = - 0,44 В (в 1 М (NН4)2СO3, Fе3+→ Fе2+); Мn2+, Е1/2 = - 1,51 В (в 1 н. КСІ, Мn2+→ Мn0).
Кількісне визначення речовини полярографічним способом проводять за калібрувальним графіком залежності величини дифузного струму від концентрації. Калібрувальний графік будують за серією стандартних розчинів. Крім цього, використовують метод добавок, при цьому прирощення висоти хвилі ∆h пропорційне прирощенню концентрації розчину при добавці певної кількості речовини: ∆h / h = ∆С/С.
В якості фонових електролітів звичайно застосовують водні розчини КСІ, NаСІ, LiСІ, буферні розчини (боратний, ацетатний). Перед проведенням полярографічного аналізу необхідно підібрати відповідний фоновий електроліт (середовище) і умови полярографії.
Інколи застосовують диференціальний варіант класичної полярографії що має більший діапазон вимірювання. На полярографі при цьому записується диференціальна полярограма, яка являє собою графічне відображення залежності прирощення струму ∆І від потенціалу і має вигляд піка, місцезнаходження якого характеризує деполяризатор (речовина), а висота або площа - кількість речовини. Замість ртутного електрода в полярографії знайшли застосування тверді електроди-платинові або графітові. Для полегшення надходження розчину до електрода використовують обертаючі тверді електроди або перемішують розчин.
Найширше в кількісному полярографічному аналізі застосовується метод градуювального графіка на основі рівняння Ільковича:
![]()
де,
![]() -
величина дифузійного струму;
-
величина дифузійного струму;
![]() -
концентрація йонів
-
концентрація йонів
Графік будують за даними полярографування декількох стандартних розчинів. На осі ординат відкладається пропорційна силі дифузійного струму висота полярографічної хвилі, а по осі абсцис – концентрація аналізованої речовини. Відповідно до рівняння Ільковича градуювальний графік повинен являти собою пряму лінію, що проходить через початок координат. Метод дає точні результати за умови строгої ідентичності умов полярографування стандартних розчинів і невідомої проби. До умов полярографування відносять умови роботи капіляра, температуру і середовище (фоновий електроліт). Метод градуювального графіка є найбільш трудомістким, але і найбільш точним.
При
аналізі деяких добре вивчених систем,
для яких застосовність рівняння Ільковича
встановлена цілком надійно,
часто застосовується менш трудомісткий
метод
стандартних розчинів.
У цьому методі в строго однакових умовах
записують полярограми|
стандартного і аналізованого розчинів
і з пропорції, основаної на рівнянні
Ільковича, розраховують невідому
концентрацію
![]() :
:
![]()
де сст - концентрація стандартного розчину;
hx| і hст - висота хвилі при полярографуванні| відповідно аналізованого і стандартного розчинів.
Метод використовується також тільки в умовах строгої стандартизації умов полярографування|.
Великими можливостями і високою чутливістю володіє осцилографічна полярографія, яка грунтується на подачі на комірку пильчастих змін напруги і реєстрації полярограми на екрані осцилографа. При цьому полярограма знімається в певний момент життя ртутної каплі.
У методі диференціальної осцилографії на екрані осцилографа реєструється залежність прирощення струму ∆І від потенціалу Е. Розвивається метод полярографії змінного струму, в якому на комірку подається лінійно змінний потенціал, модульований невеликими (30 мВ) імпульсами різної форми.
Полярографічний аналіз, що базується на процесі електролізу і вивченні залежності сили струму від прикладеної напруги, застосовується для визначення цим методом у природних водах і грунтах вмісту цинку, кадмію, плюмбуму, купруму; з попереднім екстракційним відділенням токсичних елементів - залишкову кількість плюмбуму у виноградному соці з чутливістю 0,002 мг/л; токсичні елементи в продуктах, повітрі, стічних водах; користуються і для визначення концентрації вітамінів, ферментів, гормонів в організмі людини, для діагностики захворювань.
Вольтамперометричні методи широко застосовуються при аналізі металів, катіонів і аніонів, органічних сполук і лікарських препаратів.
Методами абсорбційної інверсійної вольтамперометрії визначають понад 40 катіонів металів, численні аніони, органічні сполуки (білки, ферменти, лікарські препарати, пестициди, стимулятори росту тварин, комплексони) в різних екологічних об'єктах.
