
- •1.1. Атомно-молекулярная теория строения вещества
- •1.2. Масса и размеры молекул
- •1.3. Броуновское движение
- •2. Газовые законы. Идеальный и реальный газы
- •2.1. Законы Бойля-Мариотта, Гей-Люссака, Шарля
- •2.2. Уравнение состояния идеального газа
- •2.3. Плотность газов
- •2.4. Основное уравнение молекулярно-кинетической теории газов
- •2.5. Постоянная Больцмана
- •3.1. Длина свободного пробега молекул
- •3.2. Скорость газовых молекул
- •3.3. Распределение Максвелла
- •4.1. Предмет термодинамики. Постулаты термодинамики
- •4.2. Температурные шкалы. Абсолютная температура
- •4.3. Температура в молекулярно-кинетической теории
- •4.3. Температура в молекулярно-кинетической теории
- •4.4. Внутренняя энергия. Работа. Теплота
- •4.5. Первое начало термодинамики.Понятие теплоемкости
- •4.6. Применение первого начала термодинамики к описанию изопроцессов в идеальном газе
- •4.7. Первое начало термодинамики как принцип эквивалентности теплоты и работы
- •4.8. Невозможность вечного двигателя первого рода
- •4.9. Принципы работы тепловых машин
- •4.10. Цикл карно. Кпд тепловых двигателей
- •4.11. Обратимые и необратимые процессы
- •4.12. Второй закон термодинамики
- •4.13. Теорема карно
- •4.14. Энтропия. Неравенство клаузиуса. Математическое выражение второго начала термодинамики
- •4.15. Статистический смысл второго начала термодинамики
- •4.16. Энтропия и термодинамическая вероятность. Формула больцмана
- •4.17. Энтропия и беспорядок
- •4.18. О "тепловой смерти" вселенной
- •5.1. Кристаллическая решетка
- •5.2. Дефекты в кристаллах
- •5.3. Плавление и кристаллизация
- •5.4. Зависимость температуры плавления от давления
- •5.5. Испарение твердых тел (сублимация)
- •5.6. Механические свойства твердых тел
- •6.1. Силы взаимодействия между молекулами. Агрегатные состояния вещества
- •6.2. Особенности строения и теплового движения в жидкостях
- •6.3. Свойства жидкостей
- •6.4. Явления на границе жидкость–пар. Насыщенный пар
- •6.5. Кипение жидкости. Зависимость температуры кипения от давления
- •6.6. Равновесие двухфазного состояния жидкость-пар. Критическая температура
- •6.7. Водяной пар в атмосфере. Влажность
- •6.8. Поверхностное натяжение
- •6.9. Давление Лапласа под искривленной поверхностью жидкости
- •6.10. Капиллярные явления. Формула Жюрена
- •6.11. Смачивание и несмачивание на границе жидкость-жидкость и твердое тело-жидкость
- •6.12. Текучесть жидкости. Сверхтекучесть гелия
6.5. Кипение жидкости. Зависимость температуры кипения от давления
Непосредственные наблюдения за поведением жидкости свидетельствуют, что при некоторых температуре и давлении в жидкостях начинается процесс кипения. Разберемся в механизме этого явления.
Обычно в жидкости или на стенках сосуда, в котором она находится, присутствуют пузырьки растворенного в ней воздуха. При нагревании жидкости растворимость содержащихся в ней газов понижается. В результате число таких пузырьков значительно увеличивается. Газовые пузырьки в процессе закипания играют роль аналогичную той, которую играют ионы или пылинки при конденсации. В эти пузырьки происходит испарение окружающей их жидкости, вследствие чего пузырьки наполняются насыщенным паром, давление которого с повышением температуры увеличивается.
Пока температура жидкости такова, что
давление насыщенного пара внутри
пузырька меньше внешнего давления над
жидкостью, пузырек не может расти. При
некоторой температуре давление
насыщенного пара внутри пузырька
становится равным давлению, оказываемому
на пузырек извне. Это давление равно
сумме атмосферного давления,
гидростатического давления, обусловленного
столбом жидкости над пузырьком и
дополнительного давления, связанного
с кривизной поверхности пузырька
(давление Лапласа). Расчеты показывают,
что вклад гидростатического давления
и давления Лапласа существенной роли
в этом процессе не играют. Чаще всего
мы имеем дело с процессом кипения при
нормальном атмосферном давлении
![]() ,
а для того чтобы гидростатическое
давление вносило вклад, сравнимый с
давлением атмосферы, столб воды должен
составлять хотя бы несколько метров,
чего обычно в реальной ситуации не
бывает. Давление Лапласа существенно
тогда, когда радиус пузырьков порядка
,
а для того чтобы гидростатическое
давление вносило вклад, сравнимый с
давлением атмосферы, столб воды должен
составлять хотя бы несколько метров,
чего обычно в реальной ситуации не
бывает. Давление Лапласа существенно
тогда, когда радиус пузырьков порядка
![]() ,
что значительно меньше размеров
пузырьков, образующихся в процессе
кипения.
,
что значительно меньше размеров
пузырьков, образующихся в процессе
кипения.
При некоторой температуре, когда давление насыщенного пара внутри пузырьков становится равным внешнему давлению, точнее говоря, несколько больше, пузырьки, быстро увеличиваясь в размерах, устремляются вверх и прорываются наружу. С этого момента жидкость начинает кипеть.
Рассмотрев механизм закипания жидкости, подчеркнем, что кипение существенно отличается от испарения. Во-первых, испарение происходит при любой температуре, кипение же для каждой жидкости при определенном давлении имеет место при строго определенной температуре, называемой точкой кипения. Если процесс кипения начался, температура жидкости, несмотря на продолжающееся сообщение теплоты, не повышается. Она так и останавливается на точке кипения до тех пор, пока не выкипит вся жидкость. Во-вторых, в процессе кипения жидкость испаряется не только с поверхности, но и с поверхности пузырьков внутри жидкости.
Итак, для того, чтобы жидкость закипела, нужно довести ее температуру до такого значения, при котором давление насыщенного пара внутри содержащихся в жидкости пузырьков хотя бы чуточку превышало внешнее давление.
Из приведенных рассуждений видно, что с уменьшением внешнего давления должна понижаться и температура кипения жидкости.
Принято считать, что точке кипения воды при нормальном атмосферном давлении соответствует температура 100º С. Однако жителям высокогорных селений хорошо известен факт закипания воды при значительно более низкой температуре. Так на вершине Эльбруса вода закипает уже при 82º С. Физическим фактором, ответственным за изменение температуры кипения, является уменьшение внешнего давления в высокогорных районах. Вода кипит при 100º С только при давлении 760 мм Hg. При давлении 0,5 атм она закипает при 82º С, а при давлении 10-15 мм Hg вода закипает в интервале температур 10-15º С. Можно получить даже "кипяток", имеющий температуру замерзающей воды. Для этого придется понизить внешнее давление до 4,6 мм Hg.
Интересный результат можно наблюдать, если в колбу поместить небольшое количество воды при комнатной температуре и начать откачивать из колбы воздух. Исход опыта зависит от скорости откачки. Если откачка производится достаточно медленно, то вода должна рано или поздно закипеть. Если же откачка производится достаточно быстро, то вода, напротив, замерзает. В результате откачки воздуха, а вместе с ним и паров воды, усиливается процесс испарения, в ходе которого вода остывает. При медленной откачке понижение температуры жидкости компенсируется за счет поступления теплоты извне, поэтому температура вода остается постоянной. Если же откачка производится быстро, то вода не успевает получить тепло от окружающей среды. Так как температура воды начинает понижаться, возможность ее закипания также уменьшается. Дальнейшее продолжение быстрой откачки воздуха из колбы со временем приведет к понижению температуры жидкости до точки замерзания.
Отмечая факт понижения температуры кипения с уменьшением давления, естественно ожидать, что с повышением давления температура кипения будет повышаться. Действительно, при давлении 15 атм кипение воды начинается при 200º С, а давление в 80 атм вызывает кипение воды даже при 300º С.
|
Отметим еще, что кривая равновесия жидкость-пар качественно имеет один и тот же вид для различных жидкостей. Во всех случаях упругость пара быстро растет с повышением температуры.
Это интересно

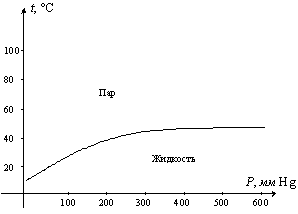 Рис.
6.6
Рис.
6.6