
- •1.1. Атомно-молекулярная теория строения вещества
- •1.2. Масса и размеры молекул
- •1.3. Броуновское движение
- •2. Газовые законы. Идеальный и реальный газы
- •2.1. Законы Бойля-Мариотта, Гей-Люссака, Шарля
- •2.2. Уравнение состояния идеального газа
- •2.3. Плотность газов
- •2.4. Основное уравнение молекулярно-кинетической теории газов
- •2.5. Постоянная Больцмана
- •3.1. Длина свободного пробега молекул
- •3.2. Скорость газовых молекул
- •3.3. Распределение Максвелла
- •4.1. Предмет термодинамики. Постулаты термодинамики
- •4.2. Температурные шкалы. Абсолютная температура
- •4.3. Температура в молекулярно-кинетической теории
- •4.3. Температура в молекулярно-кинетической теории
- •4.4. Внутренняя энергия. Работа. Теплота
- •4.5. Первое начало термодинамики.Понятие теплоемкости
- •4.6. Применение первого начала термодинамики к описанию изопроцессов в идеальном газе
- •4.7. Первое начало термодинамики как принцип эквивалентности теплоты и работы
- •4.8. Невозможность вечного двигателя первого рода
- •4.9. Принципы работы тепловых машин
- •4.10. Цикл карно. Кпд тепловых двигателей
- •4.11. Обратимые и необратимые процессы
- •4.12. Второй закон термодинамики
- •4.13. Теорема карно
- •4.14. Энтропия. Неравенство клаузиуса. Математическое выражение второго начала термодинамики
- •4.15. Статистический смысл второго начала термодинамики
- •4.16. Энтропия и термодинамическая вероятность. Формула больцмана
- •4.17. Энтропия и беспорядок
- •4.18. О "тепловой смерти" вселенной
- •5.1. Кристаллическая решетка
- •5.2. Дефекты в кристаллах
- •5.3. Плавление и кристаллизация
- •5.4. Зависимость температуры плавления от давления
- •5.5. Испарение твердых тел (сублимация)
- •5.6. Механические свойства твердых тел
- •6.1. Силы взаимодействия между молекулами. Агрегатные состояния вещества
- •6.2. Особенности строения и теплового движения в жидкостях
- •6.3. Свойства жидкостей
- •6.4. Явления на границе жидкость–пар. Насыщенный пар
- •6.5. Кипение жидкости. Зависимость температуры кипения от давления
- •6.6. Равновесие двухфазного состояния жидкость-пар. Критическая температура
- •6.7. Водяной пар в атмосфере. Влажность
- •6.8. Поверхностное натяжение
- •6.9. Давление Лапласа под искривленной поверхностью жидкости
- •6.10. Капиллярные явления. Формула Жюрена
- •6.11. Смачивание и несмачивание на границе жидкость-жидкость и твердое тело-жидкость
- •6.12. Текучесть жидкости. Сверхтекучесть гелия
5.3. Плавление и кристаллизация
Нет такого твердого тела, которое сколько угодно долго противостояло бы повышению температуры. Рано или поздно твердый кусочек превращается в жидкость. Почему?
По мере возрастания температуры молекулы движутся все интенсивнее. При нагревании возрастает не только молекулярно-кинетическая энергия тела, но и потенциальная энергия взаимодействия его атомов, поскольку при увеличении амплитуды колебаний атомы отходят друг от друга на большее расстояние и сближаются на меньшее расстояние, благодаря чему энергия взаимодействия их электрических зарядов возрастает. С повышением температуры наступает, наконец, такой момент, когда поддержание порядка среди сильно раскачивающихся атомов становится невозможным, и с этого момента начинается разрушение кристаллической решетки, в результате чего исчезает и дальний порядок. Твердое тело плавится. Ниже приводятся температуры плавления некоторых веществ (таблица 5.3).
Таблица 5.3
Вещество |
Точка плавления, °С |
Вещество |
Точка плавления, °С |
Лед |
0 |
|
|
Вольфрам |
3380 |
Цинк |
419 |
Золото |
1063 |
Свинец |
327 |
Железо |
1535 |
Олово |
232 |
Медь |
1083 |
Ртуть |
–39 |
Пока плавление не началось, температура тела при нагревании растет. Как только температура плавления будет достигнута, начинается плавление, повышение температуры прекращается, и температура остается неизменной, пока процесс плавления не закончится полностью. При дальнейшем повышении температуры расплав нагревается как однородная жидкость. Описанные изменения температуры в процессе нагревания тела в зависимости от времени представлены на рис. 5.8.
|
Обратный переход вещества в твердое состояние возможен как из жидкого, так и из газообразного состояния. И в том и в другом случае такой переход осуществляется из состояния, лишенного симметрии, в состояние, в котором симметрия существует (это относится к дальнему порядку, который имеет место в кристаллах и которого нет ни в жидкостях, ни в газах). Поэтому переход в твердое состояние должен происходить скачком при определенной температуре, в отличие от перехода жидкость–пар, который может происходить непрерывно. Процесс образования твердого тела при охлаждении жидкости есть процесс образования кристалла (кристаллизация) и происходит он при определенной температуре – температуре кристаллизации. Так как при таком превращении энергия системы уменьшается, то такой переход должен сопровождаться выделением энергии в виде теплоты кристаллизации. Из закона сохранения энергии следует, что теплота плавления и теплота кристаллизации должны быть равны друг другу.
Процесс образования кристалла иллюстрируется на рис. 5.8 (кривая а). Участок 1 кривой а соответствует понижению температуры жидкости при отводе от нее тепла в процессе охлаждения. Горизонтальный участок 2 показывает, что при определенном значении температуры ее понижение прекращается, несмотря на то, что отвод тепла продолжается. Спустя некоторое время температура вновь начинает понижаться. Температура, соответствующая участку 2, и есть температура кристаллизации. Выделяющееся при кристаллизации тепло компенсирует отвод тепла от вещества, в результате чего понижение его температуры в процессе кристаллизации прекращается. После окончания процесса кристаллизации температура, теперь уже твердого тела, вновь начинает понижаться. Отметим еще, что для начала процесса кристаллизации большую роль играет присутствие в жидкой фазе центров кристаллизации.
Возможно образование кристалла непосредственно из пара. Такая возможность реализуется и в природе, когда мы любуемся деревьями, украшенными изморозью. При этом также выделяется скрытая теплота перехода, которая, однако, всегда больше скрытой теплоты плавления.
Проделайте опыт

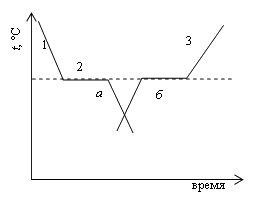 Рис.
5.8
Рис.
5.8