
- •1.1. Атомно-молекулярная теория строения вещества
- •1.2. Масса и размеры молекул
- •1.3. Броуновское движение
- •2. Газовые законы. Идеальный и реальный газы
- •2.1. Законы Бойля-Мариотта, Гей-Люссака, Шарля
- •2.2. Уравнение состояния идеального газа
- •2.3. Плотность газов
- •2.4. Основное уравнение молекулярно-кинетической теории газов
- •2.5. Постоянная Больцмана
- •3.1. Длина свободного пробега молекул
- •3.2. Скорость газовых молекул
- •3.3. Распределение Максвелла
- •4.1. Предмет термодинамики. Постулаты термодинамики
- •4.2. Температурные шкалы. Абсолютная температура
- •4.3. Температура в молекулярно-кинетической теории
- •4.3. Температура в молекулярно-кинетической теории
- •4.4. Внутренняя энергия. Работа. Теплота
- •4.5. Первое начало термодинамики.Понятие теплоемкости
- •4.6. Применение первого начала термодинамики к описанию изопроцессов в идеальном газе
- •4.7. Первое начало термодинамики как принцип эквивалентности теплоты и работы
- •4.8. Невозможность вечного двигателя первого рода
- •4.9. Принципы работы тепловых машин
- •4.10. Цикл карно. Кпд тепловых двигателей
- •4.11. Обратимые и необратимые процессы
- •4.12. Второй закон термодинамики
- •4.13. Теорема карно
- •4.14. Энтропия. Неравенство клаузиуса. Математическое выражение второго начала термодинамики
- •4.15. Статистический смысл второго начала термодинамики
- •4.16. Энтропия и термодинамическая вероятность. Формула больцмана
- •4.17. Энтропия и беспорядок
- •4.18. О "тепловой смерти" вселенной
- •5.1. Кристаллическая решетка
- •5.2. Дефекты в кристаллах
- •5.3. Плавление и кристаллизация
- •5.4. Зависимость температуры плавления от давления
- •5.5. Испарение твердых тел (сублимация)
- •5.6. Механические свойства твердых тел
- •6.1. Силы взаимодействия между молекулами. Агрегатные состояния вещества
- •6.2. Особенности строения и теплового движения в жидкостях
- •6.3. Свойства жидкостей
- •6.4. Явления на границе жидкость–пар. Насыщенный пар
- •6.5. Кипение жидкости. Зависимость температуры кипения от давления
- •6.6. Равновесие двухфазного состояния жидкость-пар. Критическая температура
- •6.7. Водяной пар в атмосфере. Влажность
- •6.8. Поверхностное натяжение
- •6.9. Давление Лапласа под искривленной поверхностью жидкости
- •6.10. Капиллярные явления. Формула Жюрена
- •6.11. Смачивание и несмачивание на границе жидкость-жидкость и твердое тело-жидкость
- •6.12. Текучесть жидкости. Сверхтекучесть гелия
5.2. Дефекты в кристаллах
Многие свойства твердых тел, имеющие большое практическое значение, зависят от того, в какой степени реальные твердые тела отличаются от тех идеальных структур, которые обязаны существованию в твердых телах дальнего порядка. В реальных кристаллах нельзя наблюдать тот безупречный порядок и строгую периодичность в расположении атомов, которая свойственна идеальному дальнему порядку, о чем свидетельствуют многочисленные экспериментальные исследования.
Прежде всего, необходимо отметить, что хотя атомы в кристаллической решетке располагаются в таких местах, которые соответствуют их равновесному положению, это, однако не значит, что они находятся в покое. Атомы в твердом теле, так же как в жидкостях и газах, совершают непрерывные тепловые движения. Эти движения имеют характер малых колебаний около положения равновесия, которое и является узлом решетки. Энергия этих колебаний определяет температуру тела. Амплитуда колебаний атомов даже при умеренных температурах может достигать нескольких процентов от межатомного расстояния, что приводит к заметному нарушению в периодической структуре решетки. Естественно, что с повышением температуры степень нарушения периодичности увеличивается. Такие тепловые нарушения в структуре твердых тел существуют всегда. Они представляют собой фон, на котором разыгрываются все явления в кристаллах. Этим объясняется то, что практически все свойства кристаллов так или иначе зависят от температуры.
Кроме нарушений периодичности, которые обусловлены тепловым движением атомов, в кристаллических телах присутствуют и другие структурные нарушения порядка, которые принято называть дефектами. Часть дефектов может возникнуть из-за присутствия в кристаллах инородных атомов. Даже наиболее чистые химические элементы, примесь в которых не превышает 10–7 %, содержит в 1 см3 примерно 1013 примесных атомов.
В зависимости от природы и количества примесей они могут находиться в кристалле или в растворенном состоянии, или в виде более или менее крупных включений. Процесс растворения состоит в том, что примесные атомы внедряются в промежутки между атомами кристалла или замещают часть этих атомов, размещаясь в узлах решетки.
|
В первом случае твердый раствор называется раствором внедрения (рис. 5.3а), во втором случае – раствором замещения (рис. 5.3б).
Примеси могут оказывать существенное влияние на химические, оптические, магнитные и механические свойства твердых тел. Так изменение концентрации мышьяка в германии всего на 1 % может изменить величину электропроводности германия на несколько порядков – вся транзисторная техника зависит от подобных явлений. Именно поэтому некоторые примеси вводятся в кристаллы преднамеренно.
|
Как атомы в междоузлии, так и вакансии не остаются локализованными в одном месте и диффундируют в решетке. Атом, покинувший свое место, путешествует по решетке, переходя из одного междоузлия в другое. Диффузия вакансии осуществляется путем последовательного эстафетного заполнения ее соседними атомами, как это представлено на рис. 5.4.
Помимо внутреннего "испарения" возможно полное или частичное "испарение" атомов с поверхности кристалла. При полном "испарении" атом покидает поверхность кристалла и переходит в пар (рис. 5.5а). При частичном "испарении" атом переходит с поверхности в положение над поверхностью, в котором удерживается одним своим нижним соседом (рис. 5.5б).
|
Атом, находящийся внутри кристалла, имеет шесть ближайших соседей (левый, правый, верхний, нижний, передний, задний). У атома в поверхностном слое кристалла только пять связей (верхняя связь уходит). Для атома, совершившего частичное "испарение", осталось четыре связи (из пяти осталась одна связь с нижним соседом). Поэтому если через Е обозначить энергию связи атома с одним из его соседей, то для полного "испарения" требуется энергия 5Е, для частичного – 4Е. Еще большая энергия требуется для внутреннего "испарения", поскольку внутри кристалла атом окружен шестью соседями. Ясно поэтому, что вероятность внутреннего "испарения" будет меньше не только вероятности полного, но и частичного "испарения".
При полном и частичном "испарении" атомов в поверхностном слое кристалла образуется вакансия. Эта вакансия замещается глубже лежащим атомом. Посредством этого механизма осуществляется процесс диффузии вакансии по кристаллу. Существенно, что появление таких вакансий не сопровождается одновременным внедрением атомов в междоузлия. Такого рода вакансии называются дефектами Шотки.
Подчеркнем, что концентрация дефектов в кристалле зависит, прежде всего, от температуры, так как с повышением температуры увеличивается число атомов, энергия которых оказывается достаточной для преодоления связи с соседями и образования дефекта.
|
Помимо линейных дислокаций в кристаллах существуют искажения иного вида, известные в литературе под названием винтовых дислокаций, на описании которых останавливаться не будем.
|
Наиболее существенна роль дислокаций в процессе роста и деформации кристаллов. Присутствие дислокаций в твердом теле уменьшает его прочность. Дислокационная теория пластической деформации исходит из предположения о том, что процесс скольжения начинается всегда в местах нарушения структуры кристалла и распространяется по плоскости сдвига путем последовательного перемещения этого искажения до выхода на поверхность.
В настоящее время благодаря хорошо разработанным экспериментальным методам удается проводить прямые наблюдения за поведением дислокаций, в том числе и за выходом дислокаций на поверхность кристалла. Достигается это методом электролитической полировки и травления. При травлении поверхности кристалла в первую очередь протравливаются участки, в которых решетка искажена наиболее сильно, так как атомы этих участков обладают избыточной энергией и химически более активны. Такими участками как раз являются места выхода дислокаций на поверхность кристалла.
Хорошо известно, что наличие структурных искажений приводит к значительному снижению прочностных свойств материалов. Поэтому перед наукой давно встала задача создания бездефектных кристаллов. В последнее время в этом направлении достигнуты определенные результаты – получены тонкие нитевидные кристаллы, обладающие идеальной внутренней структурой. Их часто называют "усами". Толщина усов колеблется обычно от 0,05 до 2 мк, длина – от 2-3 мм до 10 мм. Замечательным свойством таких кристаллов является их исключительно высокая прочность, близкая к теоретической величине. Для сравнения приводим значения пределов прочности для материалов в обычном состоянии и для нитевидных кристаллов (таблица 5.2).
Таблица 5.2
|
Обычные кристаллы σпр·10–8 Н/м2 |
Нитевидные кристаллы σпр·10–10 Н/м2 |
Железо |
3,000 |
1,336 |
Медь |
2,600 |
0,300 |
Цинк |
1,800 |
0,225 |

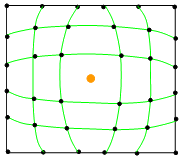
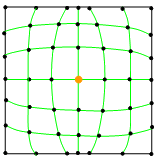 Рис.
5.3
Рис.
5.3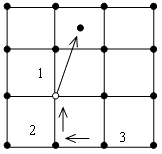 Рис.
5.4
Рис.
5.4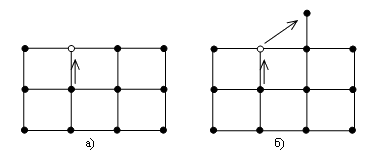 Рис.
5.5
Рис.
5.5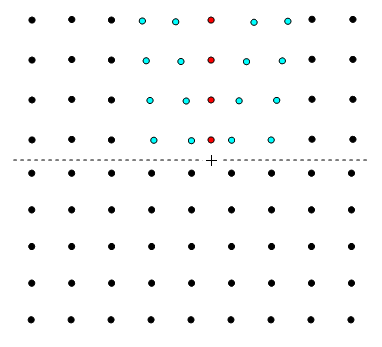 Рис.
5.6
Рис.
5.6 Рис.
5.7
Рис.
5.7