
- •5. Катализ: гомогенный и гетерогенный. Энергетический профиль каталитической реакции.
- •6. Химическое равновесие. Обратимые и необратимые по направлению реакции. Константа химического равновесия. Прогнозирование смещения химического равновесия.
- •8. Классификация дисперсных систем: по степени дисперсности, по агрегатному состоянию фаз, по силе межмолекулярного взаимодействия между дисперсной фазой и дисперсионной средой.
- •10. Осмос, осмотическое давление. Закон Вант-Гоффа. Осмоляльность и осмолярность биологических жидкостей.
- •11. Понятие о коллоидных растворах. Методы получения и очистки коллоидных растворов. Строение мицеллы. Коагуляция, порог коагуляции.
- •12. Факторы устойчивости коллоидных растворов. Механизм возникновения электрического заряда коллоидной частицы. Мицелла. Ядро. Гранула.
- •13. Ионное произведение воды. Методы определения pH растворов. Индикаторы.
- •Методы определения значения pH
- •14. Протолитические реакции. Понятия о кислотах и основаниях. Амфолиты. Ионизация слабых кислот и оснований. Константа кислотности и основности.
- •15. Буферные системы: определение, классификация, уравнение Гендерсона-Гассельбаха. Механизм действия буферных систем. Зона буферного действия и буферная емкость
- •16. Буферные системы крови: гидрокарбонатная, фосфатная, гемоглобиновая, белковая. Взаимодействие буферных систем организма человека.
- •17. Понятие о кислотно-основном состоянии организма. Виды нарушений кос и способы коррекции.
- •18. Типы окислительно-восстановительных реакций, протекающих в организме.
- •19. Физико-химические принципы транспорта электронов в электронотранспортной цепи митохондрий.
- •20. Классификация комплексных соединений, их строение. Представление о строении металлоферментов и других биокомплексных соединений (гемоглобин, цитохромы, кобаламины).
- •21. Типы изомерии органических соединений.
- •1.Структурная изомерия.
- •2.Пространственная изомерия.
- •22. Многоатомные спирты: этиленгликоль, глицерин, инозит. Их структура и функции. Образование сложных эфиров с неорганическими кислотами (нитроглицерин, фосфаты глицерина, инозита).
- •24. Аминофенолы: дофамин, норадреналин, адреналин. Понятие о биологической роли этих соединений и их производных.
- •26. Насыщенные дикарбоновые кислоты: щавелевая, малоновая, янтарная, глутаровая. Соли щавелевой кислоты- оксалаты.
- •27. Ненасыщенные дикарбоновые кислоты: фумаровая, малеиновая, их пространственное строение. Превращение янтарной кислоты в фумаровую как пример биологической реакции дегидрирования.
- •30. Классификация углеводов (моно-, олиго-, полисахариды). Моносахариды, их классификация (альдозы, кетозы).
- •31. Изомерия моносахаридов: стереоизомерия, цикло-оксо-таутомерия, а- и в-аномерия на примере глюкозы.
- •34. Дисахариды: классификация (редуцирующие- мальтоза, целлобиоза, лактоза) и нередуцирующие (сахароза, трегалоза). Строение, химические свойства: гидролиз, окисление редуцирующих сахаров.
- •35. Классификация полисахаридов (гомо- и гетерополисахариды). Примеры.
- •36. Гомополисахариды: крахмал (амилоза и амилопектин), гликоген, декстран, целлюлоза. Структура, типы, химических связей, гидролиз.
- •37. Липиды: определение, классификация.
- •39. Простые (нейтральные липиды) – триглицериды. Номеклатура, состав, строение, их гидролиз.
- •40. Фосфатидная кислота. Её образование и гидролиз.
- •41.Фосфолипиды: фосфатидилсерины, фосфатидилэтаноламины и фосфатидилхолин (лецитины) – реакция гидролиза.
- •42.Стероиды: структура холестерина, желчных кислот.
- •43.Липидный состав мембран. Амфифильная природа мембранных липидов.
- •44.Классификация нуклеиновых кислот.
- •45.Пиримидиновые и пуриновые основания. Ароматические свойства. Лактим-тактамная таутометрия.
- •46.Нуклеозиды: номенклатура, строение, гидролиз.
- •47. Нуклеотиды: номенклатура, строение, гидролиз
- •48.Первичная структура нуклеиновых кислот: химический состав рнк и днк, типы химических связей.
- •49.Вторичная структура днк. Роль водородных связей в формировании вторичной структуры. Комплиментарные пары. Третичная структура днк.
- •50.Природные аминокислоты.Номенклатура и стереоизомерия.
- •51.Классификация аминокислот по: строению радикала, кислотно-основным свойствам.
- •52.Кислотно-основные свойства аминокислот, биполярная структура, изоэлектрическая точка.
- •53.Химические свойства α-аминокислот как гетерофункциональных соединений: реакции этерификации, ацилирования, алкилирования, образование иминов, реакция комплексообразования.
- •5,4. Биологические важные реакции α-аминокислот
- •55. Первичная структура белка. Строение пептидной группы. Гидролиз пептидов.
- •56. Вторичная, третичная, четвертичная структуры белка. Химические связи, участвующие в образовании структур белка. Биологическая роль структурной организации белковых молекул.
- •59. Миоглобин и гемоглобин: строение и функции.
- •60. Конформационные изменения и кооперативные взаимодействия субъединиц гемоглобина (кооперативный эффект). Эффект Бора. Роль 2,3 – бисфосфоглицерата.
- •61. Особенности ферментов как белковых катализаторов. Активный центр, кофакторы и коферменты. Механизм действия ферментов. Этапы ферментативного катализа.
- •62. Классификация и номенклатура ферментов.
- •64. Зависимость активности ферментов от температуры и pH среды. Единицы активности ферментов.
- •65. Специфичность действия ферментов.
- •66. Аллостерические ферменты: структура, аллостерический и регуляторный центры. Гомо- и гетеротропные эффекты.
- •67. Ингибирование активности ферментов: обратимое, необратимое, конкурентное, неконкурентное.
- •I. Обратимое ингибирование
- •68. Индукция и репрессия синтеза ферментов. Компартментация ферментов. (Нихуя не нашел толком. Говно, а не ответ)
- •69. Виды регуляции ферементов: ассоциация-диссоциация.
- •70. Ковалентная модификация ферментов: ограниченный протеолиз проферментов, фосфорилирование и дефосфорилирование.
- •71. Применение ферментов и их ингибиторов в медицине (диагностика, лечение). Энзимопатии.
47. Нуклеотиды: номенклатура, строение, гидролиз
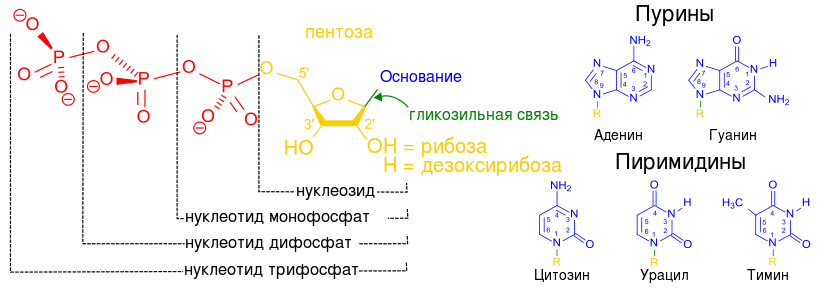 Нуклеотиды
(нуклеозидфосфаты) - эфиры фосфорной
кислоты и нуклеозидов по одному или
нескольким. гидроксилам остатка
моносахарида;
в более широком смысле - соединения, в
которыхрых моносахаридный остаток
нуклеозида или его неприродного аналога
этерифицирован одной или несколькими
моно- или олигофосфатными группами. В
зависимости от природы нуклеозида
различают рибо- и дезоксирибонуклеотиды,
пиримидиновые и пуриновые нуклеотиды.
Нуклеотиды
(нуклеозидфосфаты) - эфиры фосфорной
кислоты и нуклеозидов по одному или
нескольким. гидроксилам остатка
моносахарида;
в более широком смысле - соединения, в
которыхрых моносахаридный остаток
нуклеозида или его неприродного аналога
этерифицирован одной или несколькими
моно- или олигофосфатными группами. В
зависимости от природы нуклеозида
различают рибо- и дезоксирибонуклеотиды,
пиримидиновые и пуриновые нуклеотиды.
Номенклатура. Обычно используют сокращенные обозначения нуклеотидов. Напр., аденозин-5'-монофосфат, или адениловую к-ту, обозначают 5'-АМФ, или AMP; аденозин-5'-дифосфат - АДФ, или ADP; 2'-дезоксицитидин-5'-три-фосфат - дЦТФ, или dCTP.
Строение. Фосфатный остаток в нуклеотидах обычно образует сложноэфирную связь с 2'-, 3'- или 5'-гидроксильными группами рибонуклеозидов, в случае 2'-дезоксинуклеозидов этерифицируются 3'- или 5'-гидроксильные группы.
Большинство нуклеотидов являются моноэфирами ортофосфорной кислоты, однако известны и диэфиры нуклеотидов, в которых этерифицированы два гидроксильных остатка — например, циклические нуклеотиды циклоаденин- и циклогуанин монофосфаты (цАМФ и цГМФ). Наряду с нуклеотидами — эфирами ортофосфорной кислоты (монофосфатами) в природе также распространены и моно- и диэфиры пирофосфорной кислоты (дифосфаты, например, аденозиндифосфат) и моноэфиры триполифосфорной кислоты (трифосфаты, например, аденозинтрифосфат).
Гидролиз проходит в кислой среде по сложно-эфирной и гликозидной связям с получением азотистого основания, пентозы и фосфорной кислоты.
48.Первичная структура нуклеиновых кислот: химический состав рнк и днк, типы химических связей.
Первичная структура НК представляет собой последовательность нуклеотидов соединенные в непрерывную цепочку с помощью 3'-5'-ковалентных связей.
Ее определяют две характеристики:
Нуклеотидный состав – набор и соотношение нуклеотидов.
Нуклеотидная последовательность – порядок чередования нуклеотидных звеньев.
Нуклеотиды РНК состоят из сахара — рибозы, к которой в положении 1' присоединено одно из оснований: аденин, гуанин, цитозин или урацил. Фосфатная группа соединяет рибозы в цепочку, образуя связи с 3' атомом углерода одной рибозы и в 5' положении другой. Каждый нуклеотид ДНК состоит из остатка фосфорной кислоты, присоединённого по 5'-положению к сахару дезоксирибозе, к которому также через гликозидную связь (C—N) по 1'-положению присоединено одно из четырёх азотистых оснований: аденин, гуанин, цитозин или тимин.
49.Вторичная структура днк. Роль водородных связей в формировании вторичной структуры. Комплиментарные пары. Третичная структура днк.
 Вторичная
структура представляет собой две
параллельные неразветвленные
полинуклеотидные цепи, направленные в
противоположные стороны (3'→5' и 5'→3') и
закрученные вокруг общей оси в двойную
спираль.
Вторичная
структура представляет собой две
параллельные неразветвленные
полинуклеотидные цепи, направленные в
противоположные стороны (3'→5' и 5'→3') и
закрученные вокруг общей оси в двойную
спираль.
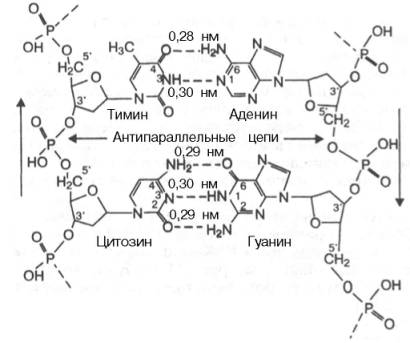
 Такая
пространственная структура удерживается
множеством водородных связей, образованных
азотистыми основаниями по принципу
комплиментарности, то есть Аденину
соответствует Тимин, а Цитозину –
Гуанин.
Такая
пространственная структура удерживается
множеством водородных связей, образованных
азотистыми основаниями по принципу
комплиментарности, то есть Аденину
соответствует Тимин, а Цитозину –
Гуанин.
Стабильность А–Т оснований обеспечивается двумя водородными связями, а пар Г–Ц – тремя, что в свою очередь определяется особенностями расположения функциональных групп азотистых оснований. Длина водородных связей между основаниями составляет около 0,3 нм.
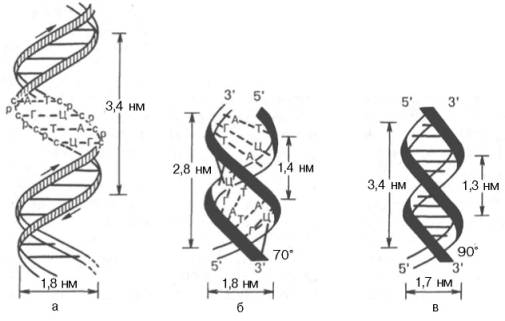
На модели ДНК видно, что расстояние между витками (шаг спирали) равно 3,4 нм. На этом участке укладываются 10 нуклеотид-ных остатков, размер одного нуклеотида составляет 0,34 нм; диаметр биспиральной молекулы равен 1,8 нм.
Третичная (кольцевая) структура ДНК у эукариотических клеток отличается тем, что многократная спирализация ДНК сопровождается образованием комплексов с белками.
Образование кольцевой формы молекулы ДНК у бактерий или в митохондриях клеток животных часто вызвано ковалентным соединением их открытых концов. Известно, что суперспиральная (суперскрученная) структура обеспечивает экономную упаковку огромной молекулы ДНК в хромосоме: вместо 8 см длины, которую она могла бы иметь в вытянутой форме, в хромосоме человека молекула ДНК настолько плотно упакована, что ее длина составляет 5 нм.
