
- •Фармакогнозия, ее задачи .
- •Основные понятия лр и лрс
- •Осн историч этапы использ-я и получ лек растений в мировой мед.
- •Создание отеч сырьевой базы лр.
- •Рациональн использование природн ресурсов лр и их охрана.
- •Методы определения запасов дикорастущих лр.
- •Сост-е сырьевой базы культивир лр на совр этапе и ее знач в пр-ве.
- •Основы процесса заготовок лрс.
- •Приёмка лрс и методы отбора проб и метод «ангро».
- •Приёмка лрс и методы отбора проб фасованной продукции.
- •Хим состав лек растений.
- •Методы выявл-я новых лр.
- •Изуч-е запасов лек растений.
- •Методы анализа бав лрс. Изуч хим состава лр.
- •Нов подходы к обеспеч-ю кач-ва лрс согласно треб gmp.
- •Сборы лек (sрес1еs).
- •Гранулы, брикеты.
- •Стероидн соед-я – кардиотонич гликозиды.
- •Перспективы использ-я лрс в соврем мед.
- •Гомеопатия.
- •Полисахариды.
- •Витамины.
- •Жирные масла.
- •Терпеноиды (изопреноиды).
- •Эфирные масла.
- •Гликозиды.
- •Иридоиды и монотерпеновые горечи (гликозиды).
- •Стероидные гликозиды.
- •Кардиотонич гликозиды. Кл-я. Распр-е. Ос-ти их накопл-я. Прим в мед.
- •Кардио гликозиды. Понятие. Хим стр-е. Физ-хим св. Сбор, анализ, хр.
- •Сапонины(с.).
- •Фитоэкдистериоды (ф.).
- •Антраценопроизводные. Локализация по органам и тканям, особ-ти хим строения, физ-хим-кие св-ва ап. Методы анализа.
- •Антраценопроизв-е. Общ хар-ка, кл-ция, распростр-е, биогенез ап. Сбор, сушка, хр-ние, прим в мед-не.
- •Флавоноиды. Общ хар-ка, кл-ция, распр-ние, влияние разл факторов
- •Кумарины и хромоны.
- •Дубильные в-ва. Клас-ция. Распростр-е в мире, накопление в растениях.
- •Дубильные в-ва. Биогенез, методы выделения, сбор, сушка, анализ, хр.
- •Алкалоиды. Хар-ка, клас-ция. Распростр. Накопление в раст. Прим-е.
- •Крахмал, инулин, камеди, пектинов в-ва. (ламинарии)
- •Витамины: шиповник, чёрн смородина, земляника.
- •Витамины: крапива, кукуруза, пастушья сумка, калина.
- •Витамины(ноготки,рябина,облепиха,калина).
- •Жирные масла (маслины, миндаль, абрикос, персик, клещевина).
- •Жирные масла (кукуруза, подсолнечник, тыква).
- •Терпеноиды(мята, шалфей, виды эвкалипта).
- •Терпеноиды: валериана лек-ная, хмель обыкновен.
- •Терпеноиды: сосна обык, можжевельник обык, хмель обык.
- •Терпеноиды: сосна обык, ель, пихта сибирск, тополь чёпный.
- •Терпеноиды: аир, имбирь, анис.
- •Терпеноиды: ромашка апт, ромашка душистая, виды арники.
- •Терпеноиды: багульник, девясил, берёза бородавчатая.
- •Терпеноиды: кориандр посевной, тмин обык, анис обык, фенхель обык.
- •Терпеноиды: душица, чабрец, тимьян.
- •Терпеноиды : гвоздичное дер, бадьян, ажгон, корица.
- •Монотерпен горечи: трилистник вод, золототысячник, одуванчик, пион.
- •Тиогликогизиды: чеснок,лук,виды горчицы.
- •Цианогенные гликозиды: миндаль горький, бузина черная.
- •Кардиотонические гликозиды (наперстянка пупуровая, наперстянка шерсистая, морской лук).
- •Кардиотонические гликозиды (ландыш майский,горицвет весенний)
- •Кардиотонические гликозиды( строфант Комбе, желтушник раскидистый)
- •Сапонины (диаскорея ниппонская,якорцы стелющиеся,смилакс)
- •Сапонины: виды солодки, астрагал, синюха гол, каштан конский.
- •Лекр растения сем-ва аралиевых (женьшень, аралия,заманиха высокая).
- •Фитоэкдистероиды – левзея.
- •Фенолы и фенологликозиды: толокнянка, брусника, родиола.
- •Фенилпропаноиды и лигнаны: лимонник и элеутерококк.
- •Антрацентпроирзводные: марена, алоэ, кассия.
- •Антраценпр-е: крушина, жостер.
- •Антраценпроизводные: ревень, щавель.
- •Флавоноиды: василёк, фиалка, бузина.
- •Флавоноиды: софора японск, рябина, пустырник, боярышник.
- •Флавоноиды: череда, сушеница, пижма, бессмертник.
- •Флавоноиды: зверобой и хвощ.
- •Флавоноиды: виды горца.
- •Флавоноиды: стальник, шлемник, гинкго.
- •Кумарины: Амми, пастернак, инжир.
- •Кумарины и хромоны: вздутоплодник, амми зубная.
- •Алкалоиды: эфедра, безвременник, перец.
- •Алкалоиды: крестовник, анабазис, гранатовое дер.
- •Алкалоиды: красавка, белена, дурман.
- •Алкалоиды: хинное дер, кокаин куст.
- •Алкалоиды: мак, мачёк, маклеи, чистотел.
- •Алкалоиды: барбарис, стефания, жёлтокорень.
- •Алкалоиды: термопсис, софора.
- •Алкалоиды: кубышка, плаун-баранец.
- •Алкалоиды: спорынья, челибуха.
- •Алкалоиды: раувольфия, катарантус, барвинок.
- •Алкалоиды: гармала, пассифлора.
- •Алкалоиды: физостигма, пилокарпус.
- •Алколоиды: чай китайск, кофейн дер, шоколадн дер.
- •Алкалоиды: паслён дольчатый, чемерица Лобеля.
- •Лек раст и сырьё различ хим сост: чага, каланхоэ, малина, почеч чай.
- •Лек сырьё животн происх-я: продукты пчеловодства.
- •Лек сырье животн происх: яды змей, мед пиявки, панты, мумиё, спермацет, ланолин.
Фитоэкдистериоды (ф.).
Ф.-
соед-ние стероидн стр-ры, облад выс
физиологич активн-тью, стимулир и
тонизирующ д-ем. Природн полигидроксилированные
стерины, произв-е циклопентанпергидрофенантрена,
обл активностью гормонов линьки насекомых
и метаморфоза членистоногих и подобные
по структуре экдистероидам. Общ структура
Ф.
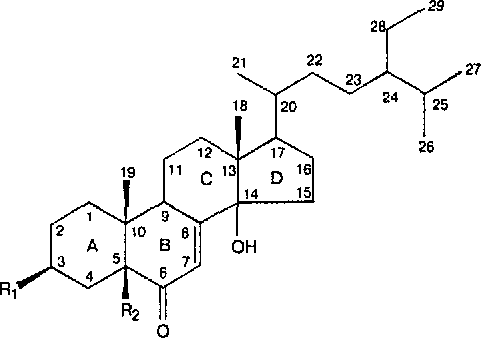 Общ структура экдистероидов R1 –OH, =O; R2
–OH. Ф. найдены у некот представителей
царств протоктист (красн водоросли),
грибов и растений. Среди растений они
довольно обычны у папоротников и
голосеменных. Ф. найдены как у двудольных,
так и у однодольных. Они довольно обычны
среди сложноцветн, гвоздичных, губоцветных
и ряда других сем-тв. В бол-ве растений
Ф. накапливаются в ничтожных кол-вах, в
десятых и сотых долях процента. Лишь в
некот видах, напр серпухе сухоцветной
(Serratula xeranthemoides Bieb.) кол-во экдистероидов
достигает почти 2 %, а в цв кукушкина
цвета (Coccyganthe flos-cuculi (L.) Fourr.) - около 3 %. Ф.
– тв кристаллич в-ва, ХР в этаноле,
метаноле, ацетоне, этилацетате, ПР - в
хлороформе, НР в петролейном эфире.
Оптически активны. Для обнаружения Ф.
ранее использовались биотесты, основанные
на окукливании специальным образом
препарированных личинок различ насекомых
при введ-и им экстрактов, содержащих
гормонально активные соед-я. Ныне
экспресс-анализ растит-ных образцов
осущ-ся благ биотесту, основанному на
линии культуры клеток В-II Drosophila
melanogaster. Для кол-ного обнаружения
фитоэкдистероидов использ методы
радиоиммунного анализа. Ф. и сод-щие их
извлечения из растительного сырья оказ
адаптогенное и психостимулир-е действие,
усил процессы белкового синтеза в орг-ме
и м.б использ-ны как анаболические ср-ва,
антимикробная активность преп, сод-щих
Ф., ранозаживляющее д-е. ЛС -жид экстр
левзеи сафлоровидной (Rhaponticum carthamoides
(Willd.) Iljin) и преп «Экдистен», к-рый содержит
20-гидроксиэкдизон из подземных органов
этого же растения.
Общ структура экдистероидов R1 –OH, =O; R2
–OH. Ф. найдены у некот представителей
царств протоктист (красн водоросли),
грибов и растений. Среди растений они
довольно обычны у папоротников и
голосеменных. Ф. найдены как у двудольных,
так и у однодольных. Они довольно обычны
среди сложноцветн, гвоздичных, губоцветных
и ряда других сем-тв. В бол-ве растений
Ф. накапливаются в ничтожных кол-вах, в
десятых и сотых долях процента. Лишь в
некот видах, напр серпухе сухоцветной
(Serratula xeranthemoides Bieb.) кол-во экдистероидов
достигает почти 2 %, а в цв кукушкина
цвета (Coccyganthe flos-cuculi (L.) Fourr.) - около 3 %. Ф.
– тв кристаллич в-ва, ХР в этаноле,
метаноле, ацетоне, этилацетате, ПР - в
хлороформе, НР в петролейном эфире.
Оптически активны. Для обнаружения Ф.
ранее использовались биотесты, основанные
на окукливании специальным образом
препарированных личинок различ насекомых
при введ-и им экстрактов, содержащих
гормонально активные соед-я. Ныне
экспресс-анализ растит-ных образцов
осущ-ся благ биотесту, основанному на
линии культуры клеток В-II Drosophila
melanogaster. Для кол-ного обнаружения
фитоэкдистероидов использ методы
радиоиммунного анализа. Ф. и сод-щие их
извлечения из растительного сырья оказ
адаптогенное и психостимулир-е действие,
усил процессы белкового синтеза в орг-ме
и м.б использ-ны как анаболические ср-ва,
антимикробная активность преп, сод-щих
Ф., ранозаживляющее д-е. ЛС -жид экстр
левзеи сафлоровидной (Rhaponticum carthamoides
(Willd.) Iljin) и преп «Экдистен», к-рый содержит
20-гидроксиэкдизон из подземных органов
этого же растения.
Антраценопроизводные. Локализация по органам и тканям, особ-ти хим строения, физ-хим-кие св-ва ап. Методы анализа.
Они
встречают в коре, древесине и подземных
органах цветковых растений, могут быть
в плодах, листьях, траве. Особенно типичны
для семейств мареновых, крушиновых,
гречишных, клюзиевых (включая зверобойные).
Они найдены не только в высших растениях,
но и в лишайниках, грибах, а также у
насекомых и морских животных. В растениях
гликозиды находятся в растворенном
виде в клеточном соке, а агликоны – в
виде кристалл-ких включений. Локализуются
чаще в клетках сердцевинных лучей
(ревень), паренхиме коры, где их можно
легко обнаружить хар-ной окраске.
Динамика накопления АП связана с
возрастом растений и фазой развития. С
возрастом в растении количество АП
увеличивается, причем в старых растениях
преобладают окисленные формы, в молодых
– восстановленные. Больше восстановленных
форм АП накапливается ранней весной, к
осени они переходят в окисленные. Это
необходимо иметь в виду при заготовке
сырья, так как более ценными фармакол-кими
св-вами обладают ок-ные формы. АП –
группа природных соед., в основе строения
к-рых структура антрацена
![]() В растениях АП могут находиться в
свободном виде (агликоны) или в виде
гликозидов. Углеводный компонент
представлен глюкозой, рамнозой, ксилозой
и арабинозой. Сахара могут быть
присоединены к агликону через гидроксил
в -
или -положениях
(О-гликозиды), но обнаружены С-гликозиды
в видах алоэ, сенны и др. Ап – крист-кие
в-ва, окр-ные в желтый, оранжевый или
красный цвета. Агликоны в диэтиловом
эфире, хлороформе, бензоле и других
неполярных растворителях, а также в
водных растворах щелочей, образуя
окрашенные в красный цвет феноляты.
Гликозиды ХР в полярных растворителях
и в воде. Это оптически активные вещества,
в УФ-свете флуоресцируют: антрахиноны
– оранжевым, розовым, красным,
огненно-красным цветом; антроны и
антранолы – желтым, голубым, фиолетовым.
Хар-ным св-вом всех АП явл. устойчивость
их ядра. Поэтому все реакции обусловлены
наличием тех или иных функциональных
групп. Используют р-цию Борнтрегера,
основанную на способности антрагликозидов
подвергаться при нагревании щелочному
гидролизу с образованием свободных
фенолятов. После подкисления гидролизата
агликоны извлекают органическим
растворителем (диэтиловым эфиром). При
встряхивании эфирного слоя с аммиаком
они переходят в аммиачный слой и
окрашивают его в вишнево-красный
(1,8-дигидроксиантрахиноны), фиолетовый
(1,2-дигидроксиантрахиноны) цвета, причем
в органический слой переходят антрахиноны,
имеющие -ОН-группу.
Антрахиноны, не имеющие -ОН-групп,
остаются в органическом слое, окрашивая
его в желтый цвет (например, хризофанол).
Для обнаружения антрахинонов, имеющих
хотя бы одну ОН-группу в -положении,
можно использовать реакцию с 1%-ным
метанольным раствором магния ацетата:
1,2-дигидроксипроизводные дают фиолетовое
окрашивание; 1,4-дигидроксипроизводные
– пурпурное; 1,6- и 1,8-дигидроксипроизводные
– оранжево-красное. Для кач-ного обнар-ния
производных антрацена часто используют
бумажную и тонкослойную хроматографию.
Для кол-ного анализа АП используют
фотоэлектроколориметрию.
хроматоспектрофотометрическое
определение антраценпроизводных как
в лекарственном растительном сырья,
так и в галеновых препаратах. Методика
заключается в хроматографическом
разделении экстрактов на силикагеле в
специально подобранной системе. После
сушки и просматривания хроматограммы
в УФ-свете пятна маркируют и элюируют.
Фотометрирование производят при
определенной длине волны. Содержание
каждого из антрахинонов рассчитывают
по калибровочному графику, построенному
по основным биологически активным
соединениям.Высокой чувствительностью
обладает денситофлуориметрический
метод, основанный на разделении веществ
на силикагеле с последующим их превращением
в флуоресцирующие соединения, имеющие
максимум флуоресценции при 555 нм. Эта
методика предложена для определения
производных 1,8-дигидроксиантрона в
экстрактах растений.
В растениях АП могут находиться в
свободном виде (агликоны) или в виде
гликозидов. Углеводный компонент
представлен глюкозой, рамнозой, ксилозой
и арабинозой. Сахара могут быть
присоединены к агликону через гидроксил
в -
или -положениях
(О-гликозиды), но обнаружены С-гликозиды
в видах алоэ, сенны и др. Ап – крист-кие
в-ва, окр-ные в желтый, оранжевый или
красный цвета. Агликоны в диэтиловом
эфире, хлороформе, бензоле и других
неполярных растворителях, а также в
водных растворах щелочей, образуя
окрашенные в красный цвет феноляты.
Гликозиды ХР в полярных растворителях
и в воде. Это оптически активные вещества,
в УФ-свете флуоресцируют: антрахиноны
– оранжевым, розовым, красным,
огненно-красным цветом; антроны и
антранолы – желтым, голубым, фиолетовым.
Хар-ным св-вом всех АП явл. устойчивость
их ядра. Поэтому все реакции обусловлены
наличием тех или иных функциональных
групп. Используют р-цию Борнтрегера,
основанную на способности антрагликозидов
подвергаться при нагревании щелочному
гидролизу с образованием свободных
фенолятов. После подкисления гидролизата
агликоны извлекают органическим
растворителем (диэтиловым эфиром). При
встряхивании эфирного слоя с аммиаком
они переходят в аммиачный слой и
окрашивают его в вишнево-красный
(1,8-дигидроксиантрахиноны), фиолетовый
(1,2-дигидроксиантрахиноны) цвета, причем
в органический слой переходят антрахиноны,
имеющие -ОН-группу.
Антрахиноны, не имеющие -ОН-групп,
остаются в органическом слое, окрашивая
его в желтый цвет (например, хризофанол).
Для обнаружения антрахинонов, имеющих
хотя бы одну ОН-группу в -положении,
можно использовать реакцию с 1%-ным
метанольным раствором магния ацетата:
1,2-дигидроксипроизводные дают фиолетовое
окрашивание; 1,4-дигидроксипроизводные
– пурпурное; 1,6- и 1,8-дигидроксипроизводные
– оранжево-красное. Для кач-ного обнар-ния
производных антрацена часто используют
бумажную и тонкослойную хроматографию.
Для кол-ного анализа АП используют
фотоэлектроколориметрию.
хроматоспектрофотометрическое
определение антраценпроизводных как
в лекарственном растительном сырья,
так и в галеновых препаратах. Методика
заключается в хроматографическом
разделении экстрактов на силикагеле в
специально подобранной системе. После
сушки и просматривания хроматограммы
в УФ-свете пятна маркируют и элюируют.
Фотометрирование производят при
определенной длине волны. Содержание
каждого из антрахинонов рассчитывают
по калибровочному графику, построенному
по основным биологически активным
соединениям.Высокой чувствительностью
обладает денситофлуориметрический
метод, основанный на разделении веществ
на силикагеле с последующим их превращением
в флуоресцирующие соединения, имеющие
максимум флуоресценции при 555 нм. Эта
методика предложена для определения
производных 1,8-дигидроксиантрона в
экстрактах растений.
