
- •1. Отримання і хімічні властивості алканів
- •4.Одерж.Та хім.Власт. Гідркосикислот.
- •1.Для карбоксильної групи
- •2. Для спиртових гідроксидів
- •3. Для гідрокислот
- •3. Алкенові вуглеводні.
- •6. Одержання та власт. Ароматичних вуглеводнів.
- •9. Отримання і хімічні властивості альдегідів
- •11. 2,4,6 Триметилнонан
- •12.Реакції альдегідів та кетонів.
- •15.Гідроксикислоти.Одержання, власт,оптична ізомерія
- •18.Жири, їх будова, класифікація та властивості.
- •Отримання і хімічні властивості естерів
- •2 Бром 3 метил пентан
- •3Метилбутан-1-ол
- •33.Отримання і хімічні властивості альдегідів
- •39 Отримання і хімічні властивості альдегідів
- •Отримання і хімічні властивості кетонів
- •48.Методи одержання і властивості багатоатомних спиртів
- •49.Ацетилен-бензен-толуен-бенз кис---м-нітробенз кис –хлорангідрид бенз кис--ізопропіловийестер м-нітробенз кис
- •51. Методи одержання та властивості галогенопохідних вуглеводнів.
- •2. Отримання етанолу
- •57. Отримання і хімічні властивості циклоалканів
- •60. Отримання і хімічні властивості ароматичних вуглеводнів
- •63. Отримання і властивості дієнових вуглеводнів.
- •2. Піроліз метану
- •140. Реакції
- •151. CoSo4
- •157. CaCo3
11. 2,4,6 Триметилнонан
CH3-CH(CH3)-CH2-CH(CH3)- CH2-CH(CH3)-CH2-CH3
Пропіоновий альдегід CH3-CH2-COH
12.Реакції альдегідів та кетонів.
Хімічні властивості альдегідів
1. приєднання водню
![]()
2. реакції окислення
• окислення біхроматом калію
![]()
• реакція срібного дзеркала
![]()
• реакція окислення гідроксидом Купруму(ІІ)
![]()
Хімічні властивості кетонів
1. приєднання водню
![]()
2. реакції окислення для кетонів протікають лише під дією дуже сильних окислювачів і супроводжуються розривом вуглецевого ланцюга. кетони не дають реакцію срібного дзеркала і не окислюються гідроксидом Купруму(ІІ).
13.кальцій карбід = ацетилен = бензин = етилбеензен = вінілбензен = полістирол
1.СаС2 + 2H2O→CHΞCH + Ca(OH)2
2. 3CHΞCH→C6H6
3. C6H6 + CH2=CH2→ C6H5-CH2-CH3
4. C6H5-CH2-CH3→ C6H5-CH=CH2 + H2
5. …C6H5-CH=CH2 + C6H5-CH=CH2 + C6H5-CH=CH2 …→…CH2-CH(C6H5)- CH2-CH(C6H5)- CH2-CH(C6H5)-CH2…
14.2,3,3-триметилгексан CH3-CH(CH3)-C(CH3)2-(CH2)2-CH3
Масляна к-та CH3-CH2- CH2-CООН
15.Гідроксикислоти.Одержання, власт,оптична ізомерія
Оптичні ізомери також відносять до стереоізомерів. Але на відміну від цис- транс-ізомерів, температури топлення й кипіння, густина та інші властивості оптичних ізомерів однакові. Вони відрізняються лише активністю відносно плоскополяризованого світла. Здатність обертати площину поляризаціїполяризованного світла була названа оптичною активністю, а самі речовини - оптично активними. Явище оптичної активності поширене серед органічних речовин природного походження (оксикислоти, амінокислоти, вуглеводи, білки, нуклеїнові кислоти). Це явище має велике біологічне значення, оскільки пов’язане з асиметрією речовин, що входять до складу живих організмів. Оптично активні речовини існують у вигляді оптичних ізомерів: правих (+)-форм (конфігурацій) і лівих (-)-форм (конфігурацій), тобто у вигляді стереоізомерів, які відрізняються різним розміщенням лігандів у просторі навколо асиметричного атома С*.
Атом вуглецю з чотирма різними замісниками (лігандами) називають асиметричним (позначається зірочкою С*).
16.ацетилен = бензин = ізопропілбензен = бензойна к-та = мета-нітробензойна к-та = хлорангідрид мета-нітробензойної к-ти
1. 3CHΞCH→C6H6
2. C6H6 + CH(CH3)=CH2→ C6H5-CH(CH3)-CH3
3. C6H5-CH(CH3)-CH3 + O2→ C6H5COOH + CH3-CH3
4. C6H5COOH + HNO3→ C6H4(NO2)COOH + HOH
5. C6H4(NO2)COOH + PCL5 → C6H4(NO2)COCL + POCL3 + HCL
17. 2-метил-бут-2-ен СН3-С(СН3)=СН-СН3
Етаналь СН3-СОН
18.Жири, їх будова, класифікація та властивості.
Жири - органічні речовини, які являють собою складні ефіри гліцерину і вищих карбонових кислот. Жири надзвичайно поширені у живій природі і входять до складу всіх тваринних і рослинних клітин. Жири виконують функцію джерела енергії і у деяких тварин також функцію терморегуляції.
Жири мають високу енергетичну цінність і тому є необхідною складовою харчування людини.
Класифікація
• класифікація за природним походженням
рослинні жири (рослинні масла)
тваринні жири
Отримання і хімічні властивості жирів
Отримання
Жири отримують з продуктів рослинного або тваринного походження.
Хімічні властивості
1. Гідроліз (омилення) жирів у лужному середовищі
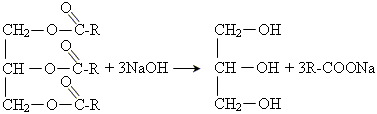
19.ацетилен = бензен = ізопропілбензен = фенол = натрій фенолят = дифенілів етер
1. 3CHΞCH→C6H6
2. C6H6 + CH(CH3)=CH2→ C6H5-CH(CH3)-CH3
3. C6H5-CH(CH3)-CH3 + O2 (+H2SO4)→C6H5OH + CH3-C=O-CH3
4. 2C6H5OH + 2Na → 2C6H5ONa + H2
5. C6H5ONa + 2C6H5I → C6H5-O-H5C6
20. 2,5-диметилгекс-3-ен CH3-CH(CH3)-CH=CH-CH(CH3)-CH3
Валеріанова к-та CH3-(CH2)3-COOH
21.
