
- •1. Отримання і хімічні властивості алканів
- •4.Одерж.Та хім.Власт. Гідркосикислот.
- •1.Для карбоксильної групи
- •2. Для спиртових гідроксидів
- •3. Для гідрокислот
- •3. Алкенові вуглеводні.
- •6. Одержання та власт. Ароматичних вуглеводнів.
- •9. Отримання і хімічні властивості альдегідів
- •11. 2,4,6 Триметилнонан
- •12.Реакції альдегідів та кетонів.
- •15.Гідроксикислоти.Одержання, власт,оптична ізомерія
- •18.Жири, їх будова, класифікація та властивості.
- •Отримання і хімічні властивості естерів
- •2 Бром 3 метил пентан
- •3Метилбутан-1-ол
- •33.Отримання і хімічні властивості альдегідів
- •39 Отримання і хімічні властивості альдегідів
- •Отримання і хімічні властивості кетонів
- •48.Методи одержання і властивості багатоатомних спиртів
- •49.Ацетилен-бензен-толуен-бенз кис---м-нітробенз кис –хлорангідрид бенз кис--ізопропіловийестер м-нітробенз кис
- •51. Методи одержання та властивості галогенопохідних вуглеводнів.
- •2. Отримання етанолу
- •57. Отримання і хімічні властивості циклоалканів
- •60. Отримання і хімічні властивості ароматичних вуглеводнів
- •63. Отримання і властивості дієнових вуглеводнів.
- •2. Піроліз метану
- •140. Реакції
- •151. CoSo4
- •157. CaCo3
3. Алкенові вуглеводні.
Отримання
Промислові методи
1. Крекінг алканів нафти
Лабораторні методи
1. Дегідратація спиртів
![]()
2. Відщеплення галогенів (Cl, Br)
![]()
3. Гідрування алкінів
![]()
Хімічні властивості
1. Реакція гідрування
2.Реакція Вагнера (окиснення перманганатом Калію у лужному середовищі)
![]()
Реакції приєднання HBr і HCl
![]()
5. Реакції приєднання Br2 і Cl2
![]()
6. Реакції приєднання води (за правилом Марковникова)
![]()
7. Реакції полімеризації
![]()
4. етил ацетилен=метилелтикетон=бутан-2-ол=втор. бутиловий естер оцтової к-ти
1. CHΞC-CH2-CH3 + HOH→CH3-CH2-C(=O)-CH3
2. CH3-CH2-C(=O)-CH3+ H2→ CH3-CH2-CH(OH)-CH3
3. CH3-CH2-CH(OH)-CH3 + CH3-COOH→CH3C=O-O-CH(CH3)-CH2-CH3 + H2O
5. 3-метил-3-етилоктан
CH3-CH2-C(CH3)(CH2-CH3)-(CH2)5-CH3
Бромитий ізобутил BrH2C-CH(CH3)2
6. Одержання та власт. Ароматичних вуглеводнів.
Промислові методи отримання бензолу і його гомологів
1. перегонка кам'яновугільної смоли
2. каталітичний риформінг нафти
3. реакція Реппе
3CHΞCH→C6H6
Лабораторні методи
1. дегідрогенізація циклогексану
![]()
2. дегідроциклізація гептану
![]()
Хімічні властивості бензену
1. реакції приєднання
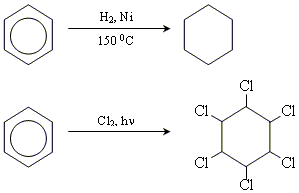
2. реакції заміщення
• реакція нітрування
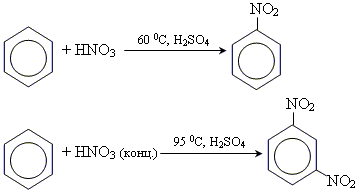
• реакція сульфування
![]()
• реакція Фриделя-Крафса
•• алкілювання
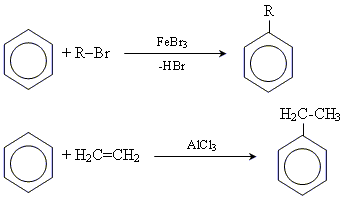
•• ацилювання
![]()
• реакції галогенування (Cl, Br)
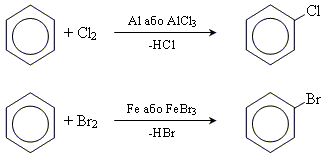
• реакція нітрування толуену
![]()
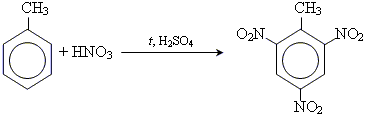 .
.
7.етилен = етанол = оцтова к-та = моно хлороцтова к-та = ізопропіловий естер моно хлороцтова к-ти
1.CH2=CH2 + HOH→CH3-CH2-OH
2. CH3-CH2-OH + [O]→CH3-COH+ [O]→ CH3-COOH
3. CH3-COOH + CL2→ CH2(CL)-COOH + HCL
4. CH2(CL)-COOH + CH(CH3)2-OH→
CH2(CL)-C=O-O-CH(CH3)2 + H2O
8. 2,4-диметил-4-етилоктан
CH3-CH(CH3)-CH2-C(CH2)(CH2-CH3)-(CH2)4-CH3
Трет. бутиловий спирт H3C-C(CH3)2-OH
9. Отримання і хімічні властивості альдегідів
Альдегіди і кетони значно поширені у природі. Значна кількість карбонільних сполук біологічного походження входить до складу ефірних масел*. Як приклад можна навести цитраль* і н-деканаль*, що входять до складу апельсинового і лимонного масел або ментон, що входить до складу м'ятного масла*.
Використання:
• органічний синтез
• виробництво полімерних матеріалів
• виробництво лікарських препаратів і дезінфікуючих засобів
• виготовлення
• виробництво барвників
Отримання
1. окислення первинних спиртів
![]()
2. каталітична дегідрогенізація первинних спиртів
![]()
Отримання оцтового альдегіду
1. каталітичне окислення етилену
![]()
2. отримання за реакцією Кучерова
![]()
Отримання і хімічні властивості кетонів
Отримання
1. окислення вторинних спиртів
![]()
2. отримання за реакцією Кучерова
![]()
3. піроліз кальцієвих солей карбонових кислот
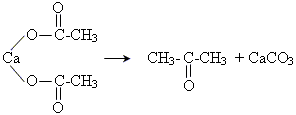
10.пропілен = 3-хлорпроп-1-ен = аліловий спирт = 1,2-дихлорпропан-3-ол = гліцерин
1. CH2=CH-CH3 + →
2. CH2=CH-CH2CL + NaOH→ CH2=CH-CH2-OH +NaCL
3. CH2=CH-CH2-OH + CL2→ CH2CL-CHCL-CH2-OH + H2
4. CH2CL-CHCL-CH2-OH + 2NaOH→CH2OH-CHOH-CH2OH + NaCL
