
- •Концентрация ионов водорода в крови больного равняется 2,46∙10-8 моль/л.
- •Определите заряд комплексообразователя и его координационное число в комплексном ионе [Fe(c2o4)2(oh)2]3-.
- •Напишите формулу комплексного соединения, имеющего название: хлорид гексаамминхрома (III).
- •Выражение константы нестойкости:
- •4. Выражение константы нестойкости:
- •Напишите коллоидно-химические формулы мицелл золей полученных по реакциям:
- •Имеются 3 коллоидных раствора: гидроксида железа (III), полученного гидролизом FeCl3, иодида серебра, полученного в избытке кi, и иодида серебра, полученного в избытке AgNo3.
- •Пороговая концентрация коллоидного раствора гидроксида алюминия равняется 0,63 ммоль/л.
- •Иэт альбумина плазмы крови равна 4,64.
- •Часть IV. Упражнения по биоорганической химии
- •Сопряжение. Ароматичность. Электронные эффекты заместителей
- •Объясните, в каком соединении – хлорбензоле или бензилхлориде (фенилхлорметане) – галоген является частью сопряженной системы.
- •Решение
- •Укажите вид и знак электронных эффектов в этиламине (этанамине) и п-аминобензойной (4-аминобензойной) кислоте.
- •Кислотность и основность органических соединений
- •Расположите в порядке уменьшения кислотности этанол, этиленгликоль (этандиол-1,2), глицерин (пропантриол-1, 2, 3).
- •Расположите в порядке уменьшения основности анилин, этанамин (этиламин), 3-аминофенол.
- •Реакции электрофильного характера
- •Напишите схему реакции гидратации пропена (пропилена).
- •Напишите схему реакции бромирования анилина.
- •Напишите схему реакции бромирования бензойной кислоты (катализатор FеBr3).
- •Напишите схемы реакций алкилирования бензола третичным изобутанолом и пропеном в кислой среде.
- •Реакции нуклеофильного характера
- •Напишите схему реакции взаимодействия 1-бромпропана с этилатом натрия.
Выражение константы нестойкости:
[Cr(NH3)6]3+ ↔ Cr 3+ + 6 NH3
Рассчитайте G процесса [Fe(CN)6]4- ↔ Fe2+ + 6CN-, если Кн в стандартных условиях равна 10-35.
Изобразите графически структурную формулу комплексной частицы.
Классифицируйте её по природе лигандов.
Напишите выражение константы нестойкости.
Решение
Изменение свободной энергии Гиббса ΔG и константа равновесия связаны соотношением:
![]()
Подставляя данные задачи и учитывая, что стандартные условия соответствуют Т=298 К,получаем:
ΔG=-8,31*298 *ln10-35=-2,3*8,31*298*lg10-35=-2,3*8,31*298*(-35)=199349 дж=199,349 кДж
Структурная формула комплексной частицы:
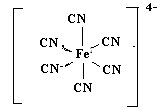
3.По природе лиганда данное соединение является ацидокомплексом, т.к. CN- - кислотный остаток синильной кислоты
4. Выражение константы нестойкости:
Физико-химия коллоидно-дисперсных систем и растворов ВМС
Напишите коллоидно-химические формулы мицелл золей полученных по реакциям:
А) AgNO3 + KI
Б) CaCl2 + H2C2O4 →
В) FeCl3 + NaOH
Г) FeCl3 + H2O
Приведите строение мицелл.
Примечания:
В вариантах А – В необходимо написать формулы мицелл в избытке каждого из исходных веществ.
Решение
Коллоидно-химические формулы мицелл золей:
А) AgNO3 + KI AgI↓+К NO3
Состав мицеллы, полученной при избытке AgNO3, может быть представлен следующим образом:
[m AgI *nAg+*(n-x) NO3-]x+ *х NO3-
Строение мицеллы:
Ядро - m AgI *nAg+; адсорбционный слой противоионов -(n-x) NO3-; диффузный слой противоионов - х NO3-.
Состав мицеллы, полученной при избытке KI, может быть представлен следующим образом:
[m AgI *nI-*(n-x) К+]x- *х К+
Строение мицеллы:
Ядро - m AgI *nI-; адсорбционный слой противоионов -(n-x) К+; диффузный слой противоионов - х К+.
Б) CaCl2 + H2C2O4→Са C2O4↓ +2 HCl
Состав мицеллы, полученной при избытке CaCl2, может быть представлен следующим образом:
[m Са C2O4 *nCa2+*2(n-x) Cl-]2x+ *2х Cl-
Строение мицеллы:
Ядро - m Са C2O4 *nCa2+; адсорбционный слой противоионов 2(n-x) Cl-; диффузный слой противоионов - 2х Cl-
Состав мицеллы, полученной при избытке H2C2O4, может быть представлен следующим образом:
[m Са C2O4 *n C2O42-*2(n-x) H+]2x- *2х H+
Строение мицеллы:
Ядро - m Са C2O4 *n C2O42-; адсорбционный слой противоионов 2(n-x) H+; диффузный слой противоионов - 2х H+
В) FeCl3 + 3NaOH Fe(OH)3↓ +3NaCl
Состав мицеллы, полученной при избытке FeCl3, может быть представлен следующим образом:
[m Fe(OH)3*nFe3+*3(n-x) Cl-]3x+ *3х Cl-
Строение мицеллы:
Ядро - m Fe(OH)3*nFe3+; адсорбционный слой противоионов 3(n-x) Cl-; диффузный слой противоионов - 3х Cl-
Состав мицеллы, полученной при избытке NaOH, может быть представлен следующим образом:
[m Fe(OH)3*nОН-* (n-x) Na+]x- *х Na+
Строение мицеллы:
Ядро - m Fe(OH)3*n ОН-; адсорбционный слой противоионов (n-x) Na+; диффузный слой противоионов - х Na+
Г) FeCl3 + 2H2O Fe(OH)2Cl+ 2HCl
Fe(OH)2Cl ↔ FeOCl+ H2O
Состав мицеллы, полученной при гидролизе хлорида железа, может быть представлен следующим образом:
[m Fe(OH)3] *nFeO+*(n-x)Cl-}+x*xCl-,
Строение мицеллы:
Ядро - m Fe(OH)3* nFeO+; адсорбционный слой противоионов (n-x) Cl-; диффузный слой противоионов - х Cl-
