- •Дисахариды. Полисахариды
- •Напишите уравнение реакции образования мальтозы.
- •Напишите уравнение реакции образования лактозы.
- •Напишите уравнение реакции образования сахарозы.
- •Напишите формулы фрагментов молекул амилозы и амилопектина.
- •Напишите формулы дисахаридных фрагментов молекул хондроитинсульфата и гиалуроновой кислоты.
- •Напишите проекционные формулы Фишера для всех изомеров треонина.
- •Напишите уравнения реакций восстановительного аминирования с участием -кетоглутаровой кислоты и трансаминирования с участием аспарагиновой и пировиноградной кислот.
- •Напишите уравнения реакций окислительного дезаминирования глутаминовой кислоты (in vivo) и неокислительного дезаминирования лейцина (in vivo, in vitro).
- •Напишите уравнения реакций солеобразования валина, декарбоксилирования тирозина, гидроксилирования фенилаланина.
- •Напишите уравнение реакции образования трипептида Три – Сер – Мет.
- •Нуклеиновые кислоты. Нуклеотидные коферменты
- •Напишите строение гуанина, урацила и комплементарных им оснований.
- •Напишите схему реакции превращения пировиноградной кислоты в молочную с участием кофермента надн.
Напишите уравнения реакций окислительного дезаминирования глутаминовой кислоты (in vivo) и неокислительного дезаминирования лейцина (in vivo, in vitro).
Назовите все участвующие в реакции вещества по ЗН ИЮПАК.
Укажите биологическое значение реакции дезаминирования.
Ответ
1. Уравнение реакции окислительного дезаминирования глутаминовой кислоты (in vivo) .
Окислительное дезаминирование происходит при участии ферментов оксидаз и кофермента НАД+, который выступает в качестве окислителя. В результате выделяется аммиак и образуется соответствующая кетокислота.
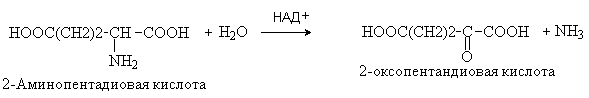
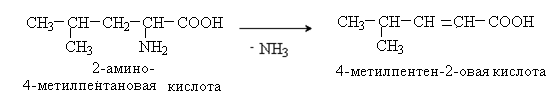
Уравнение реакции неокислительного дезаминирования лейцина (in vivo).
Неокислительное дезаминирование происходит путем отщепления аммиака под действием ферментов с образованием , -непредельных кислот.
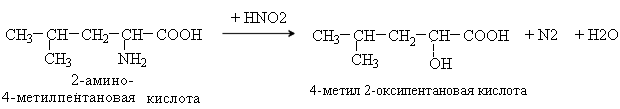
Уравнение реакции неокислительного дезаминирования лейцина (in vitro).
Аминокислоты содержат первичную аминогруппу и подобно первичным аминам взаимодействуют с азотистой кислотой с выделением азота. При этом происходит замещение аминогруппы на гидроксильную. Реакция используется для количественного определения аминокислот по объему выделившегося азота (метод Ван-Слайка).
Биологическое значение реакции дезаминирования: с помощью реакций дезаминирования снижается избыток аминокислот в организме.
Напишите уравнения реакций солеобразования валина, декарбоксилирования тирозина, гидроксилирования фенилаланина.
Назовите все участвующие в реакции вещества по ЗН ИЮПАК.
Укажите значение этих реакции.
Ответ
1. Уравнения реакций
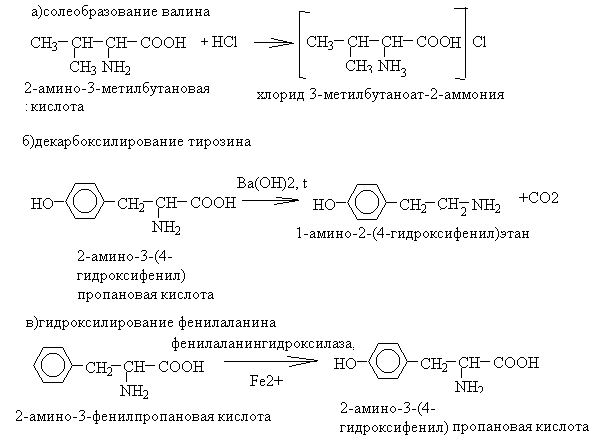
2. Значение реакций: реакции солеобразования используют для защиты аминогруппы при пептидном синтезе, декарбокислирование – один из способов получения биогенных аминов, гидроксилирование фенилаланина – первый этап его метаболизма.
Напишите уравнение реакции образования трипептида Три – Сер – Мет.
Выделите пептидные связи.
Назовите незаменимые аминокислоты, входящие в состав трипептида.
Укажите, в какой среде находится ИЭТ трипептида.
Объясните роль серина в формировании пространственной структуры пептидов и белков.
Ответ
Уравнение реакции образования трипептида Три – Сер – Мет

2.В состав трипептида входят незаменимые аминокислоты триптофан и метионин
3.Изоэлектрическая точка пептида находится в среде, близкой к нейтральной, поскольку входящие в него аминокислоты содержат неполярные радикалы (триптофан и метионин) и полярный неионогенный радикал (серин). Предположительно, ИЭТ пептида =5,7-5,8.
4. Роль серина в формировании пространственной структуры пептидов и белков определяется наличием гидроксогруппы, способной образовывать водородные связи. Водородные связи участвуют в формировании вторичной, третичной и четвертичной структур белков.
Нуклеиновые кислоты. Нуклеотидные коферменты
Напишите строение гуанина, урацила и комплементарных им оснований.
Продемонстрируйте варианты образования водородных связей.
Объясните механизм их возникновения.
Ответ
1. Строение гуанина, урацила и комплементарных им оснований.

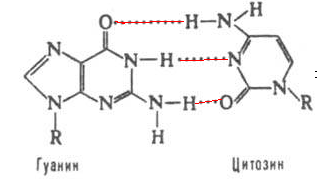
Урацил комплементарен аденину , гуанин –цитозину. На схемах указаны варианты образования водородных связей между основаниями.
2. Механизм возникновения водородных связей: атомы водорода, на которых, вследствие разности электроотрицательностей водорода и азота, формируется частичный положительный заряд, притягиваются к атомам кислорода, входящим в состав карбонильных групп и атомам азота, входящим в состав гетероциклов. На атомах О и N сформирована избыточная электронная плотность. Электростатическое притяжение противоположно заряженных частиц приводит к образованию водородной связи.
Напишите схемы полного и неполного гидролиза аденозин-5'-фосфата.
Выделите сложноэфирную и гликозидную связи.
Назовите продукты реакций.
Укажите механизм реакций.
Ответ
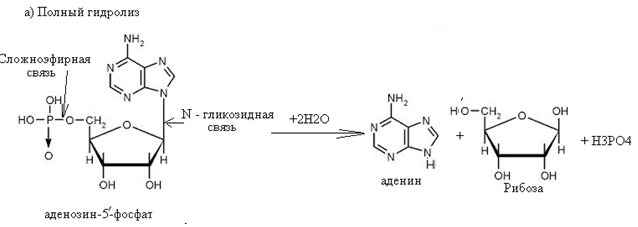
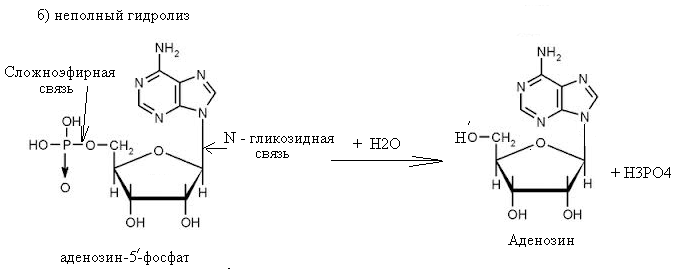
Аденозин-5'-фосфат легко гидролизуется под влиянием слабых кислот при нагревании. При этом образуется аденозин, рибоза и фосфорная кислота. При неполном гидролизе могут образовываться различные продукты, в том числе аденозин и ортофосфорная кислота.
Напишите схему взаимодействия АТФ с -аланином (образование аминоациладенилатного комплекса).
Назовите биологическую роль этого процесса.
Ответ
1. Схема взаимодействия АТФ с -аланином (образование аминоациладенилатного комплекса).
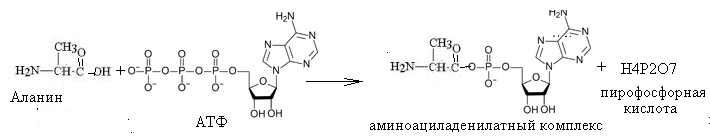
2. Биологическая роль этого процесса –активирование аминокислоты для реакции биосинтеза.
Напишите строение антикодона в т-РНК, соответствующего кодону УГУ в и-РНК.
Ответ
Антикодоны тРНК комплементарны кодонам иРНК. Т.о. антикодон будет представлен последовательностью нуклеотидов, комплементарных урацилу, гуанину, урацилу. Таковыми нуклеотидами, соотвественно, являются: аденин (А), цитозин(Ц) и аденин (А). т.о., строение антикодона -АЦА
Напишите схему превращения яблочной (гидроксибутандиовой) кислоты в щавелевоуксусную (оксобутандиовую) кислоту с участием кофермента НАД+.
Укажите биологическое значение реакции.
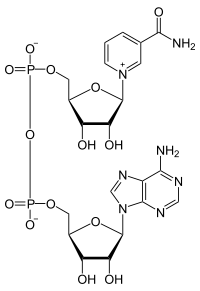
Покажите строение НАД+.
Ответ
1. Схема превращения яблочной (гидроксибутандиовой) кислоты в щавелевоуксусную (оксобутандиовую) кислоту с участием кофермента НАД+.

2. Биологическое значение реакции: данная реакция входит в цикл Кребса, в ходе которого осуществляется биологическое окисление субстратов до воды и углекислого газа.
3. Строение НАД+ (окисленная форма никотинамидадени́ндинуклеоти́да)