
- •Тканевое дыхание. Атф как макроэргическое соединение. Цикл атф-адф. Виды фосфорилирования как реакции образования атф.
- •Окис-е фосф-е: сущноть процесса, обобщённая схема. Строение митохондрий и локализация в них компонентов окислительного фосфорилирования.
- •Убихинол-дегидрогеназа (цитохром с-редуктаза). Цитохром с-оксидаза. Особенности состава, строения, функций. Компоненты дыхательной цепи митохондрий.
- •Трансмембранный электрохимический потенциал как промежуточная форма энергии при окислительном фосфорилировании. Н- атф- синтаза: биологическая роль, локализация, строение, механизм синтеза атф.
- •Окислительное декарбоксилирование пировиноградной кислоты: биологическое значение, последовательность реакций. Механизмы регуляции скорости.
- •Пируватдегидрогеназный комплекс животных. Строение, коферменты активных центров, тонкий механизм катаболизма.
- •Анаболитическая функция общего пути катаболизма.
- •Энергетическая функция опк. Гипоэнергетические состояния. Причины развития гипоксии.
- •Углеводы. Определение. Особенности химического состава и строения углеводов. Классификация углеводов по химической структуре.
- •Биологические функции углеводов. Соответствие химической структуры этих соединений выполняемым функциям
- •Переваривание и всасывание углеводов в желудочно-кишечном тракте человека. Ферменты, принимающие участие в этих процессах.
- •Аллостерическая регуляция гликолиза и глюконеогеза в печени. Субстратные циклы.
- •Гормональная регуляция гликолиза, глюконеогенеза и обмена гликогена. Взаимосвязь с ритмом питания.
- •Пути образования и утилизации лактата в печени и мышцах. Лактатдегидрогеназа. Цикл Кори.
- •Пентозофосфатный путь превращения глюкозы. Биологическая функция. Схема процесса лимитирующая реакция. Окислительный и неокислительный этапы, Обратимость неокислительной стадии.
- •Нарушение углеводного обмена. Гипо- и гепергликемия. Инсулин и углеводный обмен, сахарный диабет.
Обмен веществ в организме. Процессы катаболизма и анаболизма. Эндергонические и Экзергонические реакции в живой клетке.
В процессе обмена веществ осуществляется связь внешней среды и организма. Обмен веществ включает 3 этапа: поступление веществ в организм, метаболизм и выделение конечных продуктов из организма.
Катаболизм - процесс расщепления органических молекул до конечных продуктов. Конечные продукты превращений органических веществ у животных и человека - СО2, Н2О и мочевина. В процессы катаболизма включаются метаболиты, образующиеся как при пищеварении, так и при распаде структурно-функциональных компонентов клеток.
Реакции катаболизма сопровождаются выделением энергии (экзергонические реакции-ΔG если, то реакция протекает самопроизвольно и сопровождается уменьшением свободной энергии, если при этом абсолютное значение ΔG велико, то реакция идёт практически до конца, и её можно рассматривать как необратимую).
Анаболизм объединяет биосинтетические процессы, в которых простые строительные блоки соединяются в сложные макромолекулы, необходимые для организма. В анаболических реакциях используется энергия, освобождающаяся при катаболизме (эндергонические реакции- если ΔG положительно, то реакция будет протекать только при поступлении свободной энергии извне; такие реакции называют эндергоническими. Если абсолютное значение ΔG велико, то система устойчива, и реакция в таком случае практически не осуществляется. При ΔG, равном нулю, система находится в равновесии).
Тканевое дыхание. Атф как макроэргическое соединение. Цикл атф-адф. Виды фосфорилирования как реакции образования атф.
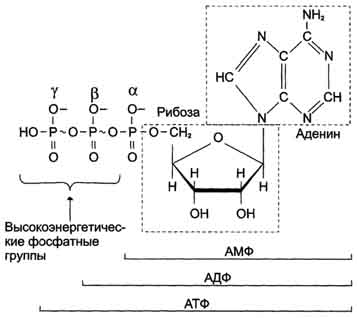
Тканевое дыхание — совокупность биохимических реакций, протекающих в клетках живых организмов, в ходе которых происходит окисление углеводов, липидов и аминокислот до углекислого газа и воды. Высвобожденная энергия запасается в химических связях макроэргических соединений (АТФ и др.) и может быть использована по мере необходимости.
К группе высокоэнергетических фосфатов, помимо АТФ, относят енолфосфаты, ангидриды и фосфогуанидины. АТФ - молекула, богатая энергией, поскольку она содержит две фосфоангидридные связи (β, γ). При гидролизе концевой фосфоангидридной связи АТФ превращается в АДФ и ортофосфат Рi.
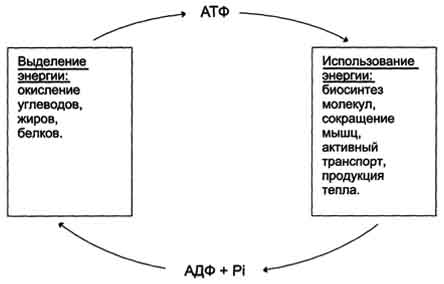
Окислительное фосфорилирование и субстратное фосфорилирование
Окис-е фосф-е: сущноть процесса, обобщённая схема. Строение митохондрий и локализация в них компонентов окислительного фосфорилирования.
Синтез АТФ из АДФ и Н3РО4 за счёт энергии переноса электронов по ЦПЭ называют окислительным фосфорилированием.
Первый процесс - перенос электронов от восстановленных коферментов NADH и FADH2 через ЦПЭ на кислород - экзергонический.
NADH + Н+ +1/2 O2 → NAD+ + H2O + 52 ккал/моль(≈220 кДж/моль).
Второй процесс - фосфорилирование АДФ, или синтез АТФ, - эндергонический:
АДФ + Н3РО4+7,3 ккал/моль (30,5 кДж/моль) = АТФ + Н2О.
Митохо́ндрия— двумембранная гранулярная или нитевидная органелла, имеющая наружнюю мембрану, межмембранное пространство, внутреннюю мембрану и матрикс.
Перенос электронов по дыхательной цепи от NADH к кислороду сопровождается выкачиванием протонов из матрикса митохондрий через внутреннюю мембрану в межмембранное
пространство. На эту работу затрачивается часть энергии электронов, переносимых по ЦПЭ.
Дыхательная цепь- ключевой компонент митохондриальной системы окислительного фотсфорилирования . Структурная организация дыхательной цепи. Митохондриальная цепь переноса электронов как часть системы дыхания всего организма.
Основные переносчики электронов встроены во внутреннюю мембрану митохондрий и организованы в 4 комплекса:
На первом этапе дегидрогеназы катализируют отщепление водорода от различных субстратов. Если субстратами служат а-гидрокси-кислоты малат, изоцитрат, 3-гидроксибутират, водород переносится на NAD+. Образовавшийся NADH в дыхательной цепи, в свою очередь, окисляется NADH-дегидрогеназой.
Если субстратом служат такие соединения, как сукцинат или глицерол-3-фосфат, акцептором водорода служат FAD-зависимые дегидрогеназы. От NADH и FADH2 электроны и протоны передаются на убихинон и далее через цепь цитохромов к молекулярному кислороду.
1. NADH-дегидрогеназа, комплекс I; 2. Коэнзим Q, убихинон; 3. рН2-дегидрогеназа, комплекс III; 4. Цитохром с; 5. Цитохромоксидаза, комплекс IV; 6. Сукцинатдегидрогеназа, комплекс II;
НАД- зависимые и флавиновые дегидрогеназы. НАДН-дегидрогеназы. Особенности состава, строения, функций. Коферменты компонентов дыхательной цепи митохондрий.
Перенос электронов от окисляемых субстратов к кислороду происходит в несколько этапов.
Никотинамидзависимые дегидрогеназы содержат в качестве коферментов NAD+ или NADP+ из витамина РР ,входят в состав активных центров дегидрогеназ, но могут обратимо диссоциировать из комплекса с апоферментами и включаются в состав фермента в ходе реакции. Субстраты NAD- и NADP-зависимых дегидрогеназ находятся в матриксе митохондрий и в цитозоле. Рабочей частью никотинамидных коферментов служит никотинамид.
R-CHOH-R1 + NAD+↔ R-CO-R1 + NADH + Н+.
Флавиновые дегидрогеназы содержат в качестве коферментов FAD или FMN. Эти коферменты образуются в организме человека из витамина В2). Флавиновые коферменты прочно связаны с апоферментами. Рабочей частью FAD и FMN служит изоаллоксазиновая сопряжённая циклическая система.
R-CH2-CH2-R1 + Е (FAD) ↔ R-CH=CH-R1 + Е (FADH2),
где Е - белковая часть фермента
Большинство FAD-зависимых дегидрогеназ –белки, локализованные в матриксе митохондрий. Исключение сукцинат-дегидрогеназа. К FMN-содержащим ферментам принадлежит NADH-дегидрогеназа, которая также локализована во внутренней мембране митохондрий; она окисляет NADH, образующийся в митохондриальном матриксе.
NADH-дегидрогеназа (NADH-Q-редуктаза, комплекс I) состоит из нескольких полипептидных цепей. Роль простетической группы играет FMN. Единственный субстрат фермента - NADH, с которого 2 электрона и протон переносятся на FMN с образованием FMNH2. Второй протон поглощается из матрикса.
NADH + Н+ + Е (FMN) → NAD+ + Е (FMNH2).
С FMNH2 электроны переносятся затем на ряд железо-серных белков (FeS) железо-серных центров, участвующих в окислительно-восстановительных реакциях. Известны 3 типа FeS-центров (FeS, Fe2S2, Fe4S4). От железо-серных центров электроны переносятся на кофермент Q (убихинон). Е (FMNH2) + Q → Е (FMN) + QH2
