
- •5. Жоғары молекулалы бионанонысандар. Дендромерлер
- •6.Ферменттер, құрылысы, қасиеттері, нанотехнологияда қолдануы
- •7) Клетканың ұйымдасуы. Органеллалар. Биологиялық материалдардың нанотехнологияда қолданылуы.
- •9. Нанотүтікшелер, құрылысы, қасиеттері, қолдануы.
- •12.Макромолекулалар (белоктар, нуклеин қышқылдары, липидтер, көмірсулар).
- •14.Көміртектің аллотропты формалары.
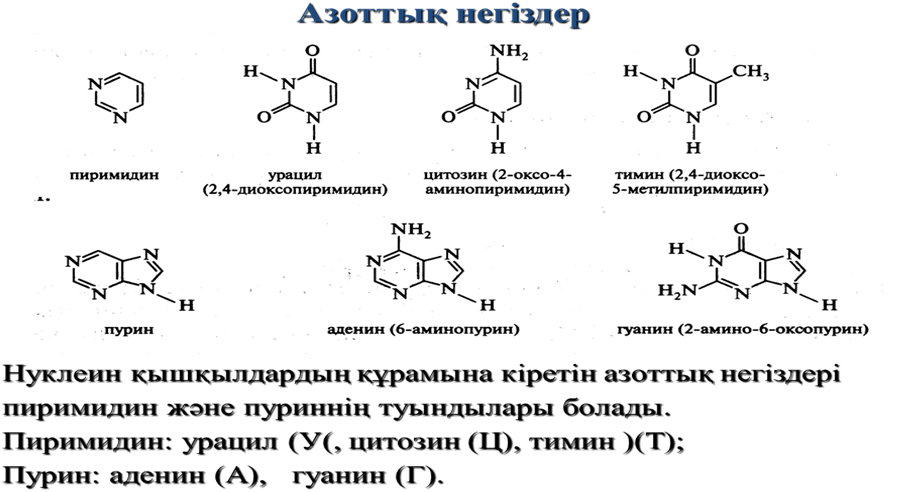
- •16)Амин қышқылдары, нуклеотидтер, қарапайым қанттар, липидтер, биологиялық белсенді қоспалар - биологиялық макромолекулардың жасалуының негізі және бионанотехнологиялардың қатысушылары.
- •20. Өндірістегі биокатализ. Нанокатализаторлар.
- •21.Электронды микроскоптар. Тарихы, түрлері, жұмыс принциптері, ажырату мүмкіншіліктері. Қазіргі күнгі электронды микроскоптардың конструкциялары
- •23. Туннельдік микроскоп
- •25.Өткізгіш электронды, сканерлейтін электронды микроскоптар. Жұмыс принциптері, ажырату мүмкіншіліктері.
- •26. Бионанороботтардың жұмысы неге негізделген? Олардың түрлері.
- •27. Биоминералдану.
- •29.Тағам өндірісінде қолданылатын нанотехнология жетістіктері.
- •30. Медицина мен фармакологияда қолданатын наноматериалдар.
- •31.Бионаноқұрылғылардың қолдану аймағы: энергетика, электроника, құрылыс.
- •33)Нанобөлшектердің алу әдістері.
- •34)Биологиялық процесстер: фотосинтез, органикалық қосылыстардың тотығу-тотықсыздануы. Олардың нанотехнологияда қолданылуы.
- •35)Нанотүтікшелердің қандай алу әдістерін білесіз?
- •40. Организмде жүретін биологиялық процесстерді (репликация, транскрипция) нанотехнологияда қолданылуы.
- •42. Нанотехнологияда қолданылатын физика-химиялық әдістер. Олардың мүмкіншіліктері (электрофорез, гельфильтрлеу, гендік инженерия әдістері, т.Б)
- •43. Гидроксиапатиттің алу жолы. Оның негізінде жасалған нанокомпозиттерді қандай салаларды қолданады?
- •49. Фуллерендердің алу әдістері.
- •50.Нанороботтар. Ассемблер, дессемблер. Нанотехнологияда қолдануы.
- •51. Нанотехнология мен бағаналы клеткалар, жетістіктері мен болашағы.
- •54.Жана Нанодәрілік препараттар жасау, адрестік жеткізу мен пролонгация проблемалары.
- •55. Биоминералдану. Табиғаттағы биоминералдану және биоминерализацияның наномедицинада қолданылуы.
- •56.Нанотехнологияда қолданатын биопроцестер.
- •57.Реттеу параметрі. Мицелла, везикула түзілу үшін реттеу параметрінің мәні қандай болуы тиіс?
- •58. Супрамолекулярлы құрылыстардың алу жолдары, қолдануы.
- •59.Көміртекті құрылымдардың (графит, графен, карбин, фуллерен, нанотүтікшелер) сипаттамаларын беріңіз.
12.Макромолекулалар (белоктар, нуклеин қышқылдары, липидтер, көмірсулар).
БЕЛОКТАР (ақуыздар, протеиндер) грек тілінде «бірінші» деген мағынаны білдіреді) - жоғары молекулалық полимерлі заттар, гидролизге түскенде аминқышқылдарына ыдырайды. Белоктардың құрамына 20 амин қышқылының қалдығы кіреді. БЕЛОКТАР – тіршіліктің көзі, бүкіл тірі организмдердің құрамына кіретін заттардың ең маңыздыларының бірі. Организмде көптеген қызметтерді атқарады. Белоктардың организмде атқаратын қызметтері (функциялары): Құрылыс - белоктар протоплазманың негізін құрайды, липидтер мен бірге олар клеткалар мен органеллалардың мембраналарын түзеді; Каталитикалық - барлық биохимиялық құбылыстар ферменттердің қатысымен жүреді; Қозғалтатын - қозғалу, бұлшық еттердің жыйырылып-созылуы; Транспорттық - оттегі транспорты (гемоглобин, миоглобин), альбумин (май қышқылдарын, органикалық заттарды мембранадан тасымалдауы); Қорғаныс - антиген-антитело, тромбин - қан ұйуы, муциндер - асқазан мен шек клеткаларының қабырғасы; Гормондық - гормондар (инсулин, вазопрессин); Қоректік - сүттегі казеин, жұмыртқадағы овальбумин; Сүйеу - сүйектер, шеміршектер, буын сүйектері; Рецепторлық – әр түрлі заттарды танып, байланыстыруы (гликопротеидтер); Белоктар - регуляторлар, белоктар - ингибиторлар.Белоктардың молекулаларында аминқышқылдарының қалдықтары өзара бiрiмен-бiрi байланысып полипептидтiк тiзбекті құрады. Полипептидтік тізбекте бір аминқышқылының карбоксил тобының көміртек атомы екінші аминқышқылының NН2 –тобының азот атомы коваленттік байланысады. Бұл байланысты (-СО-NH-) пептидтiк байланыс деп атайды.
NН2-СН-СООН + NH2-СН2-СООН NН2-СН-СО-NH-СН2-СООН +Н2О
| |
СН3 СН3
Аланин Глицин Аланил-глицин
Полипептидтiк тiзбек бiр белгiлi бағытта жазылады, оң жақта бос NН2-тобы бар, сол жақта бос СООН-тобы бар аминқышқылының қалдығы орналасады.
Полипептидтiк тiзбектi үнемi қайталанатын (NH-СН-СО) және өзгерiске ұшырайтын (R - бүйiрлiк топтары) бөлiктерге бөлуге болады. Белок молекуласының құрылымы 1. Белоктың бiрiншi реттiк құрылымы – полипептидтiк тiзбекте аминқышқылдарының белгiлi бiр ретпен жалғасып орналасуы. 2 Белоктың екiншi реттiк құрылымы – полипептидтiк тiзбекте жақын орналасқан аминқышқылы қалдықтарының кеңiстiкте өзара құрылысы. 3. Белоктың үшiншi реттiк құрылымы – полипептидтiк тiзбекте алыс орналасқан аминқышқылы қалдықтарының кеңiстiкте құрылысы. 4. Белоктың төртiншi реттiк құрылымы – екi, үш, төрт немесе одан да көп полипептидтiк тiзбектерден (суббөлiктерден) құрылған белок молекуласында суббөлiктердiң кеңiстiкте өзара орналасуы.
Нуклеин қышқылдары –клетканың ядросында табылған жоғары молекулалық қосылыстар. Нуклеин қышқылдарының молекулалары – тiзбектi полимерлер.
ДНҚ-ның бiр молекуласы клетканың ядролық бөлiгiнде орналасқан. Диплоидті эукариоттардың клеткаларында ДНҚ – негiзiнен, клетканың ядросында, шағын ғана мөлшерi цитоплазмада және митохондрияда орналасқан. Ядрода орналасқан ДНҚ молекуласы гистондармен байланысқан. Гистондар – бұл негiздiк қасиетi бар белоктар.
Нуклеин қышқылдары – генетикалық мәлiметтi сақтау және оны ұрпақтан-ұрпаққа тарату (негiзгi қызметі). Ағзада қызмет атқаратын белоктардың молекулаларындағы аминқышқылдарының ретпен орналасуы туралы мәлiмет нуклеин қышқылының құрылымында жазылған. Нуклеин қышқылдары екi топқа бөлiнеді:
-дезоксирибонуклеин қышқылдарына (ДНҚ)
-рибонуклеин қышқылдарына (РНҚ).
ДНҚ молекуласы барлық тiрi ағзада генетикалық ақпаратты сақтаушы. ДНҚ молекуласында жазылған мәлiмет делдал-молекула арқылы белок
молекулаларына берiледi.
13.Қатты, саңылаулы материалдар. Қатты денелер сұйықтар сияқты өзінің көлемін ғана сақтап қоймайды, сонымен бірге пішінін де сақтай алады. Олар негізінен кристалл күйде болады. Табиғатта және техникада кездесетін қатты материалдардың көпшілігі – поликристалдар. Олар ретсіз орналасқан ұсақ кристалдан (кристалиттер) құралады. Бұған көптеген минералдар, металдар мен қорытпалар жатады. Кристалдың жеке ірі түрі монокристалл деп аталады. Табиғатта салмағы жүздеген кг-ға жететін кварц, дала шпаты, флюорит кристалымен қатар мөлшері өте ұсақ алмас кристалы да кездеседі. Молекула-кинетикалық теориядағы термодинамикалық тепе-теңдік жағдайда өсірілген кристалдың пішіні белгілі бір симметриялы, дұрыс көпжақ түрінде болады. Олардың жақтары жазық болып келеді де, қырлары түзу сызық бойымен тұрақты бұрыш жасай қиылысады, яғни кристалдану кезінде кристалдың жақтары өзіне-өзіпараллель жылжиды. Бұл заңдылық кристаллографияда бұрыштардың тұрақтылық заңы деп аталады. Кристалдар қатты денелердің тепе-теңдік күйі болып табылады. Белгілі бір термодинамикалық жағдайда (қысым, температура) кристалдық күйде болатын заттың нақты, тек өзіне тән кристалдық атомдық құрылымы болады. Бұл құрылым атомдардың орналасуына байланысты кристалдардың сыртқы симметриясын және олардың анизотропиялық қасиеттерін бейнелейді. Нанокеуекті материалдардың кеуектерінің өлшемдері, әдетте, 100 нм-ден кіші болады.Бұл цеолиттік және цеолит тәрізді, және де каналдары мен қуыстары кеңістікте қайталанатын, газдарды диффузиялық бөлуге және функционалдық арналымы бар нанобөлшектерді орналастыруға және стабилизациялауға (катализге арналған төсеніштер, эмиттерлер, датчиктер) арналған көміртекті және полимерлік наноқұрылымдар. Нанокеуекті материалдарды алудың технологиялық амалдары көп түрлі: гидротермалды синтез, золь-гель-процестері, электрохимиялық әдістер, карбидті материалдарды хлормен өңдеу және т.б. Түрлі ұялы структуралар стандартты литография (болашақ тордың суретін түсіру), сілтілік травление, анодтық еріту, тотығу-қайта қалпына келу және т.б. әдістерінің түрлі комбинациясымен алынады. Полимерлер, диэлектриктер мен жартылай өткізгіштерді жоғары энергиялы иондармен өңдегенде нанофильтрлер, наношаблондар және т.б. алуға қолданатын наноөлшемді иондық тректер пайда болады.
АҚШ-та жасалған каналдарының өлшемі 2-ден 10 нм-ге дейінгі МСМ-41 нанокеуекті материалдар автоклавта 150°С температурасында 48 сағ өңделген ерітіндіден (натрий мен алюминий силикаттары және беттік-активті қоспалары бар) алынады, соңынан жуылып, кептіріліп, 540°С температурасында азот және ауа атмосфераларында өңделеді. Бұл технологиямен гексагоналды орналасқан каналдарының ішінде мицеллдер (тетра-алкиламмоний қоспалары) бар сұйықкристалды темплаттарды да алуға болады. Мицелдер қыздырғанда кетеді, ал силикат каналдар айналасындағы кеңістікті толтырады (сур. 11.4). Цеолитті типіндегі нанокомпозитті молекулярлық ситоларға тиісті осындай матрицалық структуралар алудың екі әдісін айырады: болашақ композиттің нанобөлшектері бар кеуекті материалдың гельден кристаллизациялануы, және цеолиттерге алдын-ала енгізілген прекурсорлардан in situ нанобөлшектердің синтезі
С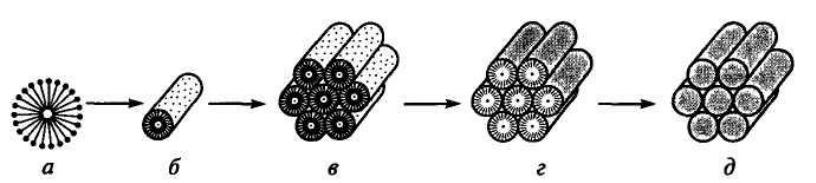 ур.
11.4.
МСМ-41 нанокеуекті материалды алу схемасы:
ур.
11.4.
МСМ-41 нанокеуекті материалды алу схемасы:
а - беттік-активті мицелла (СnН2n+1)3N;
б - мицеллярлық стержень; в – гексагоналды жинақ;
г - гексагоналды силикатты жинақ; д – күйдіргеннен кейінгі МСМ- 41
