
- •1.Суть и значение цтк.
- •2 .Основные пути распада углеводов.
- •3. Критерии радиочувствительности живых организмов. Оценка биологического риска облучения в малых дозах.
- •4. Биосинтез белка состоит из трех этапов – инициации, элонгации и терминации.
- •8.Законы термодинамики в биологии, доказательства их применимости к живым системам.
- •9.Строение, основные характеристики атф и др. Макроэргических соед. Живых организмов.
- •12.Направления в эволюции онтогенеза. Целостность организма в онтогенезе.
- •14.Главные направления эволюции филогенетических групп.
- •13.Основные структурные компоненты эукариотической клетки и их функции.
- •15.Хромосомная теория наследственности. Наследование признаков сцепленных с полом. Группы сцепления генов. Кроссинговер. Генетическая карта хромосом.
- •16.Особенности организации клеток прокариот, грибов, растений и животных.
- •17.Вид: критерии, признаки, структура. Пути видообразования.
- •18.Мутационный процесс. Молекулярные механизмы мутации. Классификация мутаций.
- •22.Пролиферация клеток, клеточные циклы.
- •24.Законы наследования при моно -, ди- и полигибрндном скрещивании.
- •25.Структура и функции гена.
- •26.Принципы и методы генетического анализа про - и эукариот.
- •28.Генотип как сложная система аллельных и неаллельных взаимодействий.
- •30.Репликация днк. Принцип комплементарности и его биологическая роль.
- •36.Мир м/о, общие признаки и разнообразие. Про- и эукариотические м/о.
- •37.Строение, химический состав и функции основных компонентов бактериальной кл.
- •38.Закономерности роста чистых бактериальных культур.
- •39.Метаболизм бактерий. Виды и основные назначения метаболических реакций.
- •40.Типы энергетического метаболизма у бактерий.
- •42.Биотехнология: сырьевая база, основные объекты и способы получения целевых продуктов биотехнологических процессов. Успехи и перспективы современной б/т.
- •45.Бактериофаги. Вирулентные и умеренные бактериофаги.
- •4 6.Типы жизненных циклов зелёных водорослей и параллелизм в развитии.
- •47.Отделы высших споровых растений и их жц.
- •48.Общая характеристика покрытосеменных, их классификация.
- •50.Характеристика грибов как отдельного царства органического мира.
- •51.Индивидуальное развитие покрытосеменных.
- •52.Водоросли. Отличия от высших растений. Основные типы морфоструктуры тела.
- •53.Лишайники (Lichenophyta): строение, питание, размножение. Роль в биогеоценозе.
- •54.Особенности высших растений как результат приспособления к жизни на суше.
- •62. Рост и развитие растений. Механизмы регуляции роста растений.
- •63. Структурная организация фотосинтетического аппарата.
- •64. Пигменты растений их функциональная роль.
- •65. Метаболизм углерода в процессе фотосинтеза, различные пути метаболизма, их особенности.
- •67. Минеральное питание растений. Физиологю роль, механизмы их поступления в клетку.
- •70.Вторичная полость тела, её функции и развитие.
- •74.Эндокринная система и её регуляторные функции.
- •75.Ранние ст. Зародыш. Развития (дробление, гаструляция, нейруляция). Органогенез.
- •76.Система пищеварения. Регуляция пищеварения.
- •77.Система кровообращения и её регуляция.
- •78.Внутренняя среда организма и гомеостаз.
- •Плазма крови. В 1 л плазмы содержится 900 г воды, 80 г белка и 20 г низкомолекулярных соединений.
- •80.Система дыхания у животных и человека. Регуляция дыхания.
- •85.Характеристика подтипа Позвоночных (Черепных)
- •86.Морфо-функциональные изменения основных систем
- •88.Земноводные. Морфобио адаптация к обитанию в водной и наземно-возд. Среде.
- •93.Эволюция наружного скелета конечностей, сегментация членистоногих
- •89.Морфо-функциональные и биологические приспособления членистоногих для жизни в воздушной среде.
- •91.Морфо-биологическай характеристика первичноводных челюстных позвоночных.
- •92.Паразитизм как обитание в среде второго порядка. Биологические выгоды паразитизма и адаптация экто- и эндопаразитов.
- •94.Метагенез и гетерогония как типы жизненных циклов беспозвоночных животных.
9.Строение, основные характеристики атф и др. Макроэргических соед. Живых организмов.
М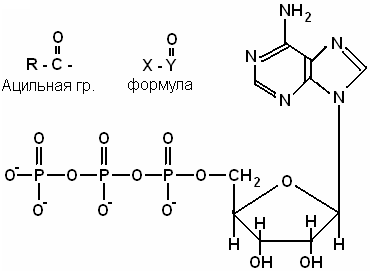 акроэргические
соед.
- природные соед-ия, содерж. богатые Е -
макроэргические
св;
присутствуют во всех живых кл., уч. в
пр-сах накопления и превращения Е. К М.
с. относятся главным образом АТФ и в-ва,
способные обр. АТФ в ферментативных
реакциях переноса преимущественно
фосфатных гр. Все известные М. с. сод.
фосфорильную (— PO2-3
/ ацильную) и описываются формулой X-Y=O,
где Х
— атом N,
О, S
/ С,
а Y
— атом Р / С.
Реакционная способность Макр.
соед. Связ-ся.
с повышенной электрофильностью (сродством
к е-) атома Y,
что обусловливает высокую свободную Е
гидролиза М. с., = 25,1—58,6 кДж/моль. К М.
с. относятся также нуклеозидтри-,
дифосфорные к-ты, пирофосфорная и
полифосфорная к-ты, креатинфосфорная,
фосфоПВК, дифосфоглицериновая
к-ты,
ацетил- и сукцинилкоферменты А и др. АТФ
- это сокр. назв. аденозинтрифосфорной
кислоты. АТФ содержится в каждой кл.
жив. и раст. Кол-во АТФ колеблется и в
ср. сост. 0,04% (на сыр. массу кл.). Наи>
кол-во АТФ содерж. в скелетных мышцах –
0,2 – 0,5%. Молекула АТФ представляет собой
нуклеотид, образованный азотистым
основанием аденином, пятиуглеродным
сахаром рибозой и тремя остатками
фосфорной кислоты. Фосфатные группы
между собой соединены высокоэнергетическими
связями. Они не очень прочные, и при их
разрыве выделяется большое количество
энергии. В результате гидролитического
отщепления от АТФ фосфатной группы
образуется АДФ и высвобождается порция
энергии. АДФ тоже может подвергаться
дельнейшему гидролизу с отщеплением
еще одной фосфатной группы и выделением
второй порции энергии; при этом образуется
АМФ, который далее не гидролизуется.
Реакция отщепления каждой молекулы
фосфорной кислоты от АТФ сопровождается
большим Е эффектом и освобождением
почти 40 кДж (при отщеплении 2ой – 40, 3ей
– 13,8 кДж). АТФ и АДФ сод. макроэргические
связи
(~).
В АТФ им. 2 макроэргические связи. Однако,
АТФ не самое богатое соед. в кл. Те в-ва
при гидролизе кот. выделяется > Е, чем
при гидролизе АТФ, способны перенос.
свои фосфатные гр. на АДФ с обр. АТФ; а
те, при гидролизе кот. выделяется < Е,
будут присоед. фосфатные гр. от АТФ.
акроэргические
соед.
- природные соед-ия, содерж. богатые Е -
макроэргические
св;
присутствуют во всех живых кл., уч. в
пр-сах накопления и превращения Е. К М.
с. относятся главным образом АТФ и в-ва,
способные обр. АТФ в ферментативных
реакциях переноса преимущественно
фосфатных гр. Все известные М. с. сод.
фосфорильную (— PO2-3
/ ацильную) и описываются формулой X-Y=O,
где Х
— атом N,
О, S
/ С,
а Y
— атом Р / С.
Реакционная способность Макр.
соед. Связ-ся.
с повышенной электрофильностью (сродством
к е-) атома Y,
что обусловливает высокую свободную Е
гидролиза М. с., = 25,1—58,6 кДж/моль. К М.
с. относятся также нуклеозидтри-,
дифосфорные к-ты, пирофосфорная и
полифосфорная к-ты, креатинфосфорная,
фосфоПВК, дифосфоглицериновая
к-ты,
ацетил- и сукцинилкоферменты А и др. АТФ
- это сокр. назв. аденозинтрифосфорной
кислоты. АТФ содержится в каждой кл.
жив. и раст. Кол-во АТФ колеблется и в
ср. сост. 0,04% (на сыр. массу кл.). Наи>
кол-во АТФ содерж. в скелетных мышцах –
0,2 – 0,5%. Молекула АТФ представляет собой
нуклеотид, образованный азотистым
основанием аденином, пятиуглеродным
сахаром рибозой и тремя остатками
фосфорной кислоты. Фосфатные группы
между собой соединены высокоэнергетическими
связями. Они не очень прочные, и при их
разрыве выделяется большое количество
энергии. В результате гидролитического
отщепления от АТФ фосфатной группы
образуется АДФ и высвобождается порция
энергии. АДФ тоже может подвергаться
дельнейшему гидролизу с отщеплением
еще одной фосфатной группы и выделением
второй порции энергии; при этом образуется
АМФ, который далее не гидролизуется.
Реакция отщепления каждой молекулы
фосфорной кислоты от АТФ сопровождается
большим Е эффектом и освобождением
почти 40 кДж (при отщеплении 2ой – 40, 3ей
– 13,8 кДж). АТФ и АДФ сод. макроэргические
связи
(~).
В АТФ им. 2 макроэргические связи. Однако,
АТФ не самое богатое соед. в кл. Те в-ва
при гидролизе кот. выделяется > Е, чем
при гидролизе АТФ, способны перенос.
свои фосфатные гр. на АДФ с обр. АТФ; а
те, при гидролизе кот. выделяется < Е,
будут присоед. фосфатные гр. от АТФ.
(гидролиз АТФ): 1) в результате дыхательной активности (Е поступает за счет дыхания); 2) за счет др. высокоЕ соед-ния, например, креатинфосфата (43,3 кДж), кот. нах в мышечных кл. Если весь АДФ мыш. кл. превращается в АТФ, то фосфат от АТФ переносится на креатин с обр. креатинфосфата. При этом вновь появл. нек. кол-во АДФ, кот. может, присоединив фосфат, образ. АТФ. При понижении ур. АТФ происходит обратный процесс: фосфат переносится от креатинфосфата на АДФ с обр. АТФ. 3) фосфорилирование, протекающее в хлорофилл-содерж. кл. зел. раст. В конце световой фазы ф/с, когда протоны протоны ч/з протонный канал в АТФ-синтазе выходят наружу – в строму. На выходе из протонного канала создается высокий ур. Е, кот. идет на синтез АТФ из АДФ и Фн.
В целом биозначение АТФ и св. с ней М. с. обусловлено их центральным положением на пересечении путей обмена в-в и Е: они обесп. осущ. разл. видов А, иг. ответственную роль в ф/с, биолюминесценции, в б/с Б, Ж, У, НК и др. прир. соед-ий. АТФ- универсальный носить Е, т.к. он сод. во всех живых кл. и способен доставлять хим. Е в любую часть кл. АТФ - важнейший лабильный переносчик энергии. Конечный продукт трех основных процессов: гликолиз, окислительное фосфорилирование, фотосинтетическое фосфорилирование. УТФ, ГТФ, ЦТФ – образуются из АТФ. Все иные фосфорилированные соединения с макроэргическим потенциалом разделяются на 3 группы:
Предшественники в процессах биосинтеза: ди- и трифосфаты в синтезе ДНК и РНК, аденилаты аминокислот и др.
Резервные вещества: креанинфосфат, аргининфосфат.
Предшественники АТФ: 1,3 дифосфоглицериновая кислота (в гликолизе), ацетилфосфат (у бактерий), ацилтиоэфиры (ацетил коэнзим А).
АТФ чрезвычайно быстро обновляется. Синтез АТФ происходит главным образом в митохондриях и хлоропластах.
10.Проницаемость и транспорт молекул и ионов через биомембраны. Кл-ия типов транспорта.
В настоящее время общепринятыми являются представления о том, что ионы и различные вещества преодолевают мембрану несколькими способами, основные из которых:
1. Простая диффузия через липидную фазу, если вещество растворимо в липидах (это не ионы).
2. Облегченная диффузия гидрофильных веществ с помощью липофильных переносчиков (тр-ров)
3. Простая диффузия ионов через гидрофильные поры (например, через ионные каналы).
4. Перенос веществ с участием активных комплексов (насосов).
5. Транспорт веществ путем пиноцитоза в условиях существенных изменений архитектуры мембран.
Пассивный транспорт – перемещение веществ путем диффузии по градиенту электрохимического потенциала (простая и, в какой-то мере, облегченная диффузия). Активный транспорт – перемещение веществ против градиента электрохимического потенциала с затратой метаболической энергии, как правило в форме АТФ или редокс-цепей.
Ионные каналы формируются интегральными (обычно субъединичными) белками. Они пронизывают мембрану таким образом, что образуется гидрофильная пора. Канал – это белковая макромолекула, образующая пору через двухслойную липидную мембрану. Основные структурные элементы канала: устье – расширенная часть поры, которая находится по обеим сторонам мембраны; узкая часть поры – туннель. Одной из важнейших характеристик ионных каналов является селективность, обусловленная особенностью их строения: диаметром канала, природой и размещением заряженных групп. Большое значение при этом имеют заряды, локализованные непосредственно у входа в канал, где они выполняют функцию селективного фильтра.
Система облегченного транспорта (переносчики).
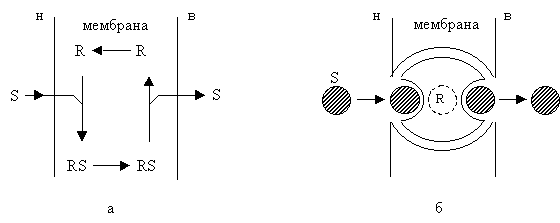
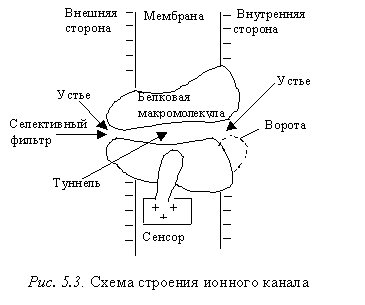
|
Процесс передвижения переносчика с ионом и самого переносчика с одной стороны мембраны на другой, который проходит без затраты энергии по законам диффузии, называют облегченной диффузией. В основе облегченной диффузии лежит обратное связывание транспортируемого иона с белком переносчиком, который проходит через мембраны с освобождением иона на другой ее стороне. Переносчики бывают подвижные и фиксированные.
В настоящее время рассматривают следующие типы активного транспорта веществ.
1. Первичный активный транспорт – трансмембранный векторный перенос иона происходит непосредственно в ходе энергетического превращения в АТФазных системах или ЭТЦ (используется или энергия АТФ или ОВ реакций): а) электрогенный активный транспорт – первичный активный трансмембранный перенос ионов во время АТФазной или ОВ реакций, которые сопровождаются генерацией электрического потенциала; б) электронейтральный активный транспорт – первичный активный трансмембранный перенос ионов во время АТФазной или ОВ реакций, который не сопровождается генерацией электрического потенциала (например, Н+/K+ обмен при стехиометрии 1:1).
2. Вторичный активный транспорт – происходит, когда в качестве энергетического источника используются градиенты других ионов. Например, электрохимический градиент ионов Н+ для сопряженного транспорта анионов, сахаров, аминокислот и т. д. (симпорт или котранспорт), или, напротив, для вывода ионов Na+ из клетки (антипорт).
|
|
