
- •1.Суть и значение цтк.
- •2 .Основные пути распада углеводов.
- •3. Критерии радиочувствительности живых организмов. Оценка биологического риска облучения в малых дозах.
- •4. Биосинтез белка состоит из трех этапов – инициации, элонгации и терминации.
- •8.Законы термодинамики в биологии, доказательства их применимости к живым системам.
- •9.Строение, основные характеристики атф и др. Макроэргических соед. Живых организмов.
- •12.Направления в эволюции онтогенеза. Целостность организма в онтогенезе.
- •14.Главные направления эволюции филогенетических групп.
- •13.Основные структурные компоненты эукариотической клетки и их функции.
- •15.Хромосомная теория наследственности. Наследование признаков сцепленных с полом. Группы сцепления генов. Кроссинговер. Генетическая карта хромосом.
- •16.Особенности организации клеток прокариот, грибов, растений и животных.
- •17.Вид: критерии, признаки, структура. Пути видообразования.
- •18.Мутационный процесс. Молекулярные механизмы мутации. Классификация мутаций.
- •22.Пролиферация клеток, клеточные циклы.
- •24.Законы наследования при моно -, ди- и полигибрндном скрещивании.
- •25.Структура и функции гена.
- •26.Принципы и методы генетического анализа про - и эукариот.
- •28.Генотип как сложная система аллельных и неаллельных взаимодействий.
- •30.Репликация днк. Принцип комплементарности и его биологическая роль.
- •36.Мир м/о, общие признаки и разнообразие. Про- и эукариотические м/о.
- •37.Строение, химический состав и функции основных компонентов бактериальной кл.
- •38.Закономерности роста чистых бактериальных культур.
- •39.Метаболизм бактерий. Виды и основные назначения метаболических реакций.
- •40.Типы энергетического метаболизма у бактерий.
- •42.Биотехнология: сырьевая база, основные объекты и способы получения целевых продуктов биотехнологических процессов. Успехи и перспективы современной б/т.
- •45.Бактериофаги. Вирулентные и умеренные бактериофаги.
- •4 6.Типы жизненных циклов зелёных водорослей и параллелизм в развитии.
- •47.Отделы высших споровых растений и их жц.
- •48.Общая характеристика покрытосеменных, их классификация.
- •50.Характеристика грибов как отдельного царства органического мира.
- •51.Индивидуальное развитие покрытосеменных.
- •52.Водоросли. Отличия от высших растений. Основные типы морфоструктуры тела.
- •53.Лишайники (Lichenophyta): строение, питание, размножение. Роль в биогеоценозе.
- •54.Особенности высших растений как результат приспособления к жизни на суше.
- •62. Рост и развитие растений. Механизмы регуляции роста растений.
- •63. Структурная организация фотосинтетического аппарата.
- •64. Пигменты растений их функциональная роль.
- •65. Метаболизм углерода в процессе фотосинтеза, различные пути метаболизма, их особенности.
- •67. Минеральное питание растений. Физиологю роль, механизмы их поступления в клетку.
- •70.Вторичная полость тела, её функции и развитие.
- •74.Эндокринная система и её регуляторные функции.
- •75.Ранние ст. Зародыш. Развития (дробление, гаструляция, нейруляция). Органогенез.
- •76.Система пищеварения. Регуляция пищеварения.
- •77.Система кровообращения и её регуляция.
- •78.Внутренняя среда организма и гомеостаз.
- •Плазма крови. В 1 л плазмы содержится 900 г воды, 80 г белка и 20 г низкомолекулярных соединений.
- •80.Система дыхания у животных и человека. Регуляция дыхания.
- •85.Характеристика подтипа Позвоночных (Черепных)
- •86.Морфо-функциональные изменения основных систем
- •88.Земноводные. Морфобио адаптация к обитанию в водной и наземно-возд. Среде.
- •93.Эволюция наружного скелета конечностей, сегментация членистоногих
- •89.Морфо-функциональные и биологические приспособления членистоногих для жизни в воздушной среде.
- •91.Морфо-биологическай характеристика первичноводных челюстных позвоночных.
- •92.Паразитизм как обитание в среде второго порядка. Биологические выгоды паразитизма и адаптация экто- и эндопаразитов.
- •94.Метагенез и гетерогония как типы жизненных циклов беспозвоночных животных.
4. Биосинтез белка состоит из трех этапов – инициации, элонгации и терминации.
На этапе инициации происходит сборка белок синтезирующей системы. Она начинается с присоединения малой единицы рибосомы 5, концу и-РНК. После присоединения малая единица рибосомы сканирует нуклеотидную последовательность, передвигаясь от 5 конца к 3 концу. После распознавания стартового кодона и связывания инициирующей т-РНК субъединицы соединяются в полную рибосому.
Этап элонгации представляет собой собственно процесс синтеза полипептида. Он состоит из трех этапов. Этап связывания состоит в распознавании и удержании клеверного листка т-РНК. Транспептидация. Т-РНК в реакционном центре взаимодействует с пептидил т-РНК, таким образом, что происходит перенос с-конца полипептида из реакционного центра в А-центр.
Стадия транслокации: рибосома обеспечивает перенос пептидил т-РНК и А-центра
Рибосома
локализована в цитоплазме эукариотической
клетки. Значительная часть рибосом
прикреплена к ЦПМ. Синтез белка происходит
на свободных рибосомах. Рибосома состоит
из 2-х субъединиц: малой и большой. Малая
субъединица состоит из головки, тела и
бокового выступа. Большая субъединица
состоит из РНК и белко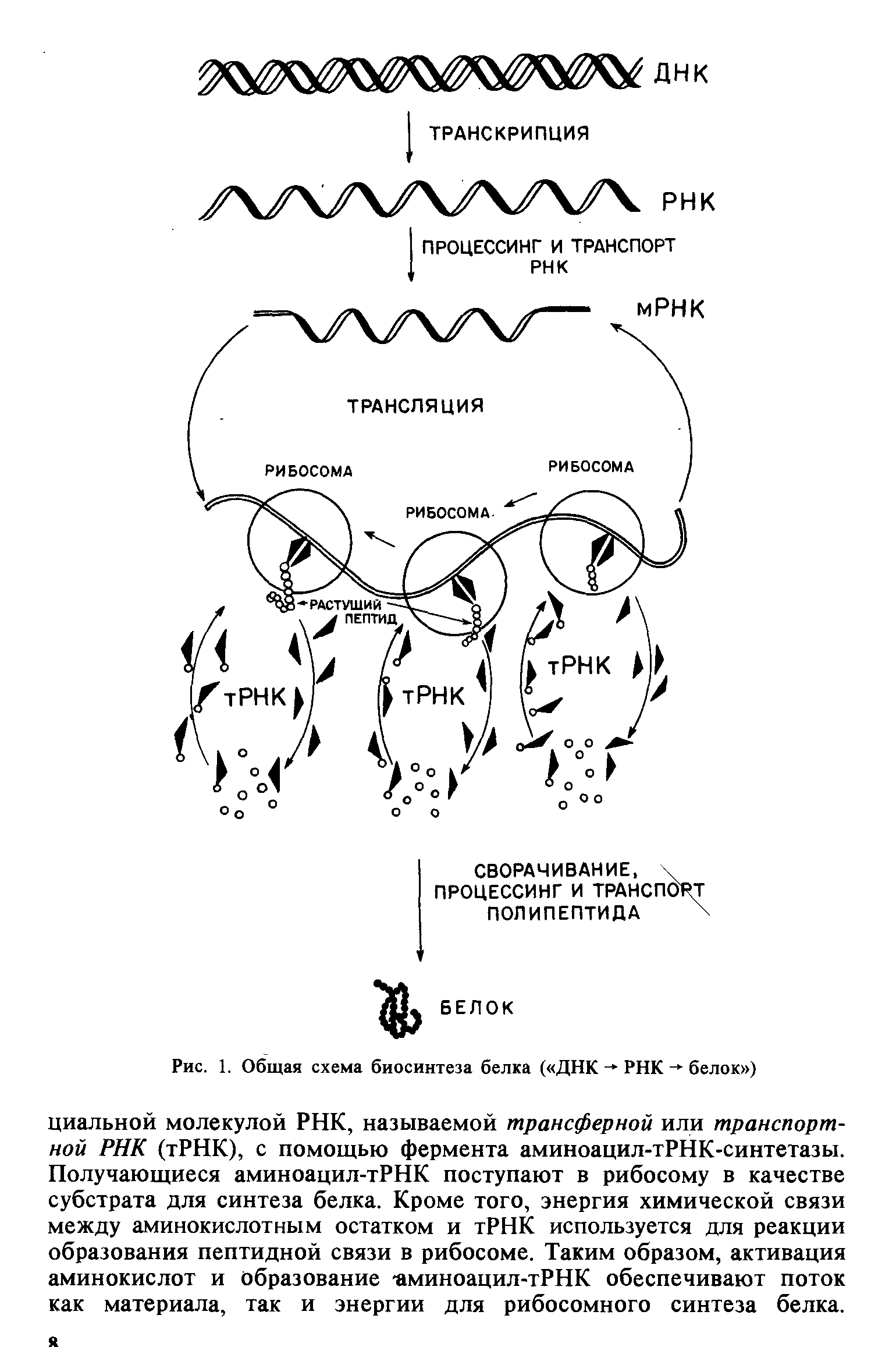 в.
Рибосома является организатор.биосинтеза
белка.
в.
Рибосома является организатор.биосинтеза
белка.


Рибосомы – открыты у всех растений и животных. Рибосомы – органеллы немембранного строения. По строению – сферические частицы 20 – 30 нм.
Состоят из 2-х субъединиц (большой и малой). Субъединицы образуются в ядре, а собираются в ядрышке, и через поры ядерных оболочек поступают в цитоплазму.
Находятся рибосомы в ЭПЦ (шероховатой), митохондриях, пластидах, цитоплазме.
Функция рибосом: биосинтез белка.
5.Метаболизм липидов. Окисление жирных кислот.
Жиры (триацилглицерины) — наиболее важный резерв Е в организме жив. Они хранятся гл. обр. в кл. жировой тк, адипоцитах. Там же они уч. в постоянно происх. процессах обр. и деградации.
ЖК, необходимые для синтеза жиров (липогенеза), в составе триацилглицеринов переносятся из печени и кишечника в виде липопротеиновых комплексов. Липопротеин-липаза, нах. на пов-сти эндотел. кл. кровеносных капилляров, отщепляет от этих липопротеинов ЖК. В адипоцитах деградация жиров (липолиз) катализируется гормонзависимой липазой. Ур. свободных ЖК, поступающих из жировой тк, зависит от активности этой липазы — Ф регулирует т.о. ур. ЖК в плазме. ЖК из жировой тк. транспорт. в плазму крови в неэтерифицированной форме. При этом растворимы только короткоцепочечные ЖК, а ЖК с >длинными цепями, < растворимые в воде, переносятся в комплексе с альбумином.
Деградация жирных кислот в печени.
ЖК поступают из плазмы крови в тк; здесь из них синтез. жиры / за счет окисления получается Е. Особенно интенсивен метаболизм ЖК в кл. печени (гепатоцитах). Наиболее сл. процессом деградации ЖК явл. β-окисление в митохондриях. При этом ЖК вначале активируются в ЦП, присоединяясь к коферменту А. Затем они с помощью транспортной системы попадают в митохондриальный матрикс, где разрушаются в результате β-окисления до ацетил-КоА. Образующиеся ацетильные остатки полностью окисляются до СО2 в ЦТК с освобождением Е в виде АТФ. После попадания в кл. ЖК активир. путем обр. ацил-КоА. Для этого нужны 2 богатые Е св. АТФ. В матрикс митохондрий активир. ЖК попадают в виде ацилкарнитина, кот. явл. трансМ переносчиком. Деградация ЖК происх. в митохондриальном матриксе путем окислительного цикла реакций, при кот. послед-но отщепляются С2-звенья в виде ацетил-КоА. Последовательное отщепление ацетильных групп начинается с карбоксильного конца активированных ЖК каждый раз между С-2 (α-атомом) и С-3 (β-атомом). Поэтому цикл реакций деградации наз. β-окислением. 1.ст. — дегидрирование активированной ЖК (ацил-КоА) с обр. β-ненасыщ. ЖК с = в транс-конфигурации (дегидрирование). При этом оба атома Н с электронами переносятся на электронпереносящий флавопротеин (ETF). ETF-дегидрогеназа переносит их на убихинон (кофермент Q), кот. явл. составной частью дыхательной цепи. 2. - присоед. молекулы воды к двойной связи ненасыщенной ЖК (гидратирование). На 3 ст. происх. окисление гидроксильной группы при С-3 в карбонильную группу (дегидрирование). Акцептором для Н и е- явл. НАД+, кот. передает их в дыхательную цепь. На 4 ст. активированная β-кетокислота расщепляется ацилтрансферазой в присутствии кофермента А (тиолитическое расщепление). Продуктами реакции являются ацетил-КоА и активированная ЖК, углеродная цепь кот. короче на 2 атома С по сравнению с длиной цепи исх. ЖК. Для полной деградации длинноцепочечной ЖК цикл должен многокр. повтор.; Образующийся ацетил-КоА может переноситься на оксалоацетат с обр. цитрата, промежуточного метаболита ЦТК. При избытке ацетил-КоА в печени обр. кетоновые тела.
Синтез жирных кислот в печени.
Биосинтез ЖК протекает в ЦП, в осн. в печени, жир. тк, почках, легких и молочных железах. Гл. ист. атомов С явл. Глю, м.б. и др. предшественники ацетил-КоА (а.к.).
Первая стадия — карбоксилирование ацетил-КоА с обр. малонил-СоА — катализируется ацетил-КоА-карбоксилазой, ключевым Ф биосинтеза ЖК. Создание длинноцепочечных ЖК осущ. синтазой жирных кислот. Исходя из молекулы ацетил-КоА под действием этого Ф, цепь удлиняется (процесс вкл. 7 реакций) путем добавления малонильных групп и отщепления СО2 (в каждой реакции) с обр. пальмитата. В результате каждой реакции молекула удлиняется на 2 атома С. В качестве восстановителя исп. НАДФН + Н+, обр. в ПФП. Удлинение цепи ЖК на синтазе жирных кислот заканчивается на C16, т.е. на пальмитиновой кислоте (16:0). В последующих реакциях пальмитат исп. в качестве предшественника для получения ненасыщенных / более длинноцепочечных ЖК. Дальнейший биосинтез жиров протекает с участием активированных ЖК (ацил-КоА) и 3-глицерофосфата. Для обеспечения др. тк. жиры в гепацитах упаковываются в липопротеиновые комплексы и поступают в кровь.
6.Действие ионизирующих излучений на живые организмы; стох. и нестох. эф. Действия бывают разные: соматическое; наследственное; стохастическое; нестохастическое. Т.о. радиационное поражение – это сложный многоэтапный процесс – стадии:
1) физическая – поглощение Е → возбуждение и ионизация атомов и молекул.
2) физико-химическая → появляются свободные радикалы – это нейтральные атомы или молекулы, которые имеют неспаренные электроны → очень активны!
3) химическая → появляются поврежденные радикалы – вторичные, появляется прямое и косвенное действие радиации. Прямое действие – молекула получает Е, которая ее повреждает.
Косвенное действие – молекула получает Е от другой молекулы (от ионизированных)
4) биомолекулярные повреждения – повреждения жизненно важных молекул в клетке.
Стадии 1-3 – это первичные стадии, стадия 4 – биохимическая стадия, увеличивающая тяжесть повреждений.
5) стойкие физиологические изменения – отдаленные биологические эффекты, повреждения формируются на всех уровнях организации живого (до биосферного!).
Процессы повреждения в клетке приводят к нарушению в обмене в-в, в функционировании макромолекул, которые ответственные за проявление биологических эффектов действия радиации. Эф. действия радиации на организмы чела и животного связан с условиями облучения:
1) доза; Уровень поглощения доз – чем выше доза, тем больше эффект.
2)Время – важное условие, т.к. параллельно идут процессы репарации. Если дозу растянуть во времени, то летального эффекта не будет.
3)При уменьшении мощности дозы происходит уменьшение биоэффекта. При малой мощности дозы скорость развития повреждения м. б. соизмерима со скоростью репарации. При увеличении мощности дозы значимость репарации уменьшается → биоэффект увеличивается.
4)Степень лучевого поражения зависит о того, подвергается ли все тело, или только его часть. Летальная доза только на часть может не приводить к летальному эффекту. т.е. от площади поверхности. При лучевой терапии опухолей это используется.
5)Эффект зависит от вида излучения, т.к. имеются различия в пространственном распределении поглощенной Е в тканях.
6) Внешнее – от наружных источников облучения, внутреннее – от инкорпорированных в организм радионуклидов. Внутреннее облучение опаснее:
наличие критического органа, где избирательно накапливаются радионуклиды (131I в щитов. ж.);
продолжительность облучения (выведение зависит от периода полураспада и биовыведения;
п
 ри
распаде образуются частицы, которые
обладают различной проникающей
способностью (α-частицы
опасны в легких, а в тканях и воздухе -
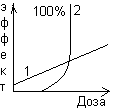
не опасны). (1)Стохастический
эффект
– с ↑ дозы облучения ↑ только частота
появления, но не тяжесть (индукция
злокачественных новообразований,
генетические изменения в потомстве
облученной особи). Линейная зависимость
доза-эффект; вероятность эффекта есть
при минимальных дозах!!!(2)Нестохастический
эффект
– с ↑ дозы облучения ↑ как частота
появления, так и тяжесть; обычно возникает
после превышения некоего дозового
порога; часто рассматривается как
ранний эффект облучения, однако, может
проявляться спустя многие годы после
воздействия. При низких дозах – нету,
но быстро становится 100% при превышении
порога. Примеры: лучевая болезнь (для
чела 1 Гр – пороговая доза, до 1 Гр –
болезни нету); лучевые ожоги; хроническая
лучевая болезнь (развитие катаракты,
минимум 2 Гр, чем ↑ доза, тем быстрее
проявляется; ↓ продолжительности жизни
(св. с ускорением процессов старения и
↑ восприимчивости к инфекциям).Есть
стимулирующие
эффекты
малых доз на живые объекты. Радиационный
гормезис
– обращение поражающего эффекта на
стимулирующий с ↓ дозы.
ри
распаде образуются частицы, которые
обладают различной проникающей
способностью (α-частицы
опасны в легких, а в тканях и воздухе -
не опасны). (1)Стохастический
эффект
– с ↑ дозы облучения ↑ только частота
появления, но не тяжесть (индукция
злокачественных новообразований,
генетические изменения в потомстве
облученной особи). Линейная зависимость
доза-эффект; вероятность эффекта есть
при минимальных дозах!!!(2)Нестохастический
эффект
– с ↑ дозы облучения ↑ как частота
появления, так и тяжесть; обычно возникает
после превышения некоего дозового
порога; часто рассматривается как
ранний эффект облучения, однако, может
проявляться спустя многие годы после
воздействия. При низких дозах – нету,
но быстро становится 100% при превышении
порога. Примеры: лучевая болезнь (для
чела 1 Гр – пороговая доза, до 1 Гр –
болезни нету); лучевые ожоги; хроническая
лучевая болезнь (развитие катаракты,
минимум 2 Гр, чем ↑ доза, тем быстрее
проявляется; ↓ продолжительности жизни
(св. с ускорением процессов старения и
↑ восприимчивости к инфекциям).Есть
стимулирующие
эффекты
малых доз на живые объекты. Радиационный
гормезис
– обращение поражающего эффекта на
стимулирующий с ↓ дозы.
Важнейшие реакции организма на действие ионизирующей радиации.
Соматические – если проявление в организме, подвергшемуся излучению
Наследственные – если проявляются повреждения генетического аппарата и проявляется в последующих поколениях потомков.
7. Физико-химическая организация биологических мембран: состав, строение, свойства и биологические фуекции.
Мембр. отделяют клеточное содержимое от внешней среды, регулируют обмен между клеткой и средой, делят клетки на отсеки, или компартменты, предназначенные для тех или иных специализированных метаболических путей. Некоторые химические реакции, в частности световые реакции фотосинтеза в хлоропластах или окислительное фосфорилирование при дыхании в митохондриях, протекают на самих мембранах. Здесь же на мембранах располагаются рецепторные участки для распознания внешних стимулов (гормоны и другие), поступающих из среды или из другой части самого организма. Плазмалемма контролирует поглощение и секрецию веществ, участвует в формировании клеточной стенки, выполняет рецепторную и осмотическую функции, а также функцию механической защиты у клеток, лишенных клеточных стенок.
Основным строительным материалом мембран являются белки и липиды. В основе соотношение их примерно 40 % липидов и 60 % белков. Однако у некоторых мембран это соотношение может быть и иным. В биологических мембранах липиды представлены главным образом фосфолипидами и стероидами. Все мембранные липиды обладают выраженной амфифильностью, т. е. в их структуре представлена полярная часть, обладающая сродством к воде, и неполярная, нерастворимая в воде. Именно благодаря этому липиды в воде образуют
мицеллы
– замкнутые структуры, в которых полярные
группы выставлены наружу, а неполярные
углеродные цепи спрятаны внутрь, и,
контактируя с друг с другом, прячутся
от воды. В торой
компонент мембран представлен белками.
Белки – высокомолекулярные соединения,
относящиеся к классу линейных биополимеров.
Они состоят из отдельных элементарных
единиц, в роли которых выступает 20
различных аминокислот. Все аминокислоты
амфолиты, объединяющие в себе положительно
заряженную аминогруппу NH3+
и отрицательно заряженную группу СОО–.С
участием амино- и карбоксильных групп
происходит полимеризация аминокислот,
т. е. образование полипептидной цепи.
Молекулярная масса мембранных белков
колеблется между 12 000 и 500 000 дальтон. По
силе сцепления с мембраной белки
разделяют на два класса – периферические
и интегральные. Первые слабо связаны с
мембраной и отделяются от нее при самых
различных воздействиях: многократной
промывкой водой или гипертоническими
растворами солей, слабыми детергентами
и ультразвуком. Эти белки не вступают
в тесное взаимодействие с липидами и
отделяются от мембраны в чистом виде.
Более липофильные интегральные белки,
составляющие свыше половины общего
фонда, прочно связаны с липидным бислоем..
В мембранах присутствуют и углеводы,
ковалентно связанные либо с белками
(гликопротеиды), либо с липидами
(гликолипиды). Углеводные компоненты
этих соединений в основном нейтральные
сахара, гексозоамины и сиаловые кислоты.
Чрезвычайно важным структурным
компонентом биологических мембран
является вода, составляющая примерно
30 % от сухого веса мембраны. Вода в
мембранах находится в связанном с
белковыми и липидными молекулами
состоянии. В состав мембран входят и
неорганические вещества, среди которых
большую структурную роль играют ионы
Са2+
и Mg2+.
торой
компонент мембран представлен белками.
Белки – высокомолекулярные соединения,
относящиеся к классу линейных биополимеров.
Они состоят из отдельных элементарных
единиц, в роли которых выступает 20
различных аминокислот. Все аминокислоты
амфолиты, объединяющие в себе положительно
заряженную аминогруппу NH3+
и отрицательно заряженную группу СОО–.С
участием амино- и карбоксильных групп
происходит полимеризация аминокислот,
т. е. образование полипептидной цепи.
Молекулярная масса мембранных белков
колеблется между 12 000 и 500 000 дальтон. По
силе сцепления с мембраной белки
разделяют на два класса – периферические
и интегральные. Первые слабо связаны с
мембраной и отделяются от нее при самых
различных воздействиях: многократной
промывкой водой или гипертоническими
растворами солей, слабыми детергентами
и ультразвуком. Эти белки не вступают
в тесное взаимодействие с липидами и
отделяются от мембраны в чистом виде.
Более липофильные интегральные белки,
составляющие свыше половины общего
фонда, прочно связаны с липидным бислоем..
В мембранах присутствуют и углеводы,
ковалентно связанные либо с белками
(гликопротеиды), либо с липидами
(гликолипиды). Углеводные компоненты
этих соединений в основном нейтральные
сахара, гексозоамины и сиаловые кислоты.
Чрезвычайно важным структурным
компонентом биологических мембран
является вода, составляющая примерно
30 % от сухого веса мембраны. Вода в
мембранах находится в связанном с
белковыми и липидными молекулами
состоянии. В состав мембран входят и
неорганические вещества, среди которых
большую структурную роль играют ионы
Са2+
и Mg2+.
Ведущую роль в удержании белков и липидов в составе биологических мембран играют нековалентные физико-химические связи.
Двойной липидный слой образуюет основу биологической мембраны.
С наружной плазматической мембраной генетически связана внутриклеточная система мембран (ЭС). Гранулярной ЭР осуществляет синтез, накопление и транспорт белков, а также участвует в процессах секреции белков. Огранулярный ЭР осуществляет синтез углеводов, липидов, терпиноидов и других веществ, участвует в процессах детоксикации вредных для клетки соединений гидрофобной природы. Вместе с митохондриями ЭР является важным компонентом окислительно-восстановительных систем клетки. ЭР может служить системой передачи раздражения (ПД) внутри клетки, а также способствует объединению процессов обмена веществ в клетке в единое целое.
ядро окружено двойной мембраной, которую часто называют ядерной оболочкой. Одно из отличий этой мембраны состоит в том, что она пронизана множеством пор, которые связаны с другими структурами и поэтому не представляют просто отверстия в оболочке ядра.
Митохондрии и хлоропласты окружены двойной мембраной, внутренний слой которой имеет весьма сложное строение. Мембраны хлоропластов и наружные мембраны митохондрий обнаруживают на поперечных срезах обычное строение: видна трехслойная структура толщиной около 7,5 нм. Наружная мембрана митохондрий легко проницаема для сахарозы, небольших анионов и катионов, адениннуклеотидов, кофермента А и многих других соединений в противоположность значительно менее проницаемой внутренней митохондриальной мембране. Внутренняя мембрана образует впячивание, в результате чего возникают митохондриальные кристы, в которые «вмонтированы» ферменты, ответственные за перенос электронов и сопутствующее образование АТФ.
В вязком пространстве между внутренними мембранами митохондрий, называемом матриксом, локализованы ферменты цикла лимонной кислоты (цикл Кребса) и другие. Внутренняя мембрана хлоропластов также образует впячивание, в результате чего возникает сложная внутренняя система тилакоидов. Мембраны тилакоидов хлоропластов содержат 52 % липидов и 48 % белка. Толщина этих мембран составляет около 10 нм.
Благодаря избирательной проницаемости мемб. регулируют транспорт веществ между наружной средой и клеткой, между органеллами цитоплазмой и т. д. Регулируя поступление и выведение веществ в клетку и из нее, мембраны тем самым регулируют скорость и направление биохимических реакций, которые составляют основу обмена веществ организма. Сама избирательная проницаемость мембран зависит от обмена веществ в клетке.
Компартментализация клетки – необходимое условие для жизнедеятельности и одна из основных функций мембран. Во-первых, мембраны увеличивают внутреннюю поверхность клетки, на которой локализованы ферменты и проходят химические реакции. Во-вторых, разные компартменты отличаются по химическому составу. Далее, поскольку компартменты имеют различный химический состав в них проходят разные биохимические реакции, то с помощью мембран осуществляется физическое разделение метаболических процессов, часто противоположного направления. В разных компартментах имеются разные концентрации органических веществ, ионов, разный химический состав. Это приводит к химической геторогенности в клетке. Неодинаковая концентрация ионов по обеим сторонам мембраны приводит к возникновению разности электрических потенциалов.
Обладая избирательной проницаемостью, пропуская в клетку необходимые вещества, мембраны выполняют еще одну функцию – регулируют гомеостаз. Гомеостазом называют свойство клетки (органеллы, органа, организма, экосистемы) поддерживать постоянство своей внутренней среды.
Большая часть мембран, кроме общих функций, таких как регулирование обмена веществ, компартментизация, выполняют и специальные. Например, мембраны митохондрий и хлоропластов принимают непосредственное участие в синтезе АТФ.
Таким образом, синтез АТФ необходим постоянно, он связан со строго определенной структурой мембран органелл (хлоропласты, митохондрии). Нарушение этой структуры приводит к снижению синтеза АТФ, а это значит – к смерти.
Лабильная структура мембран позволяет им выполнять разные функции: барьерные, транспортные осмотические, электрические, структурные, энергетические, биосинтетические, секреторные, рецепторно- регуляторные и некоторые другие.
В заключение укажем на основные свойства мембран:
1. Мембраны являются сложными структурами. Они состоят из структурных белков и липидов, но могут также включать высокоспецифические молекулы ферментов, пигментов и кофакторов.
2. Благодаря химической вариабильности составляющих мембраны молекул белков и липидов и в зависимости от их функций, различные мембраны могут иметь разную структуру.
3. Структура мембран обеспечивает высокую степень упорядоченности которой специфические молекулы могут образовывать комплексные функциональные единицы.
4. Ферментные реакции и другие процессы в мембранах могут приводить к пространственно направленным, или векторным, реакциям; мембраны асимметричны.
