
- •§ 1. Предмет радиохимии
- •Особенности радиохимии
- •4. Значение радиохимии
- •§ 2. Краткий очерк истории развития радиохимии
- •Общая радиохимия
- •1. Радиоактивность и .Свойства изотопных частиц.
- •Общехимические свойства изотопных частиц
- •Термодинамическое поведение изотопных частиц
- •3. Кинетическое поведение изотопных частиц
- •§ 1. Классификация реакций изотопного обмена
- •§ 2. Причины протекания реакций изотопного обмена
- •§ 3. Особенности реакций идеального изотопного обмена
- •§ 4. Основное уравнение кинетики реакций идеального изотопного обмена
- •. Основы экспериментальных методов исследования процессов изотопного обмена
- •Глава 4
- •§ 1. Состояние радиоактивных элементов [нуклидов] в жидкой фазе
- •§ 2. Процессы радиоколлоидообразования
- •§ 3. Основы экспериментальных методов исследования радиоколлоидов
- •Химия радиоактивных элементов
- •Глава 10
- •§ 1. Технеций
- •§ 2. Прометий
- •§ 3. Полоний
- •§ 4. Астат
- •§ 5. Радон
- •§ 6. Франций
- •§ 7. Радий
- •Особенности явления ядерной изомерии
- •. Химические последствия изомерных переходов
- •Практическое использование химических последствий изомерного перехода
- •Глава 14
- •§ 1. Теоретические аспекты химических последствий --распада
- •Практическое использование химических последствий --распада
- •§ 2. Экспериментальные методы исследования химических последствий --распада
- •1. Основы ядерной энергетики
- •2. Взаимодействие нейтронов с ядерным веществом, реакция деления ядер.
- •3. Жизненный цикл нейтронов
- •1902 – 1903. Начало пути: а. Беккерель, ф.Содди, э. Резерфорд
- •Виды ядерных зарядов
- •Мощность ядерных боеприпасов
- •Поражающие факторы ядерного взрыва.
- •Основы патогенеза радиационного поражения Взаимодействие ионизирующего излучения с веществом.
- •Классификация и характеристика радиозащитных веществ
- •Радиозащитные вещества кратковременного действия
- •Серосодержащие радиозащитные вещества.
- •Производные индолилалкиламинов
- •Комбинации радиозащитных веществ
- •Химические радиопротекторы и гипоксия
- •Механизм радиозащитного действия
- •1. Радиохимические механизмы
- •2. Биохимико-физиологические механизмы
§ 1. Классификация реакций изотопного обмена
Процессы изотопного обмена классифицируются по степени близости свойств изотопов, по механизму реакций изотопного обмена, по степени сложности процессов и по характеру систем, в которых протекают эти процессы.
По степени близости свойств изотопов различают процессы идеального и неидеального изотопного обмена. В процессах идеального изотопного обмена участвуют изотопные атомы, тождественные по своим физико-химическим свойствам. Процессы неидеального изотопного обмена характерны для заметно отличающихся по физико-химическим свойствам изотопов самых легких элементов. Для радиохимических исследований наибольшее значение имеют процессы идеального изотопного обмена.
По механизму реакций, лежащих в основе процессов изотопного обмена, последние классифицируются следующим образом*.
1. Процессы изотопного обмена, связанные с нарушением одних и образованием других химических связей, сопровождающиеся пространственным перемещением изотопных атомов от одной частицы к другой. Эти процессы осуществляются по механизмам, характерным для обычных химических реакций, протекающих через стадию образования активированного комплекса. При этом возможны следующие три случая: 1) наиболее общий случай—превращение активированного комплекса в конечные продукты—взаимообменный механизм — обмен частицами внутренней и внешней координационных сфер. При этом происходит согласованное перемещение обменивающихся изотопных атомов внутри активированного комплекса по схеме
[MXn] + X* {[MXn] ... X*} [MXn-1X*] + X
где {[MXn] ... X*} - внешнесферный комплекс, например:
[Co(NH3)5Cl]2+ + 35Cl- {[Co(NH3)5Cl]2+ ... 35Cl-} [Co(NH3)5 35Cl]2+ + Cl-
2) превращение активированного комплекса в относительно устойчивый промежуточный продукт с координационным числом,
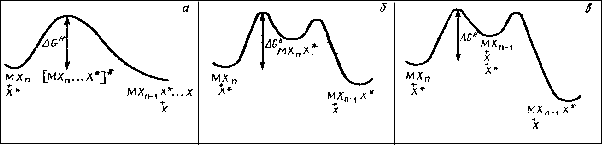 Рис.
2. Энергетические профили реакций
изотопного обмена:
а
— взаимообменный механизм; б —
ассоциативный механизм; в — диссоциативный
механизм
Рис.
2. Энергетические профили реакций
изотопного обмена:
а
— взаимообменный механизм; б —
ассоциативный механизм; в — диссоциативный
механизм
большим, чем у исходного соединения,— ассоциативный механизм, который можно представить в общем виде схемой
MXn + X* [MXn ... X*] MXnX* MXn-1X* + X
например:
K 131I + I2 [K 131I ... I2] KI2 131I I 131I + KI
3) распад активированного комплекса также с образованием относительно устойчивого промежуточного продукта, но с меньшим координационным числом—диссоциативный механизм:
MXn + X* [MXn ... X*] MXn-1 + X + X* MXn-1X* + X
например:
[IrCl6]3- + 36Cl- [IrCl3-6 ... 36Cl-]4- [IrCl5]2- + Cl- + 36Cl- [IrCl5 36Cl]3- + Cl-
Предельным случаем обмена по этому механизму является обмен в растворах сильных электролитов. Энергетические профили реакций изотопного обмена, протекающих по рассмотренным механизмам, представлены на рис. 2.
2. Процессы изотопного обмена, не сопровождающиеся нарушением химических связей и перемещением изотопных атомов. К их числу относятся процессы, связанные с электронными переходами между изотопными атомами химических форм, участвующих в обмене:
Mn+
![]() M*
(n+1)+
M(n+1)+
+ M* n+
M*
(n+1)+
M(n+1)+
+ M* n+
например:
239Pu3+ + 238Pu4+ 238Pu3+ + 239Pu4+ 99mTcO-4 + 99TcO2-4 99TcO-4 + 99mTcO2-4
Эти процессы отличаются от обычных окислительно-восстановительных реакций тем, что они протекают между формами, отвечающими различным степеням окисления, при наличии окислительно-восстановительного равновесия в системе.
Кроме того, процессы изотопного обмена подразделяются на простые и сложные. К простым относятся реакции между двумя частицами, содержащими по одному участвующему в обмене атому, занимающему строго определенное положение в молекуле. Например:
C6H5 81Br + Li 82Br C6H5 82Br + Li 81Br o-CH3C6H4Br + Li 82Br o-CH3C6H4 82Br + Li 81Br
К сложным относятся процессы изотопного обмена, в которых участвуют более двух частиц, содержащих изотопы данного элемента, например:
C6H5 127I + 2Li 131I C6H5 131I + C6H5 131I + 2Li 127I C2H5 127I
или реакции между двумя химическими формами, из которых хотя бы одна содержит атомы, неэквивалентные в химическом отношении. Примером может служить реакция изотопного обмена брома между дибромалкилбензолом и бромидом лития:
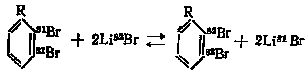
По характеру систем процессы изотопного обмена подразделяются на гомогенные, протекающие в одной фазе, и гетерогенные, в которых изотопный обмен протекает между веществами, находящимися в разных фазах.
Наибольший интерес с точки зрения радиохимических исследований представляют простые реакции идеального гомогенного изотопного обмена. Эти реакции поддаются количественному описанию и будут более подробно рассмотрены ниже.
* Эта классификация не включает чисто физические механизмы обмена (процессы, связанные с испарением, диффузией, перекристаллизацией и т. д.).
