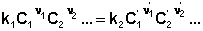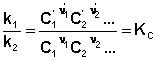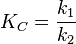- •Аналитикалық химия пәні, оның ғылыми зерттеулердегі және өндірістік практикадағы орны. Аналитикалық химия әдістерінің жіктелу түрлері.
- •Аналитикалық реакциялардың мінездемелері. Олардың орындалу жолдары.
- •Аналитикалық катиондарды бөлшектеп және жүйелеп талдау.
- •Катиондардың қышқылдық-негіздік жіктелуі. Топтық реагенттің әсері. Түзілген тұнбалардың ерігіштігі.
- •Күшті және әлсіз электролиттер. Гомогенді жүйедегі химиялық тепе-теңдіктер
- •Гомогенді тепе-теңдік тұрақтылары – термодинамикалық, концентрациялық, шартты.
- •Күшті қышқыл және күшті негіз ерітінділерінің рН есептеу
- •Әлсіз қышқыл және әлсіз негіз ерітінділерінің рН есептеу
- •Тотығу-тотықсыздану реакциялары.Тотығу-тотықсыздану потенциалы. Нернст теңдеуі. Тотығу-тотықсыздану реакцияларының тепе-теңдік константалары.
- •1) Тотықтырғыш пен тотықсыздандырғыш анықтап алу керек. Ол үшін типті тотықтырғыш пен тотықсыздандырғыштың тізімін пайдалану керек.
- •4) Ттр теңдеуіндегі коэффициенттер электрондық және электронды-иондық баланс арқылы анықталады.
- •Тотығу-тотықсыздану реакцияларының аналитикалық химиядағы сапалық талдауда пайдаланылуы. Күшті тотықтырғыштар мен тотықсыздандырғыштар.
- •Аналитикалық химиядағы комплекс түзу реакцияларының сапалық талдауда қолданылуы.
- •Аниондардың әртүрлі қасиеттеріне қарай жіктеліну түрлері. І-ііі топ аниондары
- •Ерігіштік және оның есептелуі. Тұнбаның еруіне әсер ететін факторлар.
- •Сандық талдау, оның түрлері, қолданылу салалары. Гравиметриялық талдау, әдістің артықшылығы және кемшілігі.
- •Титриметриялық талдау, оның түрлері. Титриметриялық талдауда қолданылатын реакцияларға қойылатын талаптар. Аналитикалық талдауда жиі қолданылатын ерітінді концентрацияларының есептеу жолдары
- •Титрлеу қисығын тұрғызу және оны талдау. Күшті қышқылды күшті негізбен титрлеуде ерітіндінің рН-ның өзгеруі (және керісінше).
- •Титрлеудің соңғы нүктесін анықтау әдістері. Қышқыл-негіздік индикаторлар. Индикаторлардың түсінің ауысу интервалы. Индикатор қателігі.
- •Комплексонометриялық титрлеу. Металл комплексонаттардың тұрақтылығына рН әсері. Тура және кері титрлеу. Металлохромды индикаторлар
- •Физика-химиялық талдау әдістері, электрохимиялық талдау әдістерінің жіктелуі. Потенциометрия.
- •Потенциометрлік титрлеу, эквивалентті нүктені анықтау жолдары.
Аналитикалық химия пәні, оның ғылыми зерттеулердегі және өндірістік практикадағы орны. Аналитикалық химия әдістерінің жіктелу түрлері.
Аналитикалық реакциялардың мінездемелері. Олардың орындалу жолдары.
Аналитикалық реакциялардың сезімталдығы, талғағыштығы, анықтау шегі, сұйылту шегі. -Ажар
Аналитикалық катиондарды бөлшектеп және жүйелеп талдау.
Катиондардың қышқылдық-негіздік жіктелуі. Топтық реагенттің әсері. Түзілген тұнбалардың ерігіштігі.
Гомогенді жүйелер және массалар әрекеттесуші заңы. Активті коцентрация, активтік коэффициенттер есептелуі. Ерітіндінің иондық күші. -Айдана
Күшті және әлсіз электролиттер. Гомогенді жүйедегі химиялық тепе-теңдіктер.
Гомогенді тепе-теңдік тұрақтылары – термодинамикалық, концентрациялық, шартты.
Ерітінділердегі қышқыл-негіздік тепе-теңдік, Бренстед-Лоури теориясы. Судың иондық көбейтіндісі және сутектік көрсеткіші. -Жазира
Күшті қышқыл және күшті негіз ерітінділерінің рН есептеу.
Әлсіз қышқыл және әлсіз негіз ерітінділерінің рН есептеу
Буферлі ерітінділерінің рН-ын анықтау жолдары, мысал келтіріңіз. –Б.Арай
Тотығу-тотықсыздану реакциялары.Тотығу-тотықсыздану потенциалы. Нернст теңдеуі. Тотығу-тотықсыздану реакцияларының тепе-теңдік константалары.
Тотығу-тотықсыздану реакцияларының аналитикалық химиядағы сапалық талдауда пайдаланылуы. Күшті тотықтырғыштар мен тотықсыздандырғыштар.
Комплексті қосылыстардың ерітіндідегі химиялық тепе-теңдігі, комплекс түзушінің координациялық саны, лигандтардың дентаттылығы, тұрақтылық, тұрақсыздық константалары. -Айгерим
Аналитикалық химиядағы комплекс түзу реакцияларының сапалық талдауда қолданылуы.
Аниондардың әртүрлі қасиеттеріне қарай жіктеліну түрлері. І-ІІІ топ аниондары.
Гетерогенді тепе-теңдік. Аналитикалық химияда нашар еритін қосылыстар тұнбалары. Ерігіштік көбейтіндісі және иондық көбейткіш. –Ж.Арай
Ерігіштік және оның есептелуі. Тұнбаның еруіне әсер ететін факторлар.
Сандық талдау, оның түрлері, қолданылу салалары. Гравиметриялық талдау, әдістің артықшылығы және кемшілігі.
Тұнбаға қойылатын талаптар. Тұнбаның тұндырылған күйі мен гравиметриялық түрлері. Мысал келтіріңіз. Тұнбаға әсер ететін факторлар Мөлдір
Титриметриялық талдау, оның түрлері. Титриметриялық талдауда қолданылатын реакцияларға қойылатын талаптар. Аналитикалық талдауда жиі қолданылатын ерітінді концентрацияларының есептеу жолдары.
Титрлеу қисығын тұрғызу және оны талдау. Күшті қышқылды күшті негізбен титрлеуде ерітіндінің рН-ның өзгеруі (және керісінше).
Әлсіз негізді күшті қышқылмен титрлеуде ерітіндінің рН-ның өзгеруі арқылы тёитрлеу кисығын тұрғызу (және керісінше). –Асыл
Титрлеудің соңғы нүктесін анықтау әдістері. Қышқыл-негіздік индикаторлар. Индикаторлардың түсінің ауысу интервалы. Индикатор қателігі.
Комплексонометриялық титрлеу. Металл комплексонаттардың тұрақтылығына рН әсері. Тура және кері титрлеу. Металлохромды индикаторлар.
Тотығу-тотықсыздану және тұндырып титрлеудің ерекшеліктері, орындалатын талаптар. –Адема
Физика-химиялық талдау әдістері, электрохимиялық талдау әдістерінің жіктелуі. Потенциометрия.
Потенциометрлік титрлеу, эквивалентті нүктені анықтау жолдары.
Оптикалық талдау әдістері. Бугер-Ламберт-Бер заңы. Фотоколориметрия мен спектрофотометрия әдістерінің ерекшелігі, қолданылу саласы. –Айжан
Аналитикалық химия пәні, оның ғылыми зерттеулердегі және өндірістік практикадағы орны. Аналитикалық химия әдістерінің жіктелу түрлері.
Аналитикалық химия пәні зерттеу пәні ол қосылыстар мен заттардың құрамы,құрылысы,қасиеттері туралы мәлімет береді.
Ан. Химия зерттеу пәні болғандықтан химиялық талдауды кеңінен қолданады.
Талдау химияның бір бөлішігі белгісіз қосылыстар мен заттардың қасиеттеріне сүйене отырып,оның құрылысы мен құрамына айқындайтын бөлу,ашу және анықтау әдісі
Ан. химия сандық және сапалық талдау болып бөлінеді.
Сапалық талдау зерттелетін қосылыс пен заттың неден тұратынын анықтау әдісі.
Сандық талдау белгісіз қосылыстармен заттар құрамындағы катион мен анионның сандық мөлшерін көрсетеді.
Талдау зерттелетін заттардың түріне,мөлшеріне,құрамына,мақсатына қарай бірнеше түрге бөлінеді.Түріне қарай :органикалық, бейорганикалық..Мөлшеріне қарай:макро,микро,субмикро, ультрамикро талдау.Мақсатына қарай: элементтік, фазалық,молекулалық, функционалдық
Аналитикалық химия мақсаты
1)зерттелетін қосылыстардың аналитикалық қасиетіне сүйене отырып реакция теңдеулерін жазу,процесті анықтау
2)сылыстың не заттың құрамына байл.аналитикалық сигнал не белгі көру
3)сылыстар мен заттарды бөліп алу және ашу жолдарының жаңа тәсілдері мен жолдарын анықтау
4)зерттелген қосылыс аналитикалық қасиетіне сүйене отырып таңдау, талдау және дамыту
Аналитикалық сигнал х-қ реакция нәтижесінде көзге көрінетін құбылыс,яғни тұнба түзілуі, газ бөлінуі не түс өзгеруі.
Ан. Сигнал байқалғанда қосылыстың формуласы өзгереді.
ВаСl 2 + H2SO4= BaSO4(тұнба) +2HCl
Аналитикалық реакциялардың мінездемелері. Олардың орындалу жолдары.
Химиялық реакция барысында көзге көрінетін құбылыс нақты әрі белгілі бір қасиетке тән аяғына дейін жүретін реакциялар аналитикалық деп аталады.
Ан.реакциялардың константа мәні үлкен үлкен болу керек және жылдам жұру керек.Ол реакциялар зерттелетін қосылыстың сапалық және сандық қасиетін көрсетеді. Химиялық талдауды жүзеге асыру үшін зерттелінетін химиялық қосылыс немесе оны құрайтын бөлшектердің ерекше көзге түсетін химиялық немесе физикалық қасиеттерін байқауға әкелетін реакциялар аналитикалық реакциялар деп аталады. Олар аналитикалық әсер көрсетеді. Химиялық өзгерістерге себеп болатын химиялық реактивтер реагенттер деп аталады. Реагенттердің әсерінен байқалатын әсер – аналитикалық белгі не сигнал.
Бір затқа ғана тән ерекше реакцияны жеке реакция деп атайды. Жеке реакцияны талғағыш (селективті) және ерекше (спецификалық) деп бөледі. Егер санаулы иондармен (2-5) химиялық реакция нәтижесінде ұқсас аналитикалық сигнал байқалса – талғағыш реакция.
Аналитикалық реакцияяға қойылатын негізгі талаптар: талғағыштығы, ерекшелігі, тазалығы, сезгіштігі. Тазалығына байланысты химиялық реагенттер : техникалық таза (бөгде қоспа үлесі 2 %-дан жоғары), таза (2% шамасында), аналитикалық таза (1%), химиялық таза (1 %-дан кіші), жоғары эталондық таза (0,01% - 0,0001%), аса таза (0,0001%-дан аз) болып жіктеледі. Аналитикалық реагент , реакцияның сезгіштігі анықталатын заттың ең аз мөлшерімен сипатталады, оны анықтау шегі дейміз. Белгілі анықталатын реакциямен анықталатын мөлшер неғұрлым аз болса, реакция сезгіштігі артады. Реакция сезгіштігі өзара бір-бірімен байланысты 4 шамамен сипатталады. Олар: 1) Шекті сұйылту -анықталатын заттың 1 грамы бар ерітіндінің аналитикалық сигнал бере алатын шегіне жете сұйылтылған көлемі (мл/г), 2) Шекті концентрация –белгілі реакциямен анықталатын заттың ең төмен концентрациясы (г /мл) ; 3) Шекті көлем – шегіне жете сұйылтылған ерітіндінің анықтауға мүмкіндік беретін ең кіші көлемі (мл); 4) анықталатын минимум – белгілі реагент көмегімен шегіне жете сұйылтылған ерітіндінің ең кіші көлемінде анықталатын заттың ең аз мөлшері (мкг). Бұл шамалардың бір-бірімен байланысы :

Неғұрлым анықталатын минимум төмен, ал шекті сұйылту жоғары болған сайын анилитикалық реакция сезгіштігі арта түседі.
Аналитикалық реакциялардың сезімталдығы, талғағыштығы, анықтау шегі, сұйылту шегі
Химиялық реакция барысында көзге көрінетін құбылыс нақты әрі белгілі бір қасиетке тән аяғына дейін жүретін реакциялар аналитикалық деп аталады.
Ан.реакциялардың константа мәні үлкен үлкен болу керек және жылдам жұру керек.Ол реакциялар зерттелетін қосылыстың сапалық және сандық қасиетін көрсетеді.
Зерттелетін қосылысқа қосылатын реакив сезімтал реагент болып табылады және оның 3 түрі бар:топтық,жалпы,жеке
Ан.химия негізгі заңдылығы зерттелетін қосылыстың концентрациясы неғұрлым аз болса,оның анықталуы соғұрлым жоғары.Осыған орай реакция сезгіштігі мына шамалар тәуелді.
1)Анықталу шегі ол зерттелетін қосылыстың ең минималды концентрациясы 10-6 тең.
2)Шекті сұйытылған ерітінді анықтауға кеткен ерітіндінің минимал көлемі ,ол 1 мл не 10 тамшы
3) концентрация шегі зерттелген қосылыстың реакцияға түсуге қабілетті ең аз көлем,ол 0,1 мл не 2 тамшы
4) сұйылту шегі құрамында зерттелетін заттың ең минималды массасы,ол минималды көлем мен минимал концентрацияға пропорцинал және де сезгіштікті анықтау үшін қолданылатын реактивтің тазалығы орындау керек.Ол химиялық таза, талдауға мүмкіндік бар қосылыстар.
Гомогенді жүйе кеңістікте ойша бөліп алынған біртекті фаза.гомогенді жүйеде өткен химиялық реакция белгілі бір заңдылыққа сүйене отырып тура және кері бағытта болады.Соның бірі масса әрекеттесуші заңдылық, ол белгілі бағытта жүрген реакция жылд. құрамындағы қосылыстардың концентрациясына көбейтіндісіне тура пропорционал.
![]()
![]()