
- •Список сокращений
- •Введение
- •Глава 1. Литературный обзор реакции нуклеофильного присоединения природных циклических a,b-еноновых монотерпеноидов
- •Использование продуктов 1,2-присоединения металлоорганических реагентов к α,β-еноновым монотерпеноидам
- •Глава 2. Обсуждение результатов
- •Оптически чистый синтон для полового феромона сосновых пилильщиков рода Diprion и Neodiprion
- •Глава 3. Экспериментальная часть
- •Методы подготовки реагентов и растворителей
- •Методика проведения реакций 1,2-присоединения металлорганических реагентов к (r)-4-ментенону
- •(2S)-метилдец-1-илбромидов
- •Литература
Оптически чистый синтон для полового феромона сосновых пилильщиков рода Diprion и Neodiprion
Оптически активный (S,S,S)-2-ацетокси-3,7-диметилпентадеканол (5) является наиболее предпочтительным аттрактантом для многих видов сосновых пилильщиков рода Diprion и Neodiprion, представляющих большую опасность для хвойных лесов. Существующие схемы синтеза оптически чистого (S,S,S)-(5) основываются на конвергентном подходе. Для получения синтона, содержащего С-7 метилразветвленный фрагмент, в большинстве работ использовали производные (R)-цитронеллола, получаемого из (R)-пулегона, а для введения остальных двух асимметрических центров: L-(+)-винную кислоту [51-53] и (3S)-гидрокси-(2R)-метилбутират, полученный асимметрическим восстановлением ацетоуксусного эфира [54]. Однако, данные способы получения целевого феромона не получили широкого внедрения ввиду сложности синтеза и высокой себестоимости.
Ретросинтетический анализ и литературные данные показывают, что достаточно оптимальным может являться конвергентный подход на основе двух хиральных синтонов (6) и (7), предложенный Tai I. и др. [54]. Однако, если ими в качестве исходного субстрата для получения оптически чистого строительного блока (7) использовался (R)-пулегон, то мы предлагаем синтез из оптически чистого (R)-4-ментен-3-она (1).
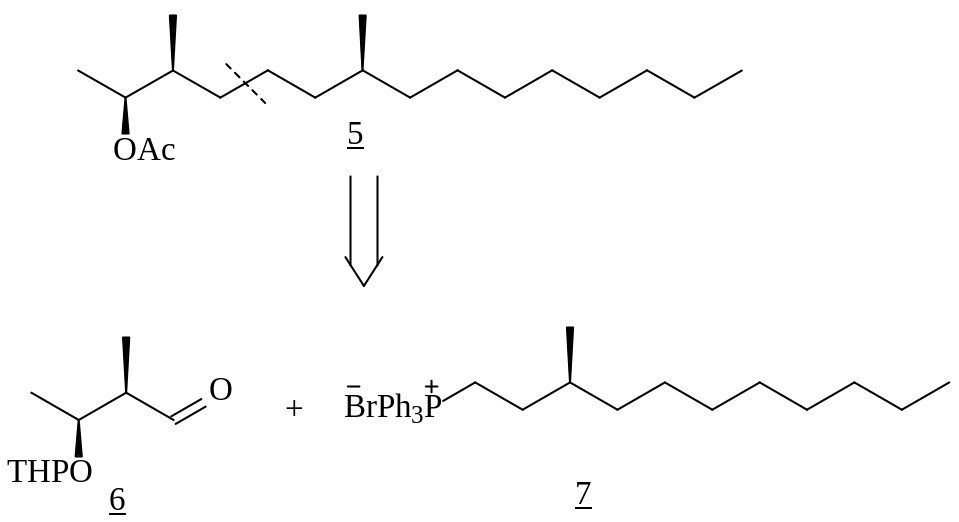
Региоселективное 1,2-присоединение n-C6H13Li к енону (1) при -78o и дальнейшая обработка промежуточного енола хлорхроматом пиридиния дали (5S)-метил-2-изопропил-3-гексил-2-циклогексен-1-он (8). Последующие озонолиз енона (8), протекающий с отщеплением изобутильного фрагмента, и метанолиз привели к кетоэфиру (9). Необходимо отметить: если обычно для озонолитических превращений сопряжённых енонов используют многократный избыток озона, то для полной конверсии циклоенона (8) было достаточно эквимолярного его количества. Дезоксигенирование кетоэфира (9) по Хуанг-Минлону, сопровождающееся омылением сложноэфирной группы, дало (3S)-метилундекановую кислоту (10). Восстановлением кислоты литийалюмогидридом получен спирт (11) , который через бромирование в пиридине был переведён в бромид (12). Реакцией Хунс-Диккера кислоты (10) бромиронием в нитрате серебра и гидроксиде натрия был синтезирован бромид (13).
Полученные хиральные синтоны могут быть использованы в синтезе целевого феромона (S,S,S)-2-ацетокси-3,7-диметилпентадеканола.
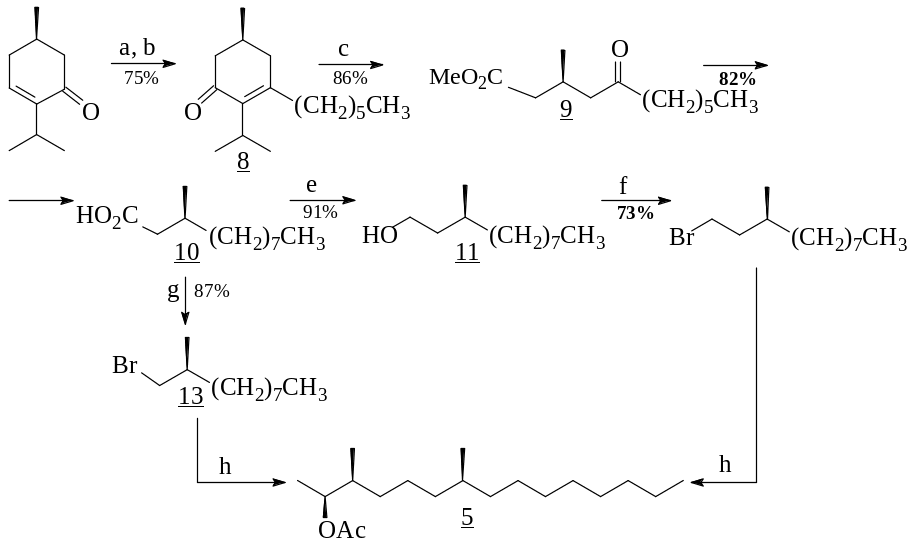
n-C6H13Li, hexane, -78oC; b. PCC, CH2Cl2; c. O3, MeOH-CH2Cl2, 0oC; d. N2H4H2O; then KOH, ∆; e. LiAlH4; f. PBr3/Py; g. NaOH, AgNO3, Br2; h. [59].
Таким образом, нами исходя из (R)-4-ментен-3-она предложен новый путь к синтезу оптически чистых синтонов для полового феромона сосновых пилильщиков рода Diprion и Neodiprion.
Глава 3. Экспериментальная часть
ИК-спектры записывали на приборе IR Prestige-21 (Shimadzu) в тонком слое. Спектры ЯМР регистрировали на спектрометре BRUKER AM-300 (рабочая частота 300.13 МГц для 1Н и 75.47 для 13С) в CDCl3. За внутренний стандарт принимали значение сигналов хлороформа: в ПМР – примесь протонов в дейтерированном растворителе (δ 7.27 м.д.), в ЯМР 13С – средний сигнал CDCl3 (δ 77.00 м.д.). Хроматографический анализ проводили на приборах Chrom-5 (длина колонки – 1.2 м; неподвижная фаза – силикон SE-30 (5%)+ OV-225 (3%) на Chromaton N-AW-DMCS (0.16-0.20 мм); рабочая температура 50-200о) и GC-9A «Shimadzu» [кварцевая капиллярная колонка длиной 25 м, неподвижная фаза DB-1 (0.25 микрон), рабочая температура 80-280о]; газ-носитель – гелий. Оптическое вращение измеряли на поляриметре «Perkin – Elmer 241-MC». Колоночную хроматографию проводили на силикагеле L (60-200 мкм) марки «Lancaster» (England). Для ТСХ использовали пластинки Sorbfil (Краснодар). Масс-спектры исследуемых соединений получены на приборе Shimadzu JCMS 2010 ЕV в условиях ХИАД при энергии электронов 20 эВ с регистрацией положительных и отрицательных электронов. Скорость газа-небулайзера (азот) – 0.05 л/мин, жидкая подвижная фаза − метанол-вода (50:50) при скорости потока носителя 0.03 мл/мин.
