
- •Содержание
- •1Аналитический обзор литературы
- •Использование уникальных свойств кадмия и его соединений в современной науке и технике
- •1.1.2 Распределение кадмия между промпродуктами гидрометаллургического способа получения цинка
- •1.1.3 Поведение кадмия при переработке меднокадмиевых кеков
- •1.2 Состояние кадмия в щелочных растворах
- •1.3 Экстракционное выделение кадмия
- •1.3.1 Экстракция кадмия анионообменными экстрагентами
- •1.3.2 Экстракция кадмия катионообменными экстрагентами
- •1.3.3 Экстракция кадмия из щелочных растворов
- •2 Экспериментальная часть
- •2.1 Исходные вещества, методики эксперимента, исследований и анализа
- •2.1.2 Методики анализа
- •2.2 Исследование экстракция кадмия нбэа-2 из сульфатных растворов
- •2.2.1 Изучение влияния времени контактирования фаз на экстракцию кадмия
- •2.2.2 Влияние рН водной фазы на экстракцию кадмия
1.3.3 Экстракция кадмия из щелочных растворов
Литературные данные по экстракции кадмия из щелочных растворов представлены скупо. Щелочные растворы опробованы для переработки некоторых видов промышленных отходов, содержащих цинк и сопутствующих ему кадмий.
В работе [4] рассмотрена экстракция кадмия из щелочных растворов экстрагентами ДСАФ и БАФФО. Экстракцию проводили из раствора содержащего Cd и ~ 50 г/л сульфата натрия. Регулирование рН вели путем добавления в исходный раствор гидроксида натрия. Начиная с рН ~ 8,5 в исходном растворе выдал осадок гидроксида экстрагируемого металла, поэтому имела место экстракция из пульп. Так как кинетика взаимодействия твердой фазы с экстрагентом отличается от кинетики жидкостной экстракции, то было установлено, что время контактирования фаз составляет 30 минут.
На рис. 7 и 8 представлены зависимости влияния рН на экстракцию кадмия. Они показывают, что экстракция кадмия коррелируется с рН осаждения гидроксида металла. Так рН полного осаждения гидроксида кадмия -9,7, при тех же значениях рН наблюдается резкий рост экстракции кадмия.
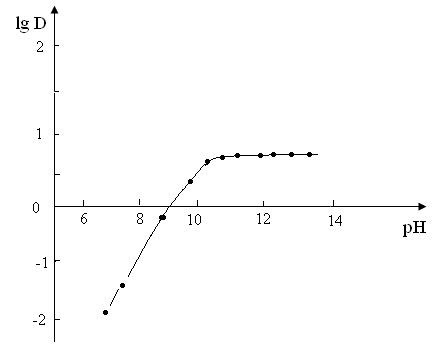
Рис.7 Экстракция кадмия 0,25 моль/л ДСАФ в толуоле из щелочных растворов.
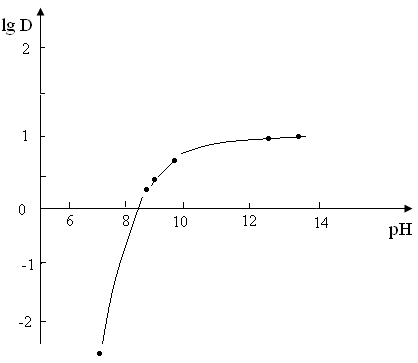
Рис.8 Экстракция кадмия 0,25 моль/л БАФФО в толуоле из щелочных растворов.
Кроме фенольных реагентов для экстракция кадмия из щелочных сред были использованы и другие реагенты [3]:
Дибензоилметан, его 0,1 М раствор в бензоле экстрагирует кадмий практически полностью из щелочных сред (рис. 9), при этом Сu, Hg и Zn остаются в растворе [70, стр. 104].
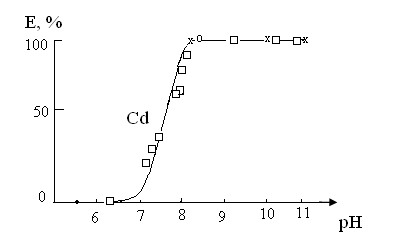
Рис.9 Влияние рН водной фазы на экстракцию кадмия 0,1 М раствором дибензоилметана в бензоле.
Ди-н-бутилфосфорная кислота в тетрахлориде углерода экстрагирует кадмий на 99% [389]. Ди-н-октилсульфид, ди-н- октилсульфоксид и ди-н-октилсульфон почти не экстрагируют кадмий из азотно- и солянокислых растворов (коэффициент распределения 10-2 — 10-3) [299].
Ди-(β-нафтил)тиокарбазон в хлороформе и тетрахлориде углерода экстрагирует кадмий из сильнощелочной среды в присутствии тартрата. Метод используют для отделения кадмия от Bi, Рb и Zn, которые в указанных условиях не экстрагируются [530].
Дитизон. Наибольшее применение нашла экстракция кадмия в виде его дитизоната [88, 136, 195, 254, 281, 686, 725]. Разделение основано на различии кислотности водной фазы, из которой экстрагируются дитизонаты тяжелых металлов, и их неодинаковая устойчивость по отношению к маскирующим комплексообразователям, кислотам и щелочам [150, 281, 686].
Из 1—2 моль/л растворов NaOH комплекс кадмия с дитизоном хорошо извлекается хлороформом. 0,2 моль/л кислоты легко разлагают его дитизонат и переводят кадмий в водную фазу. Hg, Au и Сu экстрагируются вместе с кадмием из щелочной среды. При обработке органического слоя 0,2 моль/л кислым раствором эти элементы остаются в экстракте. Таким путем можно отделить кадмий от 100-кратных количеств указанных металлов. От 1000-кратных количеств ионов Bi+3, Pb2+ и Т1+ кадмий отделяют экстракцией раствором дитизона в ССl4 при рН >14. Препятствуют экстракции кадмия ионы S2-, CN- в сильнощелочной среде, цитраты и тартраты — в нейтральной.
Лучшим экстрагентом для кадмия служит этилпропионат, который при рН > 7,5 за одну экстракцию практически полностью экстрагирует его дитизонат [718].
0,01—0,03 M раствор диэтилдитиокарбамината натрия в ССl4 используют как экстрагент кадмия. Растворимость его комплекса с кадмием в хлороформе (2 г/100 мл) значительно выше, чем в ССl4 (8 мг/100 мл). При рН 5 в органический слой совместно с кадмием переходят Со, Mn, Ni, Pb и V [142], но при обработке экстракта l М HCl кадмий реэкстрагируется. Константа экстракции диэтилдитиокарбамината кадмия равна 5,81 [143,389]. Описана экстракция кадмия раствором реагента в ССl4 при рН 3,7 [447]. В щелочной среде, содержащей тартрат, с этим экстрагентом можно разделить кадмий и медь [203].
Смесью (1:2) н-амилметилкетона и н-бутилфосфата экстрагируется роданидный комплекс кадмия из слабощелочных растворов, содержащих 15 % NH4SCN [619].
β-Изопиразолон экстрагирует кадмий из щелочных растворов на 99 % [389].
