
- •Содержание
- •1Аналитический обзор литературы
- •Использование уникальных свойств кадмия и его соединений в современной науке и технике
- •1.1.2 Распределение кадмия между промпродуктами гидрометаллургического способа получения цинка
- •1.1.3 Поведение кадмия при переработке меднокадмиевых кеков
- •1.2 Состояние кадмия в щелочных растворах
- •1.3 Экстракционное выделение кадмия
- •1.3.1 Экстракция кадмия анионообменными экстрагентами
- •1.3.2 Экстракция кадмия катионообменными экстрагентами
- •1.3.3 Экстракция кадмия из щелочных растворов
- •2 Экспериментальная часть
- •2.1 Исходные вещества, методики эксперимента, исследований и анализа
- •2.1.2 Методики анализа
- •2.2 Исследование экстракция кадмия нбэа-2 из сульфатных растворов
- •2.2.1 Изучение влияния времени контактирования фаз на экстракцию кадмия
- •2.2.2 Влияние рН водной фазы на экстракцию кадмия
1Аналитический обзор литературы
Использование уникальных свойств кадмия и его соединений в современной науке и технике
Кадмий применяют главным образом для электролитического железа с целью предохранения его от коррозии, а также для производства сплавов и красок. Кадмий в качестве защитного покрытия обладает существенными преимуществами перед цинком и никелем. Детали, покрытые кадмием, обладает хорошей ковкостью, вследствие чего их можно формовать и штамповать. Покрытые кадмием детали легче свариваются, чем оцинкованные. При повреждении поверхности изделия кадмиевые покрытия не отслаиваются, как это наблюдается с покрытиями из цинка или никеля.
По химической стойкости кадмиевые покрытия более стойки, чемцинковые в щелочных и солевых средах. Вследствие этого кадмиевые покрытия обладают большей защитной способностью, чем цинковые, при одинаковой и даже меньшей толщине слоя. Широкому внедрению кадмирования способствовало также и то , что кадмиевые покрытия получаются более красивыми по сравнению с цинковыми. Также покрытия,как правило, применяют как предохранительные покрытия для деталей, которые постоянно подвергаются сильной коррозии, но не воспринимают значительных механических усилий[2]
Основные области применения кадмиевых покрытий:
Защита от коррозии металлических изделий, соприкасающихся с морской водой и подобными ей растворами, цинковые покрытия в этом случае совсем непригодны;
Защита от коррозии деталей машин, работающих в закрытых помещениях с умеренной или сильной влажностью;
Защита от коррозии электрических контактов.
Большое количество кадмия используют в производстве сплавов:
антифрикционных, легкоплавких, сплавов с драгоценными металлами и др.Антифрикционные сплавы содержат до 80% Cd.При введении кадмия в подшипниковые сплавы достигается низкий коэффициент трения при длительной эксплуатации. Сплавы, содержащие 98,3- 98,5% Cd и различные количества никеля, серебра или меди, применяют обычно в двигателях внутреннего сгорания, работающих при высоких скоростях и темперетурах.
Наиболее распространены легкоплавких, сплавы кадмия со свинцом , оловом и висмутом, имеющие температуру плавление ниже точки кипения воды. Эти сплавы используют для изготовление электрических предохранителей, пожарных сигнализаторов, пробок к автоматическим огнетушителям и к паровым котлом.
Из сплавов меди с кадмием изготовляют телефонные и трамвайные провода. Добавление около 1% Cd увеличивает прочность медной проволоки почти вдвое при небольшом снижении электропроводности. Сплав медь- цирконий кадмий употребляется в линиях высоковольтных передач и отличается еще более высокой прочностью и твердостью, чем меднокадмиевые сплавы[3].
Кадмий употребляют в ювелирном деле в виде двойного сплава с золотом (зеленого цвета), тройного сплава с золотом и серебром и т.д. Кадмий придает различные оттенки изделиям из драгоценных металлов.
Металлический кадмий используют при сооружении атомных реакторов. Обладая большим сечением захвата тепловых нейтронов, кадмий является хорошим поглотителем нейтронов, что позволяет применять его для контрольных стержней, регулирующих скорость атомной реакции.
Кадмий применяют в радиотехнике, особенно в качестве фотоэлементов. Соединения кадмия – теллуриды, селениды, сульфиды, являются эффективными полупроводниковыми материалами, применяемыми в фотоэлектрических приборах. Например, сульфид кадмия является широкозонным полупроводником с шириной запрещенной зоны 2,42 эВ. Это свойство CdS, полезное в оптоэлектронике, используется как в фоточувствительных, так и в фотогальванических устройствах. Его используют для изготовления фоторезисторов (приборов, электрическое сопротивление которых меняется в зависимости от освещенности). Теллурид кадмия (CdTe) и теллурид цинка-кадмия (CdZnTe) используются для изготовление электрооптических модуляторов, приемников радиационного и ИК- излучения и других оптических элементов ИК- оптических систем. CdTe - используется в солнечных батареях и в детекторах радиации. Промышленные солнечные элементы (СЭ) на основе тонких пленок CdTe, со структурой, изображенной на рис.1, в настоящее время обладают КПД до 10%, а в ближайшие годы ожидается увеличение до 15%.
На изготовление СЭ площадью 1м2 требуется около 10г теллура и 9г кадмия. Сегодня при к.п.д. около 10% для генерации 1ГВт требуется 100т Te
Селенид кадмия, сульфид и сульфоселенид кадмия используются для изготовления преобразователей длин волн лазерного излучения, квантоскопов красного, оранжевого, желтого и зеленого цветов излучения.
Созданный английской компанией Миллард фотоэлемент из сульфидного кадмия обладает исключительно высокой чувствительностью, примерно в 20 тыс.раз большей, чем обычный фотоэмиссионный элемент.
Новая перспективная область применения кадмиевых соединений – химическая промышленность :поливиниловые пластики, выпускаемые в США, стабилизируются системами , в основе которых лежат бариевокадмиевые
Наиболее распространены легкоплавких, сплавы кадмия со свинцом , оловом и висмутом, имеющие температуру плавление ниже точки кипения воды. Эти сплавы используют для изготовление электрических предохранителей, пожарных сигнализаторов, пробок к автоматическим огнетушителям и к паровым котлом.
Из сплавов меди с кадмием изготовляют телефонные и трамвайные провода. Добавление около 1% Cd увеличивает прочность медной проволоки почти вдвое при небольшом снижении электропроводности. Сплав медь- цирконий кадмий употребляется в линиях высоковольтных передач и отличается еще более высокой прочностью и твердостью, чем меднокадмиевые сплавы[3]
Металлический кадмий используют для изготовления электродов к нормальным кадмиевым элементам Вестона и аккумуляторам. Аккумуляторы с кадмиевыми электродами имеют перед свинцовыми то преимущество, что могут быть нацело разряжены и в таком виде оставаться произвольно долгий срок, не теряя своих качеств. Особенно широко применяются кадмиеникелевые аккумуляторы . На всех американских спутниках аппаратура питалась от кадмиеникелевых батарей.
Кадмий употребляют в ювелирном деле в виде двойного сплава с золотом (зеленого цвета), тройного сплава с золотом и серебром и т.д. Кадмий придает различные оттенки изделиям из драгоценных металлов.
Металлический кадмий используют при сооружении атомных реакторов. Обладая большим сечением захвата тепловых нейтронов, кадмий является хорошим поглотителем нейтронов, что позволяет применять его для контрольных стержней, регулирующих скорость атомной реакции.
В работе (4) представлены результаты комплексного исследования свойств твердых растворов арсенид кадмия –арсенид цинка. Изучены их гальваномагнитные, термомагнитные, фотоэлектрические и оптические свойства, на основе которых определены зонные параметры растворов, проанализированы механизмы рассеяния носителей заряда. На основании полученных результатов исследованний твердых растворов в приемниках ИК-излучения.
Характерной тенденцией развития электроники является миниатюризация функциональных элементов и увелечение плотнасти их размещения в схемах Однако при этом возникают некоторые проблемы. Во-первых электронные оптические и другие свойства миниатюризированных элементов могут существенно отличаться от свойств соответсвующих обьемных фаз например появляется туннелированние электронов или размерное квантование энергетических уровней. Во-вторых миниатюризация приводит к экономическим проблемам вызванным сильним увелечением стоимости производства устройств все меньшего размера. Для наилучшей упорядоченности частиц и узкого распределения их по размерам необходима разработка эффективных методов синтеза.
В статье (5) представлен способ приготавление наночастиц полупроводникового материяла на основе кадмия- селенида кадмия( CdSe) .
В основе эксперементального подхода лежит реакция взаймадействия стеарата кадмия с селенидом трифенилфосфина,в среде гептадекана,и в приссутсвий поверхностно-активных веществ (особым образом влияющих на процесс формирования наночастиц) – олеиламина и трефинил фосфиноксида
Размеры и формы полученных наночастиц были определены методом просвечивающей микроскопии, на электронном микроскопе фирмы JEOL марки JEM-100B. Наночастицы имели форму ,близкую к сферической со средним диаметром 3-4 нм. На рисунке приведена микрофотография полученных наночастиц.
Структура полученных наночастиц была исследована методом дифракции электронов,и установлена,что в наночастицах CdSe реализуется кристаллическая структура типа вюрцита.
Полученные наночастиц могут являться хорошей моделью для создания систем передачи данных нового типа , работающих на особеннастях электролюменесценции наночастиц этого класса материалов.
В работе (6) сообщается о существовании следующих фосфидов : Cd3p2, Cd6P7, Cd7P10?, CdP2, CdP4,обладающих полупроводниковыми свойствами.
Авторами работы [1] разработаны условия синтеза новых координационных соединений на основе CdCl2*2,5Н2О и Е- капролактама. С помощью рентгенофазого анализа установлено, что индивидуальные соединения кадмия с Е – капролактамом соответствуют составу 1:1(1) и 1:2 (2)
Е – капролактама (1665см) в низкочастотную область, что свидетельствует о координации с кадмием через атом кислорода карбонильной группы.
При нагревании е – капролактама на кривой ДТА наблюдается два эффекта:первый при 69 С, не сопровождающийся потерей массы образца, соответствует плавлению вещества, второй при 262С, отражает процесс кипения, в результате которого происходит полная потеря массы
В последние годы возрос интерес к координационным полимерам. Это вызвано возможностью использования их как материалов с наноразмерными монодисперсными порами. Интересным свойством координационных полимеров любой размерности, является их способность переплетаться, образуя пространственно неразделимые, но химически не связанные конгломераты. Известно, что кристаллы, содержащие такие конгломераты, проявляют особые механические, электрические, магнитные, оптические и каталитические свойства.
Метод пересублимации в вакууме является основным при получении монокристаллов Cd3P2, CdP2 и CdP4.
Было установлено что критическое переохлаждение для образования зародышей CdP2 оставляет 3 – 8К, а температура зоны кристаллизации 980- 1010К. Для управления зародышеобразования и органичением разумными временами процесса, в ампулах большого диаметра (18-20мм) создавались более низкие пересыщения. Обеспечив необходимое зародышеобразование, проводилось перемещение ампулы со скоростью 0.6-0.8 мм/час, с увеличением температурного градиента. Были получены массивные монокристаллические були диаметром в основании до 20мм и длиной до 40-50мм (рисунок 2.8).

Рисунок 2.8-Монокристаллы дифосфида кадмия тетраганольный модификации.
Концентрирование кадмия по промпродуктам при пирометаллургическом способе переработки цинковых концентратов
Современная цинковая промышленность в настоящее время перерабатывает почти исключительно сульфидные цинковые руды, в которых цинк находится главным образом в виде цинковой обманки (сфалерита) ZnS [1].
Обогащение цинковых руд. Цинковые руды, из–за невысокого содержания в них извлекаемых металлов, как правило, в металлургическую переработку не поступают. Их предварительно обогащают.
Для обогащения полиметаллических руд, содержащих, кроме цинка, и другие ценные цветные металлы, применяют обычно методы селективной или коллективной флотации с последующей селекцией. Целью селективной флотации является разделение рудных минералов с получением по возможности монометаллических концентратов. Благодаря флотации на металлургические заводы поступают сравнительно богатые и чистые цинковые концентраты.
Содержание цинка в цинковых концентратах обычно колеблется от 40 до 60 %. Перерабатывают богатые (более 55 % цинка) и чистые концентраты, содержащие менее 8 % железа, менее 2 % свинца и других примесей, таких как галлий, индий, таллий и т.д.
В процессе обогащения сульфидных полиметаллических руд в цинковые концентраты переходит от 55 % до 78 % Cd; в хвостах флотации остается 18-38 % Cd [8].
Следует отметить, что в цинковом цикле флотации кадмий сопутствует цинку с отставанием по степени извлечения в концентрат в пределах 10- 30 %. Анализы цинковых концентратов, полученных из руд различных месторождений, показывают, что содержание кадмия колеблется в них от 0,1 до 0,6 %, наиболее часто оно составляет 0,2-0,3%.
Наиболее применяемые цинковые концентраты содержат, %: 50-55 Zn; 30-32 S; 1-3 Pb; 5-10 Fe; до 2 Cu; 0,25 Cd и немного CaO, MgO, SiO2, Al2O3, As, Co, Sb, Ag и др.
Цинк содержится в концентрате преимущественно в виде ZnS, поэтому вначале для удаления серы проводят окислительный обжиг.
При обжиге протекает следующая реакция:
2ZnS + 3O2 = 2ZnO + 2SO2. (1)
За счет азота воздуха и избыточного кислорода в обжиговых газах обычно содержится 5-6 % SO2. Такие обжиговые газы используют для производства серной кислоты.
При обжиге концентратов основная масса рассеянных элементов остается в огарке.
На дистилляционных заводах обжиг цинкового концентрата обычно не доводят до конца, оставляя в обожженном порошковидном концентрате около 10 % сульфидной серы. Для удаления оставшейся серы и спекания концентрата применяют агломерирующий обжиг, газы от которого иногда также используют для производства серной кислоты.
Полученный цинковый агломерат смешивают с углем – восстановителем, и направляют на дистилляцию, для этого его загружают в специальные керамические сосуды (реторты), помещенные в дистилляционную печь и нагревают.
Шихта в ретортах постепенно нагревается до температуры 1250- 1350 оС, и оксид цинка при этом восстанавливается согласно реакциям:
ZnO+C=Zn + CO (2)
ZnO+CO=Zn+CO2 (3)
Диоксид углерода, полученный по третьей реакции, восстанавливается углем по реакции СО2 + С=2СО, в результате чего в реторте в течение всего процесса дистилляции поддерживается восстановительная атмосфера.
В момент получения цинк находится в парообразном состоянии (цинк кипит при температуре 906 оС). Ретортные газы, содержащие пары цинка, поступают в другой сосуд – конденсатор, в котором цинк сжижается.
Из конденсатора жидкий цинк периодически вычерпывают. Часть паров цинка не успевает сконденсироваться в конденсаторе и, пройдя его, поступает в железный сосуд – аллонж. В последнем цинк улавливается из газов в виде тонкой пыли, или пуссьеры. В результате процесса получают, %: черновой цинк 75 – 86, пусьеру ~ 4, твердый остаток – раймовку ~ 7 [4].
При пирометаллургическом способе получения цинка в процессе восстановления и дистилляции кадмий наряду с цинком восстанавливается и в парообразном состоянии улетучивается вместе с парами цинка (рис.2) [1, 2, 8].
Поскольку восстановление кадмия из его кислородных соединений углеродом и оксидом углерода, а также его дистилляция протекают при более низких по сравнению с цинком температурах, то наиболее интенсивное улетучивание кадмия наблюдается в начальный период дистилляционного процесса получения цинка в горизонтальных ретортах. Дистилляция цинка в вертикальных непрерывно действующих ретортах и в электропечах сопровождается более или менее равномерным улетучиванием кадмия в течение всего процесса.
При конденсации паров металлов кадмий распределяется между металлическим цинком, пуссьерой и конденсаторной пылью. Ниже приведен состав продуктов дистилляции цинка при работе горизонтальных реторт периодического действия.
В пыли, которая образуется в конденсаторах на поверхности жидкого цинка, содержание кадмия невелико (0,13%). Конденсаторная пыль является оборотным продуктом, направляемым на повторную дистилляцию.
Достаточно высоким содержанием кадмия отличается цинковая пуссьера; последняя представляет собой слегка окисленную пыль цинка и кадмия с примесями железа, свинца, мышьяка, хлора, серы, угля и кремнекислоты. В зависимости от времени получения в процессе дистилляции пуссьера содержит различные количества кадмия. Пуссьера первых часов дистилляции более богата содержанием кадмия, чем последних. Масса пуссьеры составляет в среднем 5 % массы получаемого цинка. Из всего количества кадмия, который вводится с огарком в реторты печи, в пуссьеру переходит около 50 %.
Таблица 1
Состав продуктов дистилляции цинка, %
Продукты |
Cd |
Zn |
Pb |
Cu |
Fe |
Конденсаторная пыль |
0,13 |
61,1 |
0,78 |
0,23 |
3,25 |
Цинковая пуссьера |
0,7 – 1,07 |
84,05-90,12 |
0,95–1,47 |
− |
0,34-0,85 |
Среднее содержание кадмия в дистилляционном цинке колеблется в пределах 0,12 %. При среднем содержании цинка в огарке, равном 60 %, и коэффициенте извлечения при дистилляции 90 % в жидкий металл переходит
около половины кадмия, имевшегося в агломерате. В раймовке содержание кадмия примерно равно его содержанию в исходной руде (0,05 % Cd) [2, 8].
Так как при дистилляции не только оксид цинка, но и некоторые другие оксиды металлов (PbO, CdO и др.) восстанавливаются, то пары этих металлов также поступают в конденсатор, в результате цинк получается загрязненный – черновой, который затем рафинируют ректификацией. Полученный после рафинирования металл является конечным продуктом дистилляционного производства, при этом получающийся цинк содержит от 99,995 до 99,998 % Zn [1].
При ректификации цинка в тарельчатых колоннах кадмий концентрируется в пылевидной фракции. Содержание кадмия в последней достигает 40 % [8]. Схема распределения кадмия при пирометаллургической переработке цинкового концентрата представлена на рис. 2.6
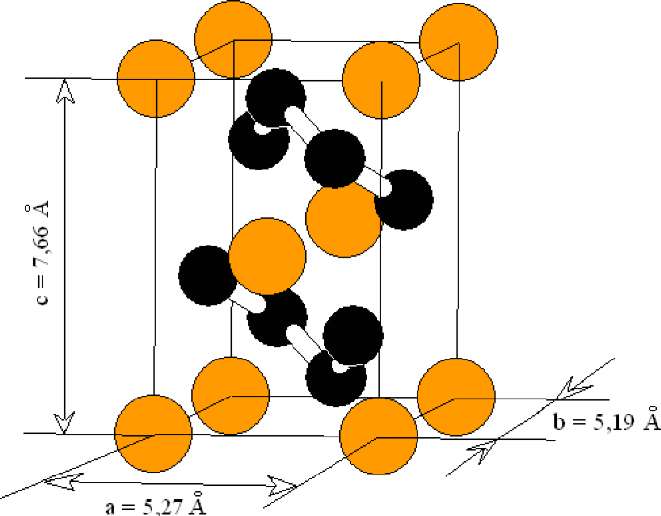
Рисунок 2.6-Кристаллическая структура тетрафосфида кадмия

Рис. 2. Схема распределения кадмия при пирометаллургической переработке цинкового концентрата.
