
- •Комплексті қосылыстар ерітіндідегі химиялық тепе-теңдігін өрнектеңіз. Тұрақтылық және тұрақсыздық константалары үшін теңдеулер келтіріп, арасындағы байланысты көрсет.
- •2.Жүйелік және бөлшектік анализ дегеніміз не? Мысал келтір. Катиондардың қышқылды-негіздік жіктелуін көрсетіңіз.
- •5. Аналитикалық химияда комплекстүзу процесінің қолданылуын көрсетіңіз ( ашу, бөліп алу, концентрлеу, бүркемелеу, иондарды анықтау). Мысалдармен жауабыңызды дәлелдеңіз.
- •6.Тотығу-тотықсыздану потенциал шамасына қандай факторлар әсер етеді?
- •7. Тұнбаның ерігіштік көбейтіндісі мен ерігіштігі арасында қандай байланыс бар?
- •8. Тұнбаның ерігіштігіне аттас иондардың қандай әсері бар?
- •8. Реалды және идеалды ерітінділер дегеніміз не? Активтілік, активтілік коэффицент пен ерітіндінің иондық күші қалай есептеледі?
- •10. Тұнбаның ерігіштігіне күшті электролиттің қандай әсері бар?
- •11. Гомогенді жүйелер дегеніміз не? Массалар әрекеттесу заңын тұжырымдаңыз. Гомогенді тепе-теңдік тұрақтыларын (термодинамикалық, концентрациялық шартты) келтіріңіз.
- •12. Титриметриялық ерітіндінің концентрациясын өрнектеу тәсілдері мен өзара байланысын көрсетіңіз.
- •13. Титриметриялық анализдің түрлерін көрсетіңіз. Реакцияларға қойылатын талаптар.
- •14. Бастапқы стандарттар және екінші ретті стандарттарға анықтама беріңіз. Бастапқы стандарттарға қойылатын талаптар. Фиксоналдар дегеніміз не? Мысал келтіріңіз.
- •15. Тура, кері және жанама титрлеу арасындағы айырмашылықты көрсетіңіз.
- •16. Титрлеу кезінде индикатор түсі өзгеруін қалай түсіндіруге болады. Мысал келтіріңіз.
- •17. Комплексонометрлік титрлеудің маңызын түсіндіріп, мысал кетіріңіз.
- •19. Комплексондар дегеніміз не? Метал иондарымен әрекеттескенде комплексондардың ерекшелігін көрсетіңіз.
- •20. Аморфты және ірі кристалды тұнбаларды алу жағдайларын көрстіңіз.
7. Тұнбаның ерігіштік көбейтіндісі мен ерігіштігі арасында қандай байланыс бар?
Қиын еритін қосылыстар – тұнбалардың түзілу реакциясы аналитикалық химияда сапалық талдауда иондарды анықтау мен бөлу үшін және сандық талдауда гравиметрлік және титриметрлік тұндыру анықтаулары үшін кең қолданылады. Тұнба түзілгеннен кейін тұнба мен қаныққан ерітінді арасында жылжымалы гетерогенді тепе-теңдік орнайды:
AgI ↔ Ag+ + I-
тұнба қаныққан еріт-лер
Тепе-теңдік жағдайында тұнба мен қаныққан ерітінді арасында процестер тура және кері бағытта жүреді, олардың жылдамдықтары тең.
Теңдеудің сол жағындағы тұрақты шаманы ЕКAgI арқылы белгілейміз, сонда:
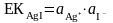 (10)
(10)
Ерігіштік көбейтіндісі үшін теңдеуді тұнба/қаныққан ерітінді жүйесіндегі тепе-теңдік жағдайы нүктесінен қарастыруға болады. Тұнбалар суда аз ериді, сондықтан тұнба үстіндегі қаныққан ерітінді идеалды жүйеге жақын сұйытылған ерітінді болып табылады. Одан басқа, тұнба молекулаларының түзілу процесі қайтымды. Сондықтан гетерогенді тепе-теңдікті тепе-теңдік константасымен сипаттауға болады:
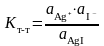 (11)
(11)

(12)
Кез-келген химиялық реакция тұрақты қысым мен температурада жүреді, сондықтан термодинамикалық қатынаста тұнба мен қаныққан ерітінді арасындағы гетерогенді тепе-теңдікті Гиббстің бос молярлы энергиясы арқылы қарастыру керек.
Жалпы түрде келесі гетерогенді тепе-теңдік бар дерлік:
AmBn ↔ mA + nB
тұнба қанық еріт-лер
Сол жақтың тұрақты шамаларын ерігіштіктің көбейтіндісімен белгілейміз:
 (22)
(22)
Берілген теңдеу ерігіштіктің термодинамикалық көбейтіндісін жалпы түрде сипаттайды. Иондардың белсенділігін олардың концентрациясының белсенділік коэффициентіне көбейтіндісімен анықталатынын ескерсек, ерігіштік көбейтіндісін былай көрсетуге болады:
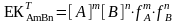 (23)
(23)
Иондар концентрацияларының көбейтіндісі – ерігіштіктің концентрациялық көбейтіндісі деп аталады және тұрақты қысымда, температурада және қиын еритін қосылыстың тұрақты сандық сипаттамасының тұрақты күшіне ие:
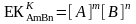 (24)
(24)
Сонда
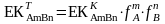 (25)
(25)
Бұл теңдеумен анықтамада көрсетілген ерігіштік көбейтіндісінің термодинамикалық шамасы бойынша және
иондардың белсенділік коэффициенті бойынша ерігіштіктің концентрациялық көбейтіндісін есептеуге болады:
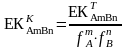 (26)
(26)
Суда қиын еритін қосылыстар жағдайында, көптеген тұнбалар сондай, ерітіндінің тұрақты иондық күшінде ерігіштіктің концентрациялық көбейтіндісін қолдану ыңғайлы.
Қиын еритін электролит ерігіштігінің көбейтіндісін табу үшін берілген температурада оның ерігіштігін білу қажет. Ерігіштік пен ерігіштік көбейтіндісінің арасында байланыс орнатамыз. Келесі гетерогенді тепе-теңдіктерді қарастырайық:
AmBn ↔ mA + nB
тұнба қанық еріт.
Тұнба ерігіштігін S арқылы белгілейміз. Сонда тұнба үстіндегі қаныққан ерітіндіде А ионының mS және В иондарының nS түзіледі. Ерігіштік көбейтіндісінің теңдеуін ерігіштік арқылы жазуға болады:
(27)
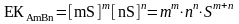
Бұдан тұнба ерігіштігі мынаған тең:
 (28)
(28)
Иондық күші 0-ге тең болмағанда, басқа күшті электролиттер қатысында тұнба ерігіштігі көбейетіндігі жақсы белгілі. Басқа күшті электролиттер қатысында тұнба ерігіштігін есептегенде ерітіндінің иондық күшін ескеру керек.
 (29)
(29)
