
- •1.Классификация органических соединений-
- •Формулы органических веществ по классам:
- •5. Применение алканов
- •6. Классификация непредельных углеводородов.
- •7. Номенклатура непредельных углеводородов.
- •13. Классификация спиртов.
- •14. Общая характеристика спиртов (определение, гомологический ряд).
- •19. Применение спиртов.
- •25. Реакция полимеризации.
- •28. Физико-химические свойства карбоновых кислот.
- •29. Номенклатура карбоновых кислот.
- •30. Качественные реакции на альдегидную группу.
- •46.Классификация солей
- •47.Номенклатура оксидов
- •48.Номенклатура кислот
- •63. Краткая характеристика металлов.
- •Строение атомов неметаллов
- •56.Метод ионный баланс
1.Классификация органических соединений-
Органические соединения классифицируют по двум основным признакам: строению углеродного скелета и функциональным группам.
По строению углеродного скелета различают ациклические, карбоциклические и гетероциклические соединения.
Ациклические соединения – содержат открытую цепь атомов углерода.
Карбоциклические соединения – содержат замкнутую цепь углеродных атомов и подразделяются на алициклические и ароматические.
К алициклическим относятся все карбоциклические соединения, кроме ароматических. Ароматические соединения содержат циклогексатриеновый фрагмент (бензольное ядро).
Гетероциклические соединения - содержат циклы, включающие наряду с атомами углерода один или несколько гетероатомов.
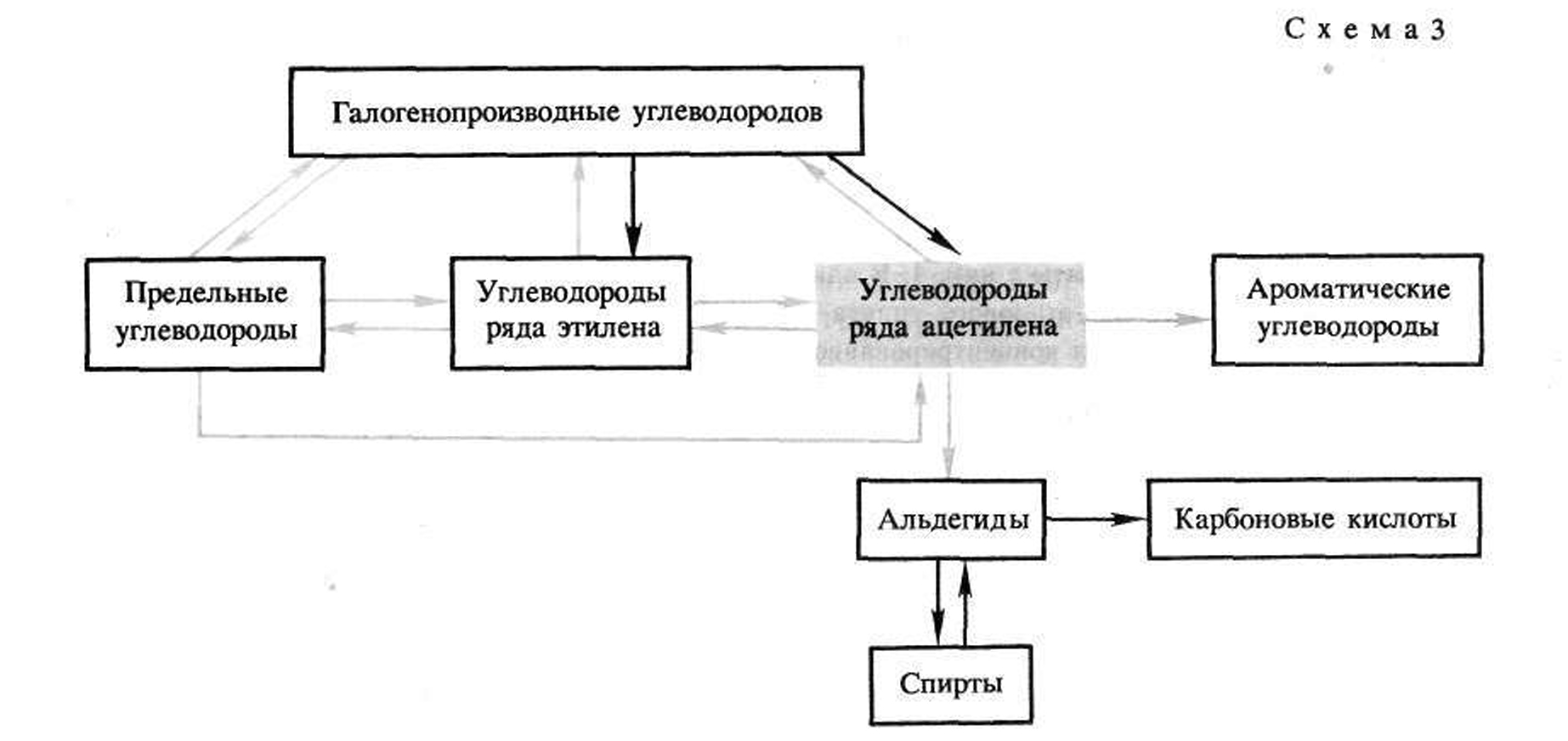
К углеводородам относятся: ациклические соединения ,предельные углеводороды (алканы), непредельные углеводороды ,алкены; алкины; алкадиены.циклические соединения:, соединения карбоциклические: , алициклические;, ароматические.соединения гетероциклические.
Есть также иные классы органических соединений, в составе которых углерод соединяется с другими веществами, кроме водорода: спирты и фенолы; альдегиды и кетоны; карбоновые кислоты; сложные эфиры; липиды; углеводы: моносахариды; олигосахариды; полисахариды. мукополисахариды. амины. аминокислоты; белки; нуклеиновые кислоты.
Формулы органических веществ по классам:
Алканы - CnH2n+2
Циклоалканы - CnH2n
Алкены - CnH2n
Алкадиены - CnH2n-2
Алкины - CnH2n-2
Арены - CnH2n-6
Предельные одноатомные спирты - R-OH / CnH2n+1 – OH
Простые эфиры - R – O – R’ / CnH2n+1– O – CnH2n+1
Альдегиды –

Кетоны –
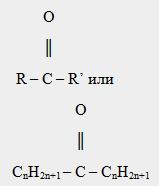
2. Общая характеристика предельных углеводородов (определение, гомологический ряд).
Углеводороды - простейшие органические соединения, состоящие из двух элементов: углерода и водорода. Предельными углеводородами, или алканами (международное название), называются соединения, состав которых выражается общей формулой С n Н2n+2, где n - число атомов углерода. В молекулах предельных углеводородов атомы углерода связаны между собой простой (одинарной) связью, а все остальные валентности насыщены атомами водорода. Алканы называют также насыщенными углеводородами или парафинами (Термин «парафины» означает «имеющие малое сродство»).
3. Номенклатура алканов
При отрыве атома водорода от молекулы алкана образуются одновалетные частицы, называемые углеводородными радикалами (сокращенно обозначаются буквой R). Названия одновалентных радикалов производятся от названий соответствующих углеводородов с заменой окончания –ан на -ил. Вот соответствующие примеры:
СН3—СН2—СН2—СН3 СН3—СН2—СН2—СН2—СН2—СH 2 —СН3
н-бутан н-гептан
(нормальный бутан) (нормальный гептан)
4. Физико-химические свойства алканов
Физические св.- Температуры плавления и кипения увеличиваются с молекулярной массой и длиной главной углеродной цепи
При нормальных условиях неразветвлённые алканы с CH4 до C4H10 — газы; с C5H12 до C13H28 — жидкости; начиная с C14H30 и далее — твёрдые вещества.
Температуры плавления и кипения понижаются от менее разветвленных к более разветвленным. Так, например, при 20 °C н-пентан — жидкость, а неопентан — газ.
Газообразные алканы горят бесцветным или бледно-голубым пламенем с выделением большого количества тепла.
Химические св.- Алканы имеют низкую химическую активность. Это объясняется тем, что единичные связи C—H и C—C относительно прочны, и их сложно разрушить. Поскольку углеродные связи неполярны, а связи С—Н малополярны, оба вида связей малополяризуемы и относятся к σ-виду, их разрыв наиболее вероятен по гомолитическому механизму, то есть с образованием радикалов.
Реакции радикального замещения: Галогенирование: Галогенирование алканов протекает по радикальному механизму. Для инициирования реакции необходимо смесь алкана и галогена облучить УФ-излучением или нагреть. Галогенирование — это одна из реакций замещения. В первую очередь галогенируется наименее гидрированый атом углерода (третичный атом, затем вторичный, первичные атомы галогенируются в последнюю очередь). Галогенирование алканов проходит поэтапно — за один этап замещается не более одного атома водорода:
Сульфохлорирование (реакция Рида): При облучении УФ-излучением алканы реагируют со смесью SO2 и Cl2, После того, как с уходом хлороводорода образуется алкильный радикал, присоединяется диоксид серы. Образовавшийся сложный радикал стабилизируется захватом атома хлора с разрушением очередной молекулы последнего. Алканы реагируют с 10 % раствором азотной кислоты или оксидом азота NO2 в газовой фазе при температуре 140 °C и небольшом давлении с образованием нитропроизводных. Реакции окисления: Горение: Основным химическим свойством предельных углеводородов, определяющих их использование в качестве топлива, является реакция горения. Пример:
CH4 + 2O2 → CO2 + 2H2O + Q.
Значение Q достигает 46 000 — 50 000 кДж/кг.
Каталитическое окисление: Могут образовываться спирты, альдегиды, карбоновые кислоты. Окисление также может осуществляться воздухом. Процесс проводится в жидкой или газообразной фазе. В промышленности так получают высшие жирные спирты и соответствующие кислоты.
Термические превращения алканов: Разложение: Реакции разложения происходят лишь под влиянием больших температур. Повышение температуры приводит к разрыву углеродной связи и образованию свободных радикалов.
Крекинг: При нагревании выше 500 °C алканы подвергаются пиролитическому разложению с образованием сложной смеси продуктов, состав и соотношение которых зависят от температуры и времени реакции. При пиролизе происходит расщепление углерод-углеродных связей с образованием алкильных радикалов.
В 1930—1950 гг. пиролиз высших алканов использовался в промышленности для получения сложной смеси алканов и алкенов, содержащих от пяти до десяти атомов углерода. Он получил название «термический крекинг».
