
- •Лабораторна робота №3
- •Самостійна робота на занятті Якісні реакції на полісахариди і. Якісні реакції, які проводяться на сухій сировині
- •Лабораторна робота №4
- •2.Проведіть якісні реакції на сім’яні та кісточкові олії та реакції дійсності риб’ячої олії. Запишіть спостереження у журнал.
- •3.Визначення коефіцієнту заломлення
- •Контрольні питання
- •Лабораторна робота №8
- •Самостійна позааудиторна робота
- •1. Визначення гемолітичного індексу (метод Кофлера).
- •2. Кількісне визначення гліциризинової кислоти (гф X, с. 573) у корені солодки.
2.Проведіть якісні реакції на сім’яні та кісточкові олії та реакції дійсності риб’ячої олії. Запишіть спостереження у журнал.
Дослід 7. Реакція на насінні олії (реакція Белієра). В пробірку наливають 2 мл олії, обережно наливають по 1 мл азотної кислоти та 0,15% розчину резорцину у бензолі. Вміст енергійно струшують. Жирні олії, отримані із насіння, на протязі 5 с дають червоне або синьо-фіолетове забарвлення, яке швидко зникає. При розділенні шарів забарвлення переходить у бензольний шар.
Дослід 8. Реакція на кісточкові олії (реакція Біберга). У пробірку наливають 2,5 мл олії, обережно додають 1 мл охолодженої суміші рівних об’ємів води та кислот сірчаної та азотної концентрованих.
Слабо-жовте забарвлення розчину вказує на мигдальну олію, червоний колір на персикову або абрикосову олію.
Дослід 9. Реакція на риб’ячий жир. 0,1 г жира розчиняють у 1 мл хлороформу та додають 5 мл розчину стибію (ІІІ) хлорида, утворюється нестійке блакитне забарвлення (вітамін А).
Розчин 1 краплі жиру у 1 мл хлороформу при струшуванні з краплею сірчаної концентрованої кислоти забарвлюється у синьо-фіолетовий колір, який переходить у бурий (ліпохром).
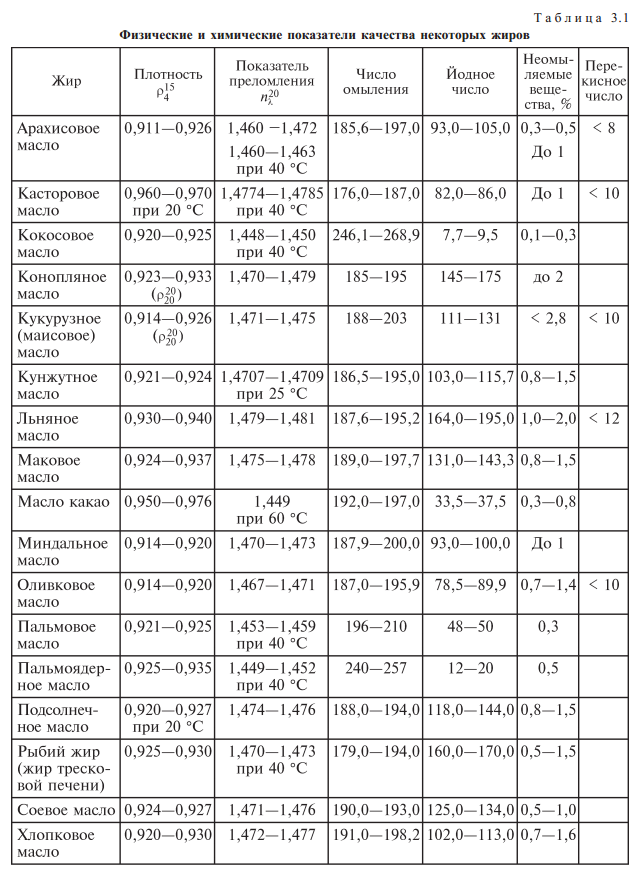
3.Визначення коефіцієнту заломлення
Коефіцієнт заломлення визначають за допомогою рефрактометра. Коефіцієнт заломлення залежить від природи речовини, температури та довжини хвилі.
ТЕМА: Фітохімічний аналіз ЛРС, що вміщує ефірні олії.
Мета: проводити кількісне визначення вмісту ефірної олії в зразках сировини за методом ДФ ХІ (перегонка з водяною парою); виявляти за допомогою якісних реакцій основні групи хімічних сполук в ефірних оліях.
Питання до самопідготовки:
1.Назвіть методики кількісного визначення ефірних олій в залежності від їх фізичних властивостей.
2.Вкажіть групи хімічних сполук, які можна виявити в ефірних оліях за допомогою якісних реакцій.
3.Охарактеризуйте за родинами місця накопичення ефірних олій в рослинах.
4.Перелічіть фармакопейні методи встановлення справжності та доброякісності ефірних олій.
5.Вкажіть хімічний склад листя м'яти, плодів коріандру, плодів фенхелю, листя евкаліпту, листя шавлії, трави чебрецю звичайного, трави материнки, квітів лаванди, кореневища з коренями валеріани.
6.Назвіть лікарські засоби, які готуються з ефіроолійної сировини, їх фармакологічну дію та застосування в медицині.
Список лікарських рослин, які містять ефірні олії:
Самостійна робота на занятті:
Робота проводиться на зразках сировини: плоди (олія) коріандру, плоди (олія) фенхелю, листя (олія) м'яти перцевої, листя (олія) евкаліпту, листя шавлії, трава чебрецю звичайного, трава материнки, квіти та олія лаванди, кореневища з коренями валеріани.
Завдання 1. Провести аналіз зразка ефірної олії Визначити справжність (колір, запах, смак, розчинність).
Колір. 10,0 мл досліджуваної ефірної олії поміщають у циліндр або пробірку з прозорого скла діаметром 2-3 см і спостерігають колір та прозорість на світлі.
Запах. 2 краплини олії наносять на смужку фільтрувального паперу довжиною 12 см і шириною 5 см так, щоб олія не змочувала краї паперу. Порівнюють запах досліджуваної олії через кожні 15 хв. з запахом контрольного зразка, нанесеного так само на фільтрувальний папір. Протягом 1 год. запах досліджуваного і контрольного зразків повинен бути однаковим.
Смак. Краплину ефірної олії, нанесеної на смужку фільтрувального паперу, або суміш краплі олії з 1 г цукрової пудри пробують на язик.
Розчинність. 1 мл ефірної олії наливають у мірний циліндр місткістю 10 мл і, збовтуючи, поступово доливають з бюретки по 0,1 мл спирту певної концентрації (вказаної у відповідній НТД) при 200С до повного розчинення олії.
Встановити чистоту: відсутність етилового спирту, жирних та мінеральних олій.
Спирт етиловий.
Кілька краплин ефірної олії наносять на воду, налиту на годинникове скло. При спостереженні на чорному фоні не повинно бути помітного помутніння навколо краплин олії.
1 мл ефірної олії наливають в пробірку, закупорюють її розпушеною ватою, всередину якої поміщають кристалик фуксину, і вміст пробірки доводять до кипіння. При наявності спирту пара його розчиняє фуксин і забарвлює вату в фіолетово-рожевий колір.
Жирні та мінеральні олії.
1 мл ефірної олії збовтують в пробірці з 10 мл етилового спирту. Не повинно з'являтися помутніння та краплини жирної олії.
1 краплю ефірної олії нанесіть на смужку фільтрувального паперу і підсушіть її, нагріваючи над плитою. Спостерігайте за зміною стану плями.
Завдання 2. провести якісні реакції на наявність певних хімічних сполук в ефірних оліях.
На альдегіди і кетони.
Одержання оксимів. До 1-2 крапель ефірної олії добавляють 3 краплі спиртового розчину хлористоводневого гідроксиламіну (15 г хлористоводневого гідроксиламіну в 100 мл 80%-го етилового спирту) та декілька краплин метилоранжу. При наявності карбонільних сполук на холоді чи при нагріванні на киплячій водяній бані суміш забарвлюється в рожевий колір.
Нітропрусидна реакція. Декілька крапель ефірної олії змішують з однаковою кількістю свіжоприготовленого розчину нітропрусиду натрію, підлужнюють. Розчин забарвлюється в червоний колір, який поступово зникає при стоянні. Наявність подвійного зв'язку, розміщеного близько біля карбонільної групи, сприяє реакції. Карвон, пулегон, цитраль дають червоне забарвлення, а камфора, фенхон, ментон, цитранеаль не реагують.
На феноли.
Реакція з заліза (ІІІ) хлоридом. До 1 мл концентрованого спиртового розчину ефірної олії додають 3-4 краплини розчину заліза (ІІІ) хлориду. Повинно з'явитися синє, фіолетове, зелене або червоне забарвлення (карвакрол і тимол не реагують). Олія, до складу якої входить карвакрол, при нагріванні з натрію гідроксидом і хлороформом забарвлюється в червоний колір.
На азуленогени.
Реакція Сабетая. 5-10 крапель ефірної олії розчиняють в 1-2 мл хлороформу і додають по краплях 0,5-1 мл 5%-го розчину брому в хлороформі. Через декілька хвилин при наявності азуленогенів з'являється зелене, блакитне або фіолетове забарвлення. Реакція проходить ще швидше і виразніше, якщо ефірну олію спочатку розчинити в оцтовій кислоті, а потім обробити розчином брому в хлороформі.
Реакція Мюллера. На паперовий фільтр діаметром 4-5 см нанесіть 4-5 крапель спиртового розчину ефірної олії і після випаровування спирту в центр плями додайте 4-5 крапель реактиву Мюллера (розчин 1,0 г n-диметиламінобензальдегіду в суміші 5,0 г фосфатної і 50,0 г ацетатної кислот, дистильованої води до 100 мл). Вміст пробірки забарвлюється в зелений, блакитний або фіолетовий колір.
На підставі проведеного дослідження зробити висновок про наявність в досліджуваній ефірній олії тих чи інших сполук.
Завдання 3. визначити кількісний вміст ефірної олії в запропонованому зразку сировини за методом дфу 1-го вид. додаток 1.
Перегонка з водяною парою (замалювати апарат).
Використовують ретельно очищений прилад. Визначення проводять відповідно до особливостей випробовуваного зразка. Зазначений об’єм рідини для перегонки поміщають у колбу, додають кілька шматків пористого фарфору і з’єднують з конденсуючою системою. Додають воду через наливну лійку до певного рівня. Пробку видаляють і додають зазначену кількість ксилолу, використовуючи піпетку таким чином, щоб її кінчик знаходився в нижній частині трубки. Установлюють пробку і переконуються, що жолоб на трубці суміщається з отвором. Рідину в колбі нагрівають до кипіння і регулюють швидкість перегонки від 2 до 3 мл на хвилину, якщо немає інших зазначень в окремій статті.
Розрахунок вмісту ефірної олії в ЛРС.
Після охолодження визначають відстояний у приймачі об'єм олії і розраховують її вміст:
а) у ваго-об'ємних відсотках за формулою:
Х=А·100/Б , де А – об'єм ефірної олії, мл;
Б – наважка повітряно сухої сировини, г;
б) у вагових відсотках – отриманий вище результат помножити на густину олії;
в) у ваго-об'ємних відсотках в перерахунку на абсолютно суху сировину за формулою:
Х1=V·100·100/m·(100 – W), де V – об'єм ефірної олії, мл;
m – маса сировини, г;
W – вологість сировини, %.
Оцінка якості сировини.
На основі проведеного аналізу зробити висновок про відповідність досліджуваного зразка сировини вимогам НТД.
Завдання 4. Визначити числові показники ефірних олій.
Фізичні числові показники.
Визначення показника заломлення за методикою ДФ ХІ. Ознайомтеся за інструкцією з роботою рефрактометра, перевірте точність його показників з допомогою води, яка має показник заломлення 1,3330 (при 20оС), потім визначте показник заломлення досліджуваної ефірної олії. Порівняйте отримані дані з коефіцієнтом заломлення стандартного зразка, зробіть висновок про їх ідентичність.
Хімічні числові показники.
Кислотне число. Відважують 1,5-2 г олії з точністю до 0,1 г в колбі на 250 мл зі шліфом, розчиняють у 5-10 мл нейтралізованого етилового спирту і титрують 0,1 М розчином калію гідроксиду у присутності 3-5 крапель фенолфталеїну до рожевого забарвлення, яке не зникатиме протягом 30 сек. (інколи забарвлення швидко зникає, що свідчить про початок омилення складних ефірів, а тому титрувати слід швидко і кінцем титрування вважати момент появи першого забарвлення, яке затримується на 2-3 сек.). Для олії з незначним КЧ (до 1) титрування проводять з мікробюретки. Обчислюють КЧ за формулою:
КЧ = V · 5,61/ m ,
де V – кількість 0,1 М розчину натрію гідроксиду, затраченого на титрування, мл;
m – наважка, г;
5,61 – кількість калію гідроксиду, що міститься в 1 мл 0,1 М розчину калію гідроксиду, мг.
Ефірне число. До розчину після визначення кислотного числа додають 20 мл 0,5 М спиртового розчину калію гідроксиду і нагрівають на водяній бані в колбі зі зворотнім холодильником 1 год., підтримуючи легке кипіння. Після припинення нагрівання розчин розводять 100 мл води, додають декілька краплин фенолфталеїну, надмір калію гідроксиду відтитровують 0,25 М розчином сульфатної кислоти до зникнення рожевого забарвлення. Розраховують ефірне число за формулою:
ЕЧ = V · 28,05/ m ,
де V – об'єм розчину 0,5 М калію гідроксиду, затраченого на омилення ефірів, мл;
m – наважка олії, г;
28,05 – кількість калію гідроксиду, що міститься в 1 мл 0,5 М розчину калію гідроксиду, мг.
Ефірне число використовують для обчислення вмісту у відсотках складних ефірів або зв'язаних спиртів за формулою:
ЕЧ1 = ЕЧ · Мr · 100/ 56,1 · 1000 = ЕЧ · Мr/ 561,
де Мr – молекулярна маса ефіру або спирту;
56,1 – молекулярна маса калію гідроксиду.
Ефірне число після ацетилювання. 10 г олії поміщають в спеціальну круглодонну колбу для ацетилювання, додають 10 мл оцтового ангідриду та 2 г свіжосплавленого натрію ацетату, закривають зворотнім холодильником і нагрівають на піщаній бані, підтримуючи слабке кипіння протягом 2 год. Після охолодження в колбу через холодильник додають 25 мл води і нагрівають на водяній бані 15 хв., час від часу збовтуючи. Суміш переносять у ділильну лійку, після відстоювання водний розчин виливають, а олію порціями промивають збовтуванням з 50 мл насиченого розчину хлориду натрію до нейтральної реакції (індикатор метиловий оранжевий), олію двічі промивають водою по 20 мл, щоб видалити сліди хлориду натрію, зневоднюють безводним сульфатом натрію і фільтрують.
1-2 г отриманої олії (з точністю до 0,001 г) зважують в конічній колбі, розчиняють в 5 мл спирту, нейтралізують 0,5 М спиртовим розчином калію гідроксиду по фенолфталеїну, а потім визначають ефірне число, як описано вище. Розраховують ефірне число після ацетилювання за формулою:
ЕЧ2 = 28,05 · V1/ m1,
де V1 – об'єм 0,5 М розчину калію гідроксиду, затраченого на омилення ефірів після ацетилювання, мл;
m1 – наважка, г;
28,05 – кількість калію гідроксиду, що міститься в 1 мл 0,5 М гідроксиду, мг.
Вміст вільних спиртів у відсотках розраховують за формулою:
ЕЧ3 = (ЕЧ2 – ЕЧ) · Мr/ 561 – 0,42 (ЕЧ2 – ЕЧ) ,
де Мr – молекулярна маса спирту;
0,42 – поправка на збільшення маси ефірної олії за рахунок приєднання ацетильного залишку (42 – різниця в молекулярній масі між вільним спиртом і його оцтовим ефіром).
Загальний вміст спиртів визначається сумою зв'язаних та вільних спиртів.
Лабораторна робота №6
ТЕМА: Кардіоглікозиди
АКТУАЛЬНІСТЬ: Лікарські рослини та сировина, що вміщують серцеві глікозиди, проявляють специфічну дію на серце, а у великих дозах вони є серцевими отрутами.
Джерелом одержання багатьох лікарських засобів і лікарських форм при серцевій недостатності на даний час є лікарська рослинна сировина (дигітоксин, кордигіт, дигоксин, медилазид, целанід, ланатозид, дигіцил, дигален-нео, корглікон, строфантин К, строфантидин ацетат, адонізид, адоніс-бром, кардіовален, настоянки, екстракти, мікстури, настої, тощо).
Для практичної діяльності провізора необхідні знання номенклатури лікарських рослин і сировини, що вміщують серцеві глікозиди у відповідності з програмою і Державним реєстром, уміння проводити їх заготівлю, сушіння і зберігання, а також аналізу для встановлення тотожності і доброякісності.
НАВЧАЛЬНІ ЦІЛІ:
ЗНАТИ:
назви лікарських рослин (ЛР), сировини і родини на латинській та українській мовах;
життєві форми та морфологічні ознаки ЛР;
ареал, еколого-фітоценотичні умови зростання та райони культури ЛР (джерела сировинної бази);
фізико-хімічні властивості серцевих глікозидів, їх класифікацію та хімічну структуру;
хімічний склад ЛРС, локалізацію серцевих глікозидів у сировині, вплив природних факторів на їх нагромадження;
лікарські засоби, які отримують із сировини, що вміщує серцеві глікозиди, застосування їх в медицині;
правила збирання, сушіння та зберігання ЛРС, а також правила техніки безпеки при роботі з сировиною, що вміщує серцеві глікозиди.
ВМІТИ:
визначати фенофазу збирання ЛРС;
розпізнавати ЛР і відрізняти ботанічно близькі до них види;
застосовувати раціональні способи збирання і зберігання ЛРС;
проводити первинну обробку ЛРС;
проводити аналіз ЛРС за зовнішніми та мікроскопічними ознаками і визначати її тотожність;
проводити виявлення серцевих глікозидів за допомогою якісних реакцій і хроматографії;
визначати кількісний вміст серцевих глікозидів в ЛРС.
САМОСТІЙНА ПОЗААУДИТОРНА РОБОТА
Вивчити теоретичний матеріал до теми:
Поняття про серцеві глікозиди, їх класифікацію. Особливості структури аглікону і вуглеводного компоненту. Фізико-хімічні властивості. Розповсюдження в рослинному світі. Особливості нагромадження серцевих глікозидів у лікарських рослинах. Особливості заготівлі, сушіння і зберігання сировини, що вміщує серцеві глікозиди. Аналіз сировини (біологічна стандартизація, хімічні методи). Будова та класифікація серцевих глікозидів. Особливості структури аглікону і вуглеводного компоненту. Фізико-хімічні властивості кардіостероїдів. Методи виділення та дослідження рослинної сировини. Реакції ідентифікації на стероїдне ядро, бутенолідне кільце, вуглеводний компонент. Методи кількісного визначення серцевих глікозидів (біологічна стандартизація, фізико-хімічні методи). Зв’язок між хімічною будовою і фармакологічною дією серцевих глікозидів.
Переробка ЛРС, шляхи використання в медичній практиці. Результати наукових досліджень лікарських рослин, що вміщують серцеві глікозиди.
Об'єкти вивчення:
1. Офіцинальні ЛР і ЛРС: наперстянка пурпурова, великоквіткова і шерстиста (листя), горицвіт весняний (трава), конвалія травнева (трава, листя, квіти), жовтушник розлогий (трава), строфант Комбе (насіння).
2. ЛР, що використовуються в гомеопатії: кендир конопляний, конвалія травнева, наперстянка пурпурова, строфант Комбе.
3. ЛР і ЛРС народної медицини: наперстянка іржава (листки) – Digitalis ferruginea, обвійник грецький (кора) – Periploca graeca, олеандр звичайний (листя) – Nerium oleander, чемерник червонуватий (кореневища з коренями) - Helleborus purpurascens, ваточник сірійський (листя) - Asclepias syriaca, секуринега мечовидна (насіння) - Securinega securidata, сиренія сиза (трава, насіння) - Syrenia cana, бруслина європейська (насіння) - Еuonymus eurоpea, в'язіль барвистий (трава, насіння) - Соronilla vагіа.
КОНТРОЛЬНІ ПИТАННЯ
Дайте визначення серцевих глікозидів. Напишіть класифікацію, наведіть приклади.
Рослини яких родин вміщують кардіостероїди, в яких органах рослин накопичуються в основному ці сполуки?
Як виявити серцеві глікозиди в ЛРС у польових умовах?
Які особливості заготівлі листків наперстянки (час заготівлі, умови сушіння, зберігання сировини)?
Вкажіть основні анатомо-діагностичні ознаки листка наперстянки, трави горицвіту весняного.
Перелічіть рослини, у яких суцвіттям є одностороння китиця.
Назвіть можливі домішки до листків конвалії та їх відмінні діагностичні ознаки.
Яка група серцевих глікозидів проявляє різко виражену кумулятивну дію?
Що роблять із сировиною, якщо її реальна біологічна активність нижча чи вища за фармакопейну?
Дайте класифікацію серцевих глікозидів. Вкажіть джерела кожної групи кардіостероїдів.
Охарактеризуйте хімічні і фізичні властивості серцевих глікозидів.
Обгрунтуйте і опишіть способи виділення серцевих глікозидів з рослинної сировини і їх очищення від супутніх речовин.
Опишіть якісні реакції визначення серцевих глікозидів, їх хімізм і специфічність.
На прикладі наперстянки шерстистої поясніть перетворення первинних глікозидів в процесі сушки і зберігання ЛРС.
Вкажіть переваги і недоліки препаратів групи наперстянки і строфанту.
Біологічні методи стандартизації лікарської сировини. Які є одиниці дії? Фізико-хімічні методи кількісного визначення кардіостероїдів в рослинній сировині. Опишіть принципи методів.
Напишіть будову основних агліконів кардіостероїдів групи карденолідів (дигітоксигенін, гітоксигенін, строфантидин), їх первинних (геноїнних) і вторинних глікозидів: пурпуреаглікозид А і Б, дигіланіди (ланатозиди) А, Б і С, К-строфантозид, дигітоксин, цимарин, К-строфантин-β, адонітоксин, конвалотоксин; хімічна будова глюкози, рамнози і дезоксицукрів – дигітоксози, цимарози. Вкажіть латинські назви сировинних джерел, що вміщують перераховані серцеві глікозиди і дезоксицукри.
Вкажіть хімічний склад і лікарські препарати рослин: наперстянка пурпурова, великоквіткова, шерстиста, строфант Комбе, горицвіт весняний, конвалія травнева, жовтушник розлогий.
САМОСТІЙНА АУДИТОРНА РОБОТА
Виконати лабораторні роботи:
ЗАВДАННЯ 1. Визначити тотожність і доброякісність цілої ЛРС за зовнішніми ознаками:
вивчити і описати зовнішні ознаки сировини;
визначити тотожність ЛРС за визначником і порівняти її з описом згідно АНД;
сформулювати висновок про тотожність, вказати від якої рослини походить, написати латинську і українську назви ЛРС, рослини і родини.
Об'єкти аналізу: листки наперстянки пурпурової, листки наперстянки шерстистої, насіння строфанту, трава горицвіту весняного, трава, листки, квіти конвалії, трава жовтушника лакфеолевидного.
ЗАВДАННЯ 2. Визначити тотожність і доброякісність подрібненої ЛРС за зовнішніми і мікроскопічними ознаками:
вивчити і описати зовнішні ознаки подрібненої ЛРС;
виготовити мікропрепарат, вивчити мікроскопічну будову, встановити та замалювати діагностичні ознаки;
визначити тотожність подрібненої ЛРС за визначником;
зробити висновок про тотожність ЛРС, вказати від якої рослини походить, до якої родини належить на латинській і українській мовах;
Об'єкти аналізу: листки наперстянки пурпурової, листки конвалії, трава горицвіту весняного і жовтушника розлогого.
Характерні мікроскопічні діагностичні ознаки цілої та подрібненої ЛРС.
Мікропрепарат листка наперстянки пурпурової: клітини епідермісу звивистостінні, продихи переважно на нижній стороні листка (аномоцитний тип). Простих волосків багато, особливо на нижній стороні, 2-8-клітинні, зі слабобородавчастою кутикулою і тонкими стінками, окремі клітини волоска часто спадаються. Головчасті волоски двох типів: з двоклітинною головкою на короткій одноклітинній ніжці і з одноклітинною кулевидною або овальною головкою на довгій багатоклітинній ніжці.
Мікропрепарат листка конвалії: клітини епідермісу прямостінні, витягнуті по довжині листка. Продихи занурені, округлі, орієнтовані по довжині листка, оточені 4 клітинами епідермісу (тетраперигенний тип). Під верхнім епідермісом видно клітини палісадної тканини, витягнуті по ширині листка (“лежача” палісадна тканина). Губчата тканина пухка і складається з розгалужених клітин, витягнутих по ширині листка. В окремих клітинах мезофілу видно пучки тонких рафід і крупні голчасті кристали (стилоїди) оксалату кальцію.
Мікропрепарат листка горицвіту весняного: клітини епідермісу великі з сильнозвивистими стінками, трохи витягнуті по довжині дольки. Стінки клітин верхнього епідермісу іноді мають вервицеподібні потовщення, кутикула поздовжньоскладчаста. Продихи тільки на нижній стороні, великі, овальні, злегка виступають над поверхнею листка, орієнтовані вздовж пластинки листка (аномоцитний тип). Зрідка зустрічаються одноклітинні волоски двох типів: довгі, стрічковидні із заокругленою верхівкою, звужені біля основи; короткі булавовидні волоски, різко звужені біля місця прикріплення. Всі волоски із спірально-складчастою кутикулою, прикріплені до дуже маленької округлої клітини епідермісу.
Мікропрепарат листка жовтушника розлогого: клітини верхнього епідермісу злегка звивисті або багатокутні, нижнього – звивистостінні. Стінки клітин верхнього епідермісу біля основи волосків мають вервицеподібні потовщення. Продихи дрібні, овальні, на нижній стороні їх значно більше, (навколопродиховий комплекс анізоцитного типу). Одноклітинні, розгалужені, грубобородавчасті, дво-п’ятикінцеві волоски покривають листок з обох сторін. Форма волосків різноманітна, на верхньому боці переважають трикінцеві, а на нижній, особливо по головній жилці і біля основи листка, - більшість волосків двокінцеві. Волосок від епідермальної (материнської) клітини перегородкою не відділений.
ЗАВДАННЯ 3. Ознайомитися з приготуванням витяжки із рослинної сировини та її очисткою. Готову очищену витяжку з ЛРС, що вміщує серцеві глікозиди студенти отримують на занятті від лаборанта, яку отримували наступним чином:
5г повітряно-сухої сировини поміщали в колбу з притертим корком, заливали 50мл 70% розчину етанолу (метанолу) і залишали на 24 години для екстракції серцевих глікозидів. Водно-спиртову витяжку відфільтровували через кусочок вати, спирт відігнали під вакуумом. Водний залишок перенесли в ділильну лійку і провели очистку шляхом збовтування з 10 мл вуглецю (IV) хлоридом. Із очищеної витяжки серцеві глікозиди двічі (по 10 мл) екстрагували сумішшю етилового або ізопропілового спирту і хлороформу у співвідношенні (1:3). Спиртово-хлороформну витяжку відфільтрували через паперовий фільтр з нанесеним на нього шаром безводного сульфату натрію. Фільтр промивали 5мл екстрагенту і промивну рідину приєднали до основного фільтрату. З одержаної витяжки відігнали розчинник до об'єму 5-10 мл, залишок перенесли у фарфорову чашку і випарили досуха. Сухий залишок розчинили в 5 мл спирту. Одержана витяжка готова для дослідження на наявність серцевих глікозидів.
ЗАВДАННЯ 4. Провести виявлення серцевих глікозидів у витяжці за допомогою якісних реакцій.
І. Реакції виявлення п’ятичленного лактонного кільця серцевих глікозидів:
Реакція Бальє. До 1 мл досліджуваного розчину додайте 0,5 мл 1% розчину пікринової кислоти і 5 крапель 10% розчину натрію гідроксиду. Зафіксуйте в протоколі результат реакції.
Реакція Легаля. До 1 мл витяжки додайте рівний об'єм 1 % розчину натрію нітропрусиду і 2-3 краплі 10% розчину натрію гідроксиду. Вміст пробірки перемішайте і спостерігайте зміну забарвлення.
Реакція Розенгейма. До 1 мл спиртового екстракту додайте 1 мл 90%-го розчину трихлороцтової кислоти в метанолі (або етанолі). Відмітьте зміну забарвлення.
II. Реакція виявлення стероїдного ядра.
Реакція Лібермана-Бурхарда. 1 мл витяжки випаріть в чашці досуха. Залишок розчиніть в 0,5 мл оцтового ангідриду, перенесіть в суху пробірку і обережно по стінках пробірки нашаруйте 0,5 мл концентрованої сірчаної кислоти. Спостерігайте появу забарвленого кільця на межі шарів двох рідин. Реакцію виконуйте під витяжною шафою і з обережністю!
Реакція Раймонда. До 1 мл спирто-водного екстракту додайте 0,5 мл м-динітробензолу (3%-й розчин м-динітробензолу в бензолі) і перемішайте. Додайте 2-3 краплини спиртового розчину калію гідроксиду.
ІІІ. Реакція виявлення дезоксицукрів.
Реакція Келлера-Кіліані. 1 мл досліджуваної витяжки випарте в чашці досуха. Залишок розчиніть в 0,5 мл концентрованої оцтової кислоти, яка вміщує 3% розчин хлориду заліза (III) і перенесіть в суху пробірку. Після чого обережно по стінках нашаровуйте 0,5 мл концентрованої сірчаної кислоти, яка вміщує 3% розчин хлориду заліза (III). Реакцію виконуйте під витяжною шафою, дотримуйтесь правил техніки безпеки.
Результати реакцій опишіть в протоколі.
ЗАВДАННЯ 5. Провести виявлення серцевих глікозидів у витяжці за допомогою хроматографії.
На стартову лінію хроматографічної пластинки з тонким шаром силікагелю КСК або хроматографічного паперу нанесіть з мікропіпетки 0,02 мл витяжки і розчинів вірогідних взірців серцевих глікозидів (свідки). Пластинки з нанесеними речовинами помістіть у хроматографічну камеру, насичену однією з систем розчинників: етилацетат-хлороформ (90:10); етилацетат-метанол (80:5); хлороформ-метанол-формамід (18:19:1). Після підняття фронту розчинників на висоту 10-12 см, хроматограму підсушіть у сушильній шафі при температурі 50-60°С. Висушені пластинки оприскуйте (під витяжкою) із пульверизатора послідовно 0,2% розчином хлораміну-Т і 25% спиртовим розчином трихлороцтової кислоти, після чого нагрійте протягом 5 хв при температурі 120°С (нагрівання проводьте під тягою у витяжній шафі!). Вирахуйте величини Rf плям глікозидів досліджуваної витяжки і порівняйте з Rf "свідків". Зробіть висновки про їх ідентичність.
ЗАВДАННЯ 6. Теоретично розібрати біологічний метод кількісного визначення серцевих глікозидів у сировині за ДФ XI, Т. 2.-С. 253-256, 300-303, 314-317.
Підсумковий контроль та захист виконаної роботи. Проводиться на основі перевірки правильності оформлення протоколу, результатів реакції, представлених студентом разом з протоколом, виявлення отриманих практичних навиків шляхом усного опитування студента методик виконання дослідів, трактовки отриманих результатів, а також за мнемокартами хімічної структури серцевих глікозидів.
Лабораторна робота № 7
ТЕМА: Тритерпеноїди. Стероїди. Сапоніни.
АКТУАЛЬНІСТЬ: Сапоніни – високомолекулярні складні органічні сполуки глікозидного характеру, які проявляють специфічні властивості: водні розчини з сировини, що вміщує сапоніни, утворюють сильну піну; потрапляючи в кров, викликають гемоліз еритроцитів; токсичні для холоднокровних тварин. ЛРС, що вміщує сапоніни проявляє муколітичні, сечогінні, протимікробні, протизапальні властивості. Деякі види ЛРС, що вміщує терпенові сапоніни має стимулюючий вплив на ЦНС. Знання та навички, здобуті студентами при вивченні даної теми, будуть корисними в практичній діяльності провізора.
НАВЧАЛЬНІ ЦІЛІ:
ЗНАТИ:
правила і терміни збору, способи первинної обробки, сушіння
та зберігання сировини, що вміщує сапоніни;
діагностичні зовнішні та мікроскопічні ознаки ЛРС, що вміщує сапоніни;
використання ЛРС, що вміщує сапоніни в медицині;
хімічну структуру тритерпенових і стероїдних сапонінів;
фізичні і хімічні властивості сапонінів;
використання ЛРС і препаратів з неї в медицині.
ВМІТИ:
встановити тотожність лікарських рослин, що вміщують
сапоніни за зовнішніми ознаками (за допомогою гербарних зразків) та відрізняти їх від морфологічно подібних видів;
встановити тотожність ЛРС за зовнішніми ознаками та визначником.;
ідентифікувати ЛРС за діагностичноми мікроскопічними ознаками;
САМОСТІЙНА ПОЗААУДИТОРНА РОБОТА
Сапоніни, поширення їх в рослинному світі, локалізація в органах рослин.
Вкажіть способи використання та застосування ЛРС, що вміщує сапоніни і лікарських препаратів з неї в медицині та фармації.
Класифікація, фізико-хімічні властивості. Методи отримання сапонінів з рослинної сировини .
Збір, сушіння, зберігання і переробка ЛРС, яка вміщує сапоніни. Шляхи використання і застосування сировини в медицині.
Назвіть на латинській та українській мові рослини, ЛРС та їх родини, що вміщують сапоніни. Опишіть зовнішній вигляд лікарських рослин: солодка гола, астрагал шерстистоквітковий, синюха блакитна, мильнянка лікарська, хвощ польовий, аралія маньчжурська, ортосифон тичинковий, женьшень, заманиха висока, діоскорея ніппонська, якірці сланкі, гуньба сінна, остудник голий.
Охарактеризуйте зовнішні ознаки ЛРС, що вміщує сапоніни. Вкажіть фенофази, методи збору, способи сушіння, первинної обробки та правила зберігання ЛРС: корінь солодки, трава астрагалу, кореневища з коренями синюхи, корінь мильнянки, трава хвощу польового, корінь аралії маньчжурської, листя ортосифону тичинкового, корінь женьшеню, кореневища з коренями заманихи, кореневища з коренями діоскореї.
Опишіть мікроскопічні ознаки ЛРС: корінь солодки, кореневища з коренями синюхи, трава хвощу польового.
