
- •Часть I
- •Часть I – номенклатура органических соединений; углеводороды; галогениды углеводородов; кислородсодержащие органические соединения.
- •Часть II – азотсодержащие и биоорганические соединения.
- •Предисловие
- •Тема 1. Номенклатура и изомерия органических соединений.
- •Тема 1. Номенклатура и изомерия алканов, циклоалканов и алкенов
- •Методические указания по выполнению заданий темы 1
- •Названия функциональных групп для [м.Н.]
- •Международная (iupac) номенклатура органических соединений – [м.Н.]
- •Общая схема международного названия [м.Н.]
- •Последовательность действий при получении [м.Н.] любого органического соединения:
- •Рациональная номенклатура (р.Н.)
- •Построение структурных формул по номенклатурным названиям
- •Построение структурных формул изомеров по брутто-формуле (б.Ф.)
- •Задание 1
- •Задание 2
- •Химические свойства и способы получения оРганических соединений различных классов (Темы 2–9)
- •Величины относительных электроотрицательностей (оэо) для некоторых элементов (по л. Полингу)
- •10 Типов (*) органических реакций (по изменению состава и структуры исходного органического вещества в сравнении с продуктом)
- •* Не путать понятия:
- •Методические указания по выполнению заданий в темах 2–5: углеводороды (ув) и их галогенопроизводные (Hal-ув)
- •I. Некоторые общие правила реагирования
- •1) Зайцева (отщепления и замещения – нiii→hii→hi) (см. Стр. 6).
- •II. Некоторые именные реакции
- •III. Приемы получения углеводородов различных классов и их галогенопроизводных
- •2. Галогенирование (внедрение атома Hal в органическую молекулу)
- •IV. Принадлежность соединения к определённому классу – качественная реакция на функциональную группу
- •V. Примеры некоторых видов заданий
- •1. Цепь химических превращений с определением типов реакций
- •2. Схема реакций превращения (Вещество а → Вещество б)
- •3. Установление структуры органического вещества по его б.Ф. И заявленному набору химических свойств
- •4. Различить изомеры
- •5. Разделение смеси органических веществ
- •Тема 2. Алканы, цикланы и алкены: химические свойства и способы получения; Типы органических реакций Задание 1
- •Задание 2
- •Тема 3. Алкины, алкадиены и циклоалкены: Номенклатура, изомерия, получение, химические свойства; типы органических реакций Задание 1
- •Задание 2
- •Задание 3
- •Тема 4. Арены: Номенклатура, изомерия, получение, химические свойства; типы органических реакций Задание 1
- •Задание 2
- •Задание 3
- •Тема 5. Галогенопроизводные углеводородов: Получение, химические свойства; типы органических реакций; Синтезы углеводородов различных классов через галогениды Задание 1
- •Задание 2
- •Кислородсодержащие органические соединения: химические свойства и способы получения Методические указания по выполнению заданий в темах 6–9:
- •II. Приемы получения функциональных групп
- •1. Получение группы (-он) спиртов
- •Названия карбоновых кислот, их солей и сложных эфиров
- •2. Получение фенолов
- •3. Получение оксогрупп
- •4. Получение карбоксилов (соон)
- •5. Именные реакции кислородсодержащих соединений
- •6. Качественные реакции на о-содержащие функциональные группы
- •Тема 6. Оксисоединения Задание 1
- •Задание 2
- •Задание 3
- •Тема 7. Оксосоединения: Номенклатура, изомерия, получение, химические свойства; типы органических реакций Задание 1
- •Задание 2
- •Задание 3
- •Тема 8. Карбоновые кислоты: Номенклатура, изомерия, получение, химические свойства; типы органических реакций Задание 1
- •Задание 2
- •Задание 3
- •Тема 9. Функциональные и радикальные производные карбоновых кислот Задание 1
- •Задание 2
- •Оглавление
II. Некоторые именные реакции
Вюрца синтез – сдваивание алифатических радикалов.
![]()
Вюрца-Фиттига синтезы с участием ароматических Hal-УВ
Гриньяра синтезы несимметричных углеводородов
![]()
Фриделя-Крафтса синтезы (алкилирование и ацилирование аренов с катализатором AlCl3)

Вильямсона синтезы (взаимодействие металл- и галогенсодержащих органических соединений)
![]()
Кучерова реакция (гидратация алкинов)

III. Приемы получения углеводородов различных классов и их галогенопроизводных
1. Получение кратных (С=С) и (СС) связей
вицинальное отщепление H-Hal действием спиртового раствора щелочи на галогениды углеводородов (см. I, 6а);
внутримолекулярная дегидратация спиртов действием H2SO4 (конц.) при t оС;
дегалогенирование вицинальных дигалогенидов (Zn или Mg).
2. Галогенирование (внедрение атома Hal в органическую молекулу)
(а) замещение атомов Н в соответствии с правилом Зайцева (последовательное замещение дает галогениды геминальной структуры:
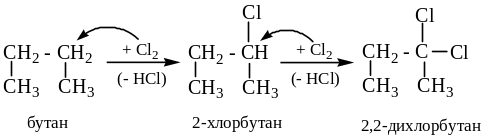
(б) высокотемпературное замещение -Н в алкенах:

(в) дигалогениды геминальной структуры получаются присоединением двух молекул H–Hal по (СС) связи (см. I, 4б)
(г) дигалогениды вицинальной структуры образуются присоединением Hal2 по (С=С) связи
(д) галогенирование ароматических УВ в разных условиях:
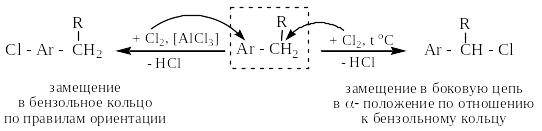
(е) замещение (ОН) и (=О) на атомы хлора действием PCl5 или SOCl2:
![]()

IV. Принадлежность соединения к определённому классу – качественная реакция на функциональную группу
1. Тесты на непредельность: (С=С) и (СС)
(а) обесцвечивание раствора Вr2;
(б) обесцвечивание раствора КMnО4 (окисление)
2. Тесты на малые циклы (ц-С3 и ц-С4):
(а) обесцвечивают раствор Br2;
(б) не обесцвечивают раствор KMnO4 (устойчивы к окислению).
3. Наличие связи (С=С) – образование осадка озонида:
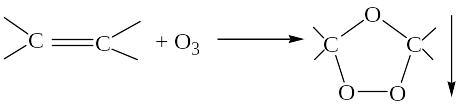
4. Наличие ацетиленидного водорода в алкин-1 (R – C CH): появление осадка ацетиленида (R–C≡CMe↓) с [Аg(NН3)2]ОН, [Cu(NH3)2]Cl или NaNH2 (качественная реакция на ацетиленидный водород).
Алкин-2 (R – C C – R) такого осадка не даёт.
5. Обнаружение карбонильного кислорода (в альдегидах и в кетонах):
(а) осадки с Н2N-Х (оксимы с H2N–OH, гидразоны с Н2N–NН2 или фенилгидразоны с Н2N–NH–C6H5);
(б) осадки с NаНSO3 (бисульфитные производные).
6. Обнаружение альдегидной группы:
альдегид
кислота
![]() ;
;
(б) реакция «медного зеркала»:

Кетоны этих реакций не дают.
7. Обнаружение фенолов:
(а) яркое окрашивание с раствором FeCl3 ;
(б) растворяются в щелочах (реагируют);
Спирты (в том числе и ароматические) со щелочами не реагируют.
8. Обнаружение спиртов (две последовательные реакции):

V. Примеры некоторых видов заданий
1. Цепь химических превращений с определением типов реакций
![]()
Для каждого превращения сначала определить тип реакции и «рвущиеся» связи. Затем определить «места» замещения, отщепления или присоединения атомов реагирующих молекул, показать себе стрелками места замещения или присоединения, а обводами – уходящие пары атомов. Из этого сразу становится понятен вид продукта реакции:
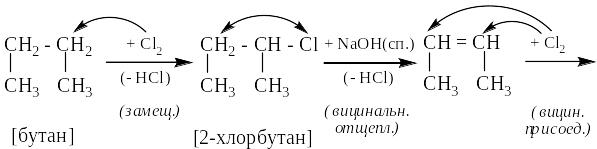
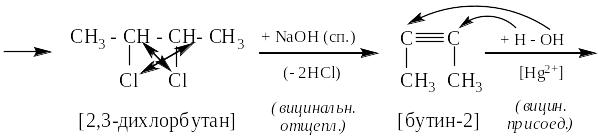
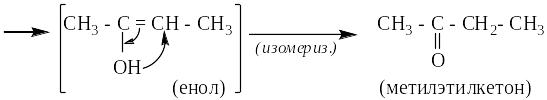
Здесь использованы: главные химические свойства классов органических соединений (реакция замещения для алканов, вицинального присоединения для непредельных углеводородов), реакции получения дополнительных связей вицинальным отщеплением и правило неустойчивости енолов.
