
- •Дефекты кристаллической решетки
- •Перемещение атомов в твердых и жидких телах
- •Структура и свойства оксидов железа
- •Термодинамика восстановления оксидов железа
- •Особенности восстановления оксидов при наличии растворов
- •Восстановление оксидов находящихся в растворе
- •Переход продукта восстановления в раствор
- •Кинетика и механизм восстановления оксидов
- •Современные представления о механизме восстановления оксидов
- •Внешняя диффузия газа
- •Диффузия газа в порах кускового материала
Внешняя диффузия газа
Диффузия вещества, как известно, обусловлена различной его концентрацией в различных частях системы, и вещество переносится в направлении от большей концентрации к меньшей. В этом случае диффузия подчиняется двум законам Фика [уравнения (2.3)—(2.5) |. Такую диффузию часто называют молекулярной или свободной диффузией. Коэффициенты свободной диффузии газоввосстановителей в бинарных смесях и длины свободного пробега молекул приведены в табл. 2.5. Коэффициент диффузии газов 1 и 2 в бинарной смеси определяется формулой
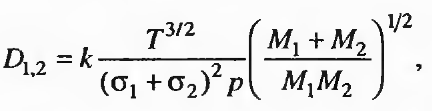 (2,49)
(2,49)
где Т— температура, р — давление, М1, и М2 —молярные массы газов 1 и 2; о, и с2— диаметры молекул газов 1 и 2, нм; к— коэффициент, зависящий от размерности величин.
При постоянной температуре коэффициент диффузии изменяется обратно пропорционально общему давлению смеси или сумме концентраций компонентов смеси. Рост температуры вызывает увеличение коэффициента диффузии пропорционально tв степени 3/2 (при постоянном давлении) или 1 в степени 1/2 (при постоянном количестве газа в единице объема). Замеры показывают, что в реальных смесях при постоянном давлении коэффициент диффузии пропорционален 1™ (где m = 1,5—2,0).
Кроме того, при движении газа, обтекающего частицы железорудного материала, происходит конвективная диффузия, которая обусловлена разной плотностью в отдельных участках системы. Такая диффузия наблюдается только в подвижной среде, для нее скорость в значительной степени зависит от характера движения потока, который может быть ламинарным и турбулентным.
Таблица 2.5
Коэффициент диффузии газов Dr,см2/с (числитель) и длина свободного пробега молекул Л-10-5, см (знаменатель), в бинарных газовых смесях (р= 98 кПа)
t,°с |
co+n2 |
h2+n2 |
н2+н2о |
со+со2 |
500 |
1,09/2,64 |
3,68/3,34 |
4,64/3,57 |
0,95/2,63 |
700 |
1,65/3,58 |
5,51/4,44 |
6,91/4,76 |
1,51/3,71 |
900 |
2,30/4,52 |
7,64/5,62 |
9,58/6,01 |
2,20/4,91 |
1100 |
3,05/5,53 |
10,06/6,84 |
12,62/7,32 |
3,01/6,22 |
При ламинарном режиме отдельные струи газа перемещаются параллельно твердой поверхности, и перенос диффундирующего вещества из среды к поверхности твердого тела и обратно (перпендикулярно потоку газа) осуществляется молекулярной диффузией. Турбулентный режим характеризуется беспорядочным движением небольших объемов газа, скорость которых непрерывно меняется по величине и направлению. Концентрация вещества в объеме в результате перемешивания сравнительно быстро выравнивается, но у твердой поверхности всегда имеется малоподвижный тонкий слой, где сохраняются ламинарный режим и градиент концентрации газа. Этот пограничный (или диффузионный) слой создает наибольшее сопротивление переносу газа, так как в нем протекает сравнительно медленная молекулярная диффузия. Следовательно, перенос определяется переходом газа через эту пленку, а наблюдаемая скорость диффузии (или диффузионный поток Г) — уравнением
![]() (2.50)
(2.50)
Уравнение (2.50) получают из выражения (2.3) при условии, что толщина пограничного слоя /, концентрации газа на границах пограничного слоя являются постоянными и равными С,, и С2, а количество газа, входящего и выходящего из пограничного слоя, постоянно. В этом случае концентрация газа в пограничном слое меняется от Cj до С2 линейно.
При оценке внешнего переноса обычно пользуются критериями подобия. Критерий Рейнольдса характеризует соотношение сил вязкости и инерции в движущейся среде:
![]() (2.51)
(2.51)
где р — плотность среды; и — скорость среды; d— характеристический размер потока; г] — коэффициент динамической вязкости.
Критерий Пекле характеризует соотношение количества вещества, переносимого за счет конвекции (udC/dx) и диффузии D d2C/dx2\
Ре = ud/D, (2.52)
где D— коэффициент диффузии газа.
При большом значении Ре молекулярной диффузией можно пренебречь по сравнению с конвективной. При Re«1, наоборот, пренебрегают конвективной диффузией по сравнению со свободной.
Критерий Шмидта является диффузионным критерием (аналогичен критерию Прандтля для теплообмена):
![]() (2.53)
(2.53)
где
v
=
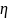 /p
— коэффициент кинематической вязкости.
/p
— коэффициент кинематической вязкости.
Для газов Sc~ 1 и Ре ~ Re.
Если
обозначить D/1
=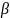 получим
получим
![]() (2.54)
(2.54)
Величину Р называют коэффициентом массопередачи. Он зависит от всех величин, определяющих скорость переноса, кроме концентраций, и по аналогии с коэффициентом пропорциональности в выражении закона действия масс его иногда называют константой скорости диффузии. При турбулентном движении Р имеет характер эмпирического коэффициента и его значение зависит от газодинамической обстановки процесса. С повышением скорости потока газа и степени его турбулентности толщина пограничного слоя газа уменьшается, а величина коэффициента массопередачи возрастает.
Связь массообмена с газодинамикой потока может быть выражена эмпирической функцией
l/d=ARe,Sc). (2.55)
При сопоставлении этой величины с формулой коэффициента массообмена можно получить критерий Шервуда (аналогичный критерию Нуссельта для теплообмена):
Sh= р d/D. (2.56)
В этих выражениях d— характеристическое расстояние, обозначающее размер обтекаемого газом сферического куска. Критерий Шервуда связан с критериями Рейнольдса и Шмидта следующим образом:
Sh = C + CRemScn, (2.57)
где С и С— константы.
Для случая, когда газ обтекает шарообразные куски, С = 2, при и = 0 величина Sh=2, С = 0,6. Для ламинарного потока т = 1/2, п = 1/3. Для турбулентного потока т = 0,5—0,8; п = 1/3. Отсюда коэффициент массопередачи приблизительно пропорционален квадратному корню из скорости газа.
Критерий Шмидта для чистых газов в зависимости от давления, температуры и типа газа составляет 0,6—0,8. Для газовых смесей критерий Шмидта, чаще всего, имеет меньшее значение, чем для чистых газов. Для смеси водорода и диоксида углерода (соотношение 1:1) Sc = 0,25 при 20 °С. С ростом доли более тяжелого компонента величина критерия Шмидта снижается, так как в интервале 50—100% С02 вязкость почти постоянна, плотность растет, a D12 остается почти постоянным. Для смесей Н2 = N2также характерно подобное явление.
До последнего времени шли споры о возможности лимитирующего влияния внешней диффузии на общую скорость восстановления железорудных материалов. Рассмотрим некоторые простые соотношения. Считаем, что процесс состоит из двух стадий: химической реакции и внешней диффузии.
Для описания совместного протекания химической реакции на поверхности и диффузии применяют различные приближенные методы. В одном из них методе равнодоступной поверхности, разработанном Д.А. Франк-Каменецким, принимается, что все участки реакционной поверхности одинаково доступны для диффузии; диффузия и химическая реакция протекают последовательно и независимо друг от друга; концентрация газа-восстановителя одинакова на всей поверхности. Это возможно при отсутствии глубоких и мелких пор в реагирующем твердом теле. Вся реакционная поверхность может рассматриваться как внешняя.
Для простых химических реакций изменение скорости
(![]() 2.58)
2.58)
где с — концентрация газа-восстановителя на поверхности оксида; к — константа скорости реакции; и — порядок реакции.
Для процесса на единице наружной поверхности беспористого материала, когда п = 1, можно записать
![]() (2.59)
(2.59)
где С0 — концентрация газа-восстановителя в ядре потока.
Равенство скоростей последовательных звеньев (диффузии и реакции) и наблюдаемой скорости процесса при установившемся режиме обосновано, например, H.JI. Гольдштейном, тогда
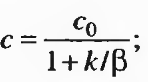 (2.60)
(2.60)
![]() (2.61)
(2.61)
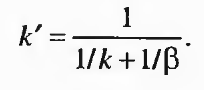
(2.62)
Ее удобнее выразить через обратные величины, т.е.
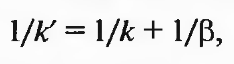 (2.63)
(2.63)
где первое слагаемое характеризует химическое, а второе — внешнедиффузионное звено процесса.
Из уравнения (2.63) следует, что обратная величина наблюдаемой константы скорости процесса восстановления равна сумме обратных значений констант скоростей последовательных звеньев процесса. Такой вывод, полученный для реакции, состоящей из двух стадий, применим в простейшем случае (если все звенья имеют первый порядок) к системам с любым числом последовательных звеньев.
Если константа скорости характеризует пропускную способность того или иного звена, то обратное ее значение представляет собой сопротивление этого звена. Следовательно, уравнение (2.63) показывает, что общее сопротивление протеканию процесса равно сумме сопротивлений последовательных звеньев. Необходимо отметить, что это явление аналогично законам построения электрических цепей.
При фильтрации газа через слой частиц или обтекании отдельных кусков по формуле Сокольского
![]()
(2.64)
повышение
линейной скорости газа приводит к
увеличению наблюдаемой константы
скорости процесса, которая стремится
к постоянному значению, когда
внешнедиффузионное сопротивление
![]() становится
пренебрежимо малым по сравнению с
химическим сопротивлением.
становится
пренебрежимо малым по сравнению с
химическим сопротивлением.
Однако эти представления, хотя и широко распространены в литературе, не подтверждаются наблюдаемой количественной связью скорости процесса с расходом газа, которая показывает, что при малых расходах газа скорость процесса возрастает в гораздо большей мере, чем это следует из указанной формулы. Наряду с этими данными (H.JI. Гольдштейна, К.К. Шкодина и др.) результаты опытов Ю.П. Свинцова, К.К. Шкодина показали, что при изменении линейной скорости газа в случае постоянного его расхода скорость процесса вообще не меняется.
Таким образом, при реальных условиях процесса восстановления и фильтрации газом слоя кусковых железорудных материалов внешняя диффузия не может лимитировать процесс восстановления, а влияние массового расхода газа на скорость процесса следует объяснять иными факторами, что будет рассмотрено ниже.
Между прочим, отсутствие тормозящего влияния внешней диффузии можно проиллюстрировать другими рассуждениями.
Если иметь в виду, что критерий Нусселъта
![]() (2.65)
(2.65)
где а — коэффициент теплопередачи, Дж/(см2 с-К); А, — коэффициент теплопроводности, ДжДсм с К); d—характеристическая величина размера твердого тела, см, а критерий Прандтля
![]() (2.66)
(2.66)
где v — кинематическая вязкость газа, см2/с; а — температуропроводность, см2/ с, то можно пересчитать критерий Нуссельта в критерий Шервуда, используя зависимости этих критериев от Re,и соответственно определить значение коэффициентов массообмена Р и теплопередачи а.
Поскольку константа С в уравнениях
![]() (2.67)
(2.67)
должна иметь для равных геометрических соотношений одинаковое численное значение, получаем
![]() . (2.68)
. (2.68)
По данным И.С. Куликова и др.,
![]() (2.69)
(2.69)
Откуда
![]() (2.70)
(2.70)
Следовательно,
![]() Если
Если
![]() то
то
![]() Температурная
зависимость других звеньев процесса
значительно сильнее. Именно поэтому
сколько-нибудь заметное влияние внешнего
массопереноса на общую скорость
восстановления может проявиться при
очень высоких температурах.
Температурная
зависимость других звеньев процесса
значительно сильнее. Именно поэтому
сколько-нибудь заметное влияние внешнего
массопереноса на общую скорость
восстановления может проявиться при
очень высоких температурах.
