
- •Дефекты кристаллической решетки
- •Перемещение атомов в твердых и жидких телах
- •Структура и свойства оксидов железа
- •Термодинамика восстановления оксидов железа
- •Особенности восстановления оксидов при наличии растворов
- •Восстановление оксидов находящихся в растворе
- •Переход продукта восстановления в раствор
- •Кинетика и механизм восстановления оксидов
- •Современные представления о механизме восстановления оксидов
- •Внешняя диффузия газа
- •Диффузия газа в порах кускового материала
Кинетика и механизм восстановления оксидов
Современные представления о механизме восстановления оксидов
Для практических целей недостаточно знать, что исследуемая реакция принципиально возможна, о чем нам сообщает термодинамика. Не менее важно иметь сведения о времени (скорости) протекания данной реакции. Восстановление оксидов, как правило, сложный и многостадийный процесс, включающий в себя разнообразные самостоятельные явления со всеми присущими лишь им закономерностями. Переплетение этих закономерностей создает достаточно сложную общую картину, которую, чаще всего, крайне трудно расшифровать.
В общем случае при рассмотрении любого восстановления приходится решать два основных вопроса: во-первых, в какой среде проходит акт химического взаимодействия, приводящего к отнятию кислорода от оксида (от этого зависит та или иная последовательность отдельных стадий процесса); во-вторых, в зависимости от схемы процесса, какая сталия является самой медленной, определяющей общую скорость процесса восстановления в целом.
В общем случае взаимодействие, сопровождающееся отнятием кислорода от оксида металла, может происходить в газовой фазе, на границе металл—оксид или низший оксид—высший оксид. Иногда основное место взаимодействия меняется во время протекания реакции, еще более затрудняя ее анализ. Однако чаще всего полагают неизменным место отнятия кислорода от оксида; основные теории восстановления оксидов металлов исходят из этого основного предположения. А.А. Байков одним из первых предложил цельную схему механизма восстановления оксидов:
МеО = Me + 1/2О2;
В + 1/2О2 - ВО;
МеО + В = Me + ВО.
Процесс состоит из двух стадий: диссоциации оксида металла МеО и окисления восстановителя В кислородом оксида. Несомненные преимущества этой модели — простота и удобство для расчетов. Время возникновения теории — первое двадцатилетие XX века, но и сейчас эта схема широко применяется при расчетах расходов тепла при восстановительных процессах и составлении тепловых балансов этих процессов.
Накопление экспериментальных данных привело к выводу о малой роли диссоциации оксидов в процессе восстановления, так как реальные упругости диссоциации оксидов, служащие, как известно, мерой их прочности, малы настолько, что ими можно пренебречь. Чем ниже упругость диссоциации, тем прочнее оксид. Так, lg рFе0 при 700 и 1700 °С составляет соответственно —20,8 и —6,9; lg PMg0-32,7 и —12,3 и т. д. Такими же свойствами обладает большинство оксидов, за исключением некоторых высших оксидов отдельных металлов. Например, при диссоциации 3Fe203= 2Fe304+1/2O2 равновесное парциальное давление кислорода становится равным атмосферному при 1383 °С, при диссоциации ЗМn203 = 2Mn304+1/2O2— при 940 °С, а при диссоциации 2Мn02 = Мn203 + 1/2O2 — даже при 460 °С. Однако таких оксидов очень мало.
Современная трактовка вопроса термической диссоциации оксидов, по И.С. Куликову, заключается в следующем. Если исходная система кроме оксида содержит и металл в виде чистых конденсированных фаз, то равновесные парциальные давления кислорода в реакциях диссоциации и образования оксида одинаковы. Если же в исходной системе присутствует только оксид, то продукт диссоциации — металл — может образоваться и в конденсированном, и в газообразном состоянии. Для получения металла в конденсированном состоянии необходимо, чтобы давление его пара, образовавшегося при диссоциации оксида, было не меньше давления насыщенного пара над твердым или жидким металлом при данной температуре. Если конденсация не происходит и металл остается в газовой фазе, константа равновесия реакций диссоциации и образования оксида различна и величина, принимаемая за упругость диссоциации, не является мерой прочности оксида.
Наряду с этим следует иметь в виду, что диссоциация не обязательно проходит по схеме: МеО = Me + У202. Возможно протекание диссоциации, например, с образованием атомарного кислорода: МеО — Me + О.
Существует мнение, что участие атомарного кислорода в диссоциации часто бывает значительным и даже преимущественным. В качестве примера ниже приведена сводка реакции диссоциации Si02(числитель — кДж; знаменатель — кДж/моль газа):
Реакция:  Н
Н

С учетом того, что наиболее вероятна реакция, характеризующаяся минимальным тепловым эффектом, отнесенным к молю газообразного продукта, предпочтительнее протекание восьмой реакции, а не второй, как обычно принимают. Эта трактовка роли диссоциации разработана еще недостаточно, однако расчеты показывают, что при температурах ниже 1300 °С диссоциация низших оксидов железа и марганца не играет заметной роли.
В середине 1930-х годов появилось новое представление о механизме восстановления оксидов, известное под названием адсорбционно- автокаталитической теории. В ее разработке активное участие принимали Г.И. Чуфаров, О.А. Есин, П.В. Гельд, С.Т. Ростовцев. Это представление можно выразить в виде схемы
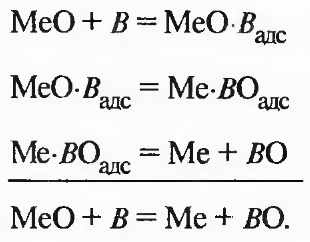
Реакция восстановления проходит в три стадии: адсорбция газа- восстановителя на поверхности восстанавливаемого оксида, химическая реакция на поверхности оксида, десорбция продукта восстановления. В адсорбционно-автокаталитической теории местом взаимодействия считается граница газ—поверхность оксида, автокатализ в некоторых случаях был обнаружен на раннем этапе восстановления.
В основу новой теории положена необходимость прямого контакта газа-восстановителя с восстанавливаемым оксидом металла. Это позволило применить для оценки механизма и кинетики восстановления известные закономерности из физической химии, физики и химии поверхности. Таким образом, были объяснены непонятные ранее такие опытные результаты, как данные Стальхане и Мальмберга о непропорционально значительном влиянии добавок окислителей (С02 и Н20) на скорость реакций восстановления. В этом случае новая теория выделила роль адсорбции и показала, что молекулы некоторых газообразных продуктов восстановления, являясь более активными адсорбентами, занимают наиболее активные места поверхности восстанавливаемого оксида, резко снижая степень и скорость восстановления. Можно привести и другие примеры.
Однако получение новых экспериментальных данных, особенно с помощью новейших методов исследований, непрерывно выявляло ограниченность адсорбционно-авгокаталитической теории. Известно, что адсорбционная способность веществ с ростом температуры снижается. Для получения надежных результатов эксперименты разработчик адсорбционно- автокаталитической теории проводил при низких температурах, но это не соответствовало реальным условиям металлургических процессов. Роль процессов доставки газа-восстановителя к поверхности железорудного материала и отвода продуктов восстановления не отрицалась, но оценивалась недостаточно. Имелись некоторые методические ошибки в экспериментах.
Современные представления о механизме восстановления кусков железорудного материала подчеркивают, прежде всего, многообразие процессов, происходящих при восстановлении. Среди них следует подчеркнуть, к сожалению, недооцениваемую до настоящего времени роль твердофазных процессов — реакций и диффузии в твердых телах. Практически для всех условий (начиная со степени восстановления 50—60%) процессы в твердой фазе лимитирующие. Необходимо отметить, что наиболее развиты представления о механизме восстановления единичного куска газом-восстановителем. Мало теоретических и экспериментальных разработок, направленных на выявление процессов восстановления газом слоя кусков, восстановления твердым восстановителем твердых и жидких оксидов, восстановления газом жидких оксидов. Поэтому авторы уделили основное внимание восстановлению единичных кусков газообразным восстановителем. Этот объект является наиболее важным для практики, так как подавляющая доля металла, внедоменного восстановления, получается при твердофазном восстановлении кускового материала газом. Для этого процесса характерна определенная последовательность этапов восстановления. В пространстве между кусками железорудного материала и в крупных порах кусков течет газ-восстановитель. Вокруг отдельных кусков и около поверхности макропор образуются граничные потоки газа.
Массообмен между газовой фазой и восстанавливаемым оксидом невозможен без транспорта реагентов (восстановителя и продукта восстановления) через этот граничный слой. Затем газ-восстановитель для контакта с поверхностью куска должен диффундировать по микропорам куска, а также через слой образовавшихся твердых продуктов восстановления внутрь куска. Газообразные продукты восстановления должны тем же путем отводиться от места реакции. Далее газ-восстановитель должен вступить в контакт с оксидом железа, т. е. должна произойти адсорбция газа на поверхности твердой фазы. На этой поверхности протекает собственно реакции восстановления, которая включает в себя отнятие кислорода от оксида, образование и рост зародышей продуктов восстановления — магнетита, вюстита или железа. Последующий рост слоя продуктов реакции происходит путем твердофазных реакций и диффузии в твердой фазе.
Таким образом, восстановление оксидов есть сумма отдельных процессов, каждый из которых характеризуется собственным равновесием. Движущий силой отдельных этапов служит отклонение от этих равновесий. Например, мера движущей силы диффузии есть падение концентраций (или давления) реагентов в начале и конце диффузионного пути. В общем случае восстановление оксидов складывается из следующих стадий: подвод газа-восстановителя к куску железорудного материала (или внешняя диффузия газа); диффузия газа-восстановителя по порам куска к его поверхности; адсорбция газа-восстановителя на поверхности оксида; диффузия газа-восстановителя или ионов в твердой фазе; собственно химическое взаимодействие с отнятием кислорода от молекулы оксида; образование зародышей металлической фазы; десорбция продуктов восстановления; отвод продуктов восстановления из пор куска. Поскольку любая из стадий может лимитировать процесс восстановления по скорости, рассмотрим кратко названные этапы.
