
- •Дефекты кристаллической решетки
- •Перемещение атомов в твердых и жидких телах
- •Структура и свойства оксидов железа
- •Термодинамика восстановления оксидов железа
- •Особенности восстановления оксидов при наличии растворов
- •Восстановление оксидов находящихся в растворе
- •Переход продукта восстановления в раствор
- •Кинетика и механизм восстановления оксидов
- •Современные представления о механизме восстановления оксидов
- •Внешняя диффузия газа
- •Диффузия газа в порах кускового материала
Термодинамика восстановления оксидов железа
Процесс восстановления железа из оксидов по принципу Байкова о последовательности превращений протекает ступенчато путем последовательного перехода от высших оксидов к низшим по схеме Fe203—>Fe304—» FeO —>Fc (выше 570 °C) или Fe203—> Fe304-» Fe (ниже 570 °C). При этом в соответствии с диаграммой Fe —» О в системе возникают не только низшие оксиды и металл, но и твердые растворы.
Приведем реакции восстановления оксидов железа газообразными восстановителями:

Каждая из этих реакций является трехкомпонентной и трехфазной, т. е. обладает двумя степенями с вободы. Следовательно, из четыре;; величин, характеризующих состояние системы (общее давление, температура, парциальное давление восстановителя и продукта восстановления), лишь чве могут произвольно меняться. Остал^.гые же являются их функцией. Учитывая, что по принципу Ле-Шателье равновесие не зависит от общего давления, полу гаем
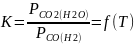 (2-15)
(2-15)
Поэтому систему можно считать моновариантной. Для реакций
(2.9)и (2.12) соответственно:
![]() (2.16)
(2.16)
Реакции (2.9) и (2.12) характеризуются очень низкими содержаниями восстановителя в равновесной газовой среде и практически являются необратимыми. Для реакций (2.10) и (2.13):
![]() (2.17)
(2.17)
Поскольку эти реакции идут с поглощением тепла, константы их равновесия растут с повышением температуры, т. е. содержание СО и Н2 в равновесной смеси падает. Реакция (2.11) сопровождается выделением тепла, в результате чего равновесие с ростом температуры смещается влево:
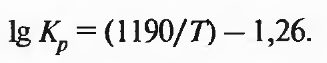 (2.18)
(2.18)
Реакция (2.14) эндотермична, поэтому равновесие с ростом температуры смещается вправо:
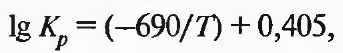 (2.19)
(2.19)
а с учетом нестехиометричности вюстита
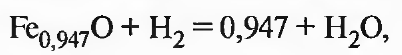 (2.20)
(2.20)
![]() (2.21)
(2.21)
Реакции восстановления магнетита до железа:
Fe304+ 4СО = 3Fe + 4С02; (2.22)
Fe304+ 4Н2 = 3Fe + 4Н20. (2.23)
Реакция (2.22) сопровождается выделением, а (2.23) — поглощением тепла. Суммарный тепловой эффект восстановления оксидов железа оксидом углерода (реакции (2.9)—(2.11)) слабо положительный (-230 кДж/кг железа), а водородом ((2.12)—(2.14)) — отрицательный (~880 кДж/кг железа).
Графическое изображение условий равновесия реакций
—(2.14) приведено на рис. 2.4. Каждая из линий на диаграмме соответствует изменению равновесного состава газовой фазы в зависимости от температуры для реакций (2.9)—(2.14), (2.22), (2.23); линии соответствуют: а—b (2.22); b—f(2.10); b—d(2.11); a'—b'(2.23); b'—/(2.13); b’—d’ (2.14). Линий, соответствующих равновесию реакций (2.9) и (2.12), на диаграмме нет, поскольку они близки к оси абсцисс. Диаграмма дает сведения о составе газа, который необходим для полного восстановления оксидов железа.
Рис.
2.4.
Диаграмма
равновесия в системах Fe—О—СО
и Fe—О—Н2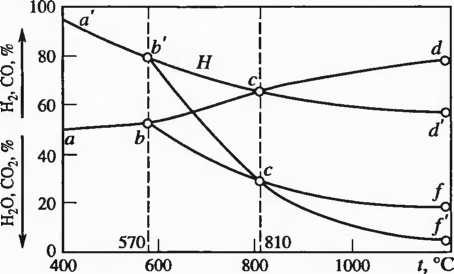
С учетом избытка газавосстановителя реакции (2.10), (2.11), (2.13) и (2.14) принимают вид:
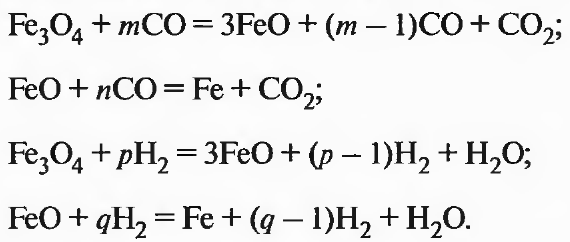
Для реакции (2.11) при 800 °С равновесный состав газа содержит -70% СО и 30% С02, тогда К = 1/(n—1) = 30/70; п = 10/3. Таким образом, требуется не 1 моль восстановителя, а 3 1/3 моля.
Из данных рис. 2.4 следует, что газ, который не может быть использован для восстановления FeO, может восстановить Fe304 до FeO, что делает возможным протекание реакций восстановления высших оксидов железа до FeO при пониженных температурах в начале процесса восстановления, например в верхней части шахтной восстановительной печи.
Анализ кривых равновесия реакций восстановления оксидов железа оксидом углерода показывает, что процесс можно условно разделить на «легкую» и «трудную» части, к первой можно отнести восстановление высших оксидов железа, ко второй — восстановление FeO. Для протекания реакций (2.9), (2.10) требуются невысокие содержания газа-восстановителя в газовой среде. Восстановление FeO возможно при высокой концентрации СО в газовой фазе, причем с ростом температуры величина необходимого избытка восстановителя возрастает.
Рис.
2.5.
Диаграмма
равновесия в системе Fe—О—Н2
с учетом
нестехиометричности
вюстита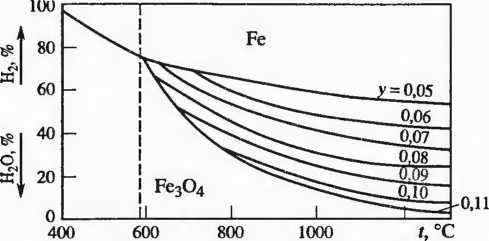
Геакиии (2.9)—(2.14) и рис. 2.4 иллюстрируют различия в термодинамике восстановления оксидов железа оксидом углерода и водородом. К основным из них надо отнести следующее. При температурах <810 °С водород является более слабым восстановителем, чем СО, поскольку равновесная концентрация водорода в смеси превышает равновесное содержание оксида углерода. При температуре >810 °С водород становится более сильным восстановителем. Суммарный тепловой эффект реакций восстановления оксидов железа водородом отрицательный и в 4 раза выше суммарного положительного эффекта реакций восстановления оксидов железа оксидом углерода.
Приведенные данные относятся к идеальным системам. В реальных условиях воздействие неучитываемых факторов (образование твердых растворов и др.) меняет приведенные данные. Так, положение линий равновесия восстановления вюстита Fe^O меняется в зависимости от доли вакансий ионов железа у в решетке вюстита при восстановлении водородом (рис. 2.5). Восстановление оксидов железа твердым углеродом возможно по следующим реакциям:
3Fe203+ С = 2Fe304+ СО - 129,07 МДж; (2.24)
Fe304 + C = 3Fe0 + СО- 187,28 МДж; (2.25)
FeO + С = Fe + СО - 152,67 МДж. (2.26)
Для реакции (2.26)
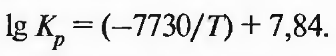 (2.27)
(2.27)
Суммарный отрицательный тепловой эффект 4240 кДж/кг железа.
В присутствии твердого углерода при анализе восстановления оксидов железа следует учитывать равновесие в системе С—СО—С02:
С02 + С = 2С0-166,32 МДж. (2.28)
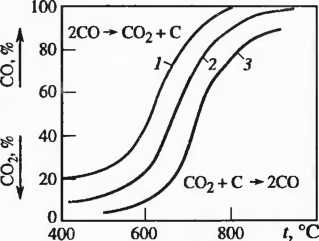
Рис. 2.6. Диаграмма равновесия в системе С—СО—С.02 при давлении, кПа:
1-50; 2- 100; 3- 150
Равновесие реакции (2.28), которую называют реакцией газификации углерода или реакцией Белла—Будуара, зависит от давления. При повышении давления равновесие сдвигается влево. На рис. 2.6 приведена диаграмма равновесных линий реакции (2.28). Реакция (2.28) является обратимой. Левее равновесной кривой реакция идет в направлении распада оксида углерода, т. е.
2СО = С02 + С + 166,32 МДж, (2.29)
правее — в направлении его образования:
С02 + С = 2СО - 166,32 МДж. (2.30)
Поскольку равновесие реакции зависит от давления, на рис. 2.6 приведена не одна линия равновесного состава газа, а семейство линий. Прямая реакция (2.30) протекает при высоких температурах, поэтому она отличается высокой скоростью и быстротой достижения равновесия. Реакция распада оксида углерода (2.29) протекает медленно: для достижения равновесия необходимо длительное время. Несколько ускоряет (как катализатор) эту реакцию свежевосстанов- ленное железо. Газ в восстановительной печи пребывает 3—15 с, этого времени достаточно для достижения равновесия в области высоких температур и недостаточно для достижения равновесия в низкотемпературной области. Поэтому газ в области высоких температур почти целиком состоит из СО, а газ, покидающий шахтную печь для металлизации, имеет 15—16% С02 и 19—20% СО или в пересчете на сумму СО + С02 40—45% С02 и 55—60% СО, что значительно отличается от равновесных данных. При высоких температурах газ содержит малое количество С02, так как скорость реакции С02 + С = 2СО велика. В связи с этим реакция восстановления при наличии твердого восстановителя и высоких температурах протекает с затратой твердого углерода, а продуктом восстановления является оксид углерода. Отсюда реакцию восстановления можно записать следующим образом:
FeO + СО — Fe + С02
С02 + С = 2СО
FeO + С = Fe + СО. (2.31)
Исходя из вида газообразного продукта восстановления, по аналогии с доменной плавкой различают прямое и непрямое (косвенное) восстановление. Восстановление, в ходе которого продуктом является СО, называют прямым, а восстановление, в ходе которого образуются С02 или Н20, — косвенным. С этой точки зрения реакцию С02 + С = - 2СО можно также рассматривать как прямое восстановление (если углекислота не является продуктом диссоциации карбонатов).
Реакция (2.31) является удобной схемой для объяснения механизма прямого восстановления. Действительно, трудно представить протекание суммарной реакции прямого восстановления в изображенном виде. В этом случае (реакция в твердой фазе) следовало бы считаться с невозможностью протекания реакции в большем объеме из-за малой протяженности контактных поверхностей оксидов железа и углерода. В действительности же эта реакция при высоких температурах проявляется достаточно сильно, что свидетельствует о том, что кислород от оксида отделяется газом (СО или Н2).
Однако механизм прямого восстановления в достаточной мере еще не расшифрован. Обычно принимают (в согласии с экспериментальными данными), что косвенное восстановление соответствует умеренным температурам (до 900—1000 °С), а прямое — высоким.
Выше рассмотрены особенности прямого восстановления при отсутствии твердых растворов. Появление твердых растворов изменяет реакцию (2.28) в том смысле, что частично вместо чистого углерода появляется связанный или растворенный в железе углерод. В выражении для определения константы равновесия
К~Рсо2ас/Рсо (2.32)
величина ас уже не будет равна единице, как принимают для реакции (2.28), так как активность растворенного углерода не равна единице и зависит (при небольших давлениях) от температуры и концентрации углерода в железе. Если ас< 1 (углерод, растворенный в железе), то при равных давлениях и температуре газовая фаза содержит меньше СО, чем по реакции 2СО = С + С02. Иными словами, линии равновесия в этом случае будут располагаться на графике правее и ниже по сравнению с линией, соответствующей реакции газификации чистого графита (рис. 2.7).
Рис.
2.7.
Полная
диаграмма равновесия систем Fe—О—СО
и С—СО—С02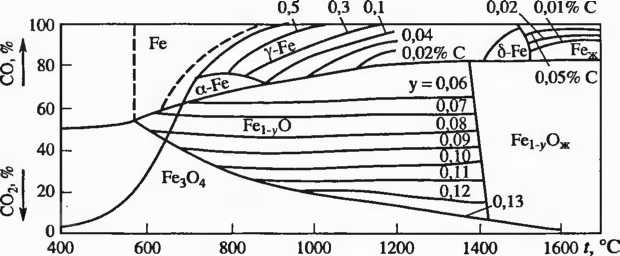
Если образуется карбид Fe3C, то активность углерода в нем больше, чем у графита, что также вызывает смещение линий равновесного состава газа, но на этот раз влево и вверх. Таким образом, для определения газовой фазы, равновесной к растворам углерода в железе, необходимо знать зависимость а от концентрации углерода в железе и от температуры. Активность углерода в у железе
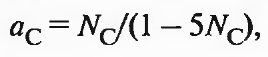 (2.33)
(2.33)
где Nq— молярная концентрация углерода, доли единицы.
На рис. 2.7 изображена полная диаграмма восстановления оксидов железа в присутствии твердого углерода, учитывающая твердые и жидкие растворы.
В шихтовых материалах оксиды железа могут находиться в виде сложных соединений и твердых растворов. Вюстит может образовывать твердые растворы с MnO, MgO и СаО. Так, при 1100 °С СаО максимально растворяет 15% FeO, а вюстит — 28% СаО. Оксид железа Fe304образует твердые растворы с кубическими шпинелями (например, с Мп304). До 5% оксида хрома растворяется в вюстите при 1350 °С и образует с вюститом соединение FeCr203, которое, в свою очередь, образует непрерывный рад твердых растворов с магнетитом.
В виде химических соединений оксиды железа присутствуют в соединениях с известью (ферриты кальция и магния) и кремнеземом (фаялит, оливины и др.). В общем случае активность оксидов железа в соединениях и растворах снижается, и в равновесной газовой смеси должна расти доля восстановителя (СО и Н2). Восстановление силикатов железа оксидом углерода при низких температурах практически не идет, т. е.:
Fe2Si04+ 2СО = 2Fe + Si02+ 2С02; (2.34)
lg Кр = (-65/7) - 1,55(298-900 К), (2.35)
lg Кр = (-510/7) - 2,01(900-1478 К). (2.36)
Силикаты железа восстанавливаются в основном прямым путем:
Fe2Si04+ 2С = 2Fe + Si02+ 2СО; (2.37)
для восстановления тверд зго силиката
lg Кр = (-17900/7) + 16,88, (2.38)
для восстановления жидкого силиката
lg Кр = (-14700/7) + 14,45. (2.39)
При восстановлении силикатов железа в области высоких температур возможна следующая схема:
Fe2Si04= 2FeO + Si02— 47,46 МДж 2FeO + 2СО = 2Fe + 2C02 + 27,30 МДж 2C02 + 2C = 4CO - 332,64 МДж
Fe2Si04 + 2C = 2Fe + Si02 + 2CO - 352,80 МДж (2.40)
или 3150 кДж/кг железа. В случае прямого восстановления вюстита расходуется 2730 кДж/кг железа. Таким образом, восстановление силикатов железа требует дополнительного расхода горючего на компенсацию отрицательного теплового эффекта реакций и проведение процесса восстановления. При плавке на основных шлаках
Fe2Si04+ 2СаО + 2С = Ca2Si04+ 2Fe + 2СО - 352,80 МДж. (2.41)
Присутствие извести значительно улучшает условия восстановления силикатов.
